Cobalto para niños
Datos para niños Hierro ← Cobalto → Níquel |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Información general | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | Cobalto, Co, 27 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie química | Metales de transición | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 9, 4, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atómica | 58,933200 u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [Ar] 3d7 4s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Mohs | 4,1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
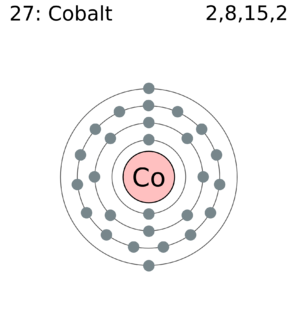
| Electrones por nivel | 2, 8, 15, 2 (imagen) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | Metálico con tono gris | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio medio | 135 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 1.88 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calc) | 152 pm (radio de Bohr) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 126 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado(s) de oxidación | 5, 4 , 3, 2, 1, -1 (anfótero) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.ª energía de ionización | 760,4 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.ª energía de ionización | 1648 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.ª energía de ionización | 3232 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4.ª energía de ionización | 4950 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Líneas espectrales | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado ordinario | Sólido (ferromagnético) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | 8900 kg/m3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusión | 1768 K (1495 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullición | 3200 K (2927 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de vaporización | 376,5 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de fusión | 16,19 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor | 175 Pa a 1768 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varios | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | Hexagonal | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor específico | 420 J/(kg·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 100 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 4720 m/s a 293,15 K (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos más estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Isótopos del cobalto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Valores en el SI y condiciones normales de presión y temperatura, salvo que se indique lo contrario. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El cobalto (símbolo Co) es un elemento químico con el número atómico 27. Se encuentra en el grupo 9 de la tabla periódica de los elementos. Su nombre viene del alemán kobalt, que se relaciona con los "Duendes" (kobolds). Los mineros de la Edad Media en Sajonia creían que estos duendes embrujaban el mineral. Pensaban que parecía mena de cobre, pero no producía este metal con los métodos usuales.
El cobalto tiene una masa atómica de 58,9332. Es un metal con propiedades magnéticas parecidas a las del hierro. Es duro, resistente y soporta bien el calor. Podemos encontrar cobalto en el agua dulce, la tierra, las plantas, los meteoritos y en los nódulos de manganeso en el fondo del océano. Los compuestos de cobalto se usan para dar un color azul intenso a vidrios, cerámicas y esmaltes.
Algunas de sus características son:
- Número atómico: 27
- Masa atómica: 58,93 g/mol
- Densidad: 8,9 g/ml
- Punto de ebullición: 2900 °C
- Punto de fusión: 1495 °C
Contenido
- ¿De dónde viene el nombre Cobalto?
- ¿Cómo es el Cobalto?
- Historia del Cobalto
- ¿Cómo se produce el Cobalto?
- ¿Para qué se usa el Cobalto?
- Compuestos de Cobalto
- Isótopos del Cobalto
- ¿Por qué es importante el Cobalto para los seres vivos?
- Precauciones con el Cobalto
- El Cobalto en la Tecnología Moderna
- El Cobalto en Argentina
- Véase también
¿De dónde viene el nombre Cobalto?
En la Edad Media, los mineros llamaban a este metal kobold. Creían que era un metal sin valor. Pensaban que un duende bueno (un kobold) lo ponía en lugar de la plata que había robado. En el diccionario castellano del siglo XVIII, ya aparece como cobalt.
¿Cómo es el Cobalto?
El cobalto es un metal ferromagnético, lo que significa que puede ser atraído por imanes. Tiene un color blanco azulado. A menudo se encuentra junto al níquel. Ambos elementos suelen estar presentes en los meteoritos de hierro.
El cobalto es muy importante para los mamíferos, incluyendo a los humanos, aunque solo se necesita en pequeñas cantidades. El Co-60, un tipo especial de cobalto, se usa en medicina y para revisar la calidad de los metales.
El cobalto metálico puede tener dos formas diferentes en su estructura cristalina: hexagonal y cúbica. La temperatura a la que cambia de una forma a otra es de 722 K (449 °C).
Se usa mucho en superaleaciones de alto rendimiento. Estas aleaciones son muy duras y resistentes al desgaste. El cobalto se mezcla con otros metales, como el cromo, para hacerlos más fuertes. Aunque son muy buenas, estas aleaciones suelen ser caras. El cobalto se parece mucho al hierro y al níquel en sus propiedades.
El cobalto es menos común y más caro que el hierro y el níquel. No se usa tanto en la industria como ellos. Es un elemento que tiene poca resistencia química, pero es más estable que el hierro en el aire y el agua, siempre que no haya otros elementos que lo corroan.
Historia del Cobalto
Desde hace muchos siglos, los compuestos de cobalto se han usado para dar un color azul intenso al vidrio, los esmaltes y la cerámica. Se ha encontrado cobalto en esculturas egipcias y joyas persas de hace más de 3000 años. También se halló en las ruinas de Pompeya y en China, en las dinastía Tang y dinastía Ming.
El cobalto se ha usado para colorear el vidrio desde la Edad del Bronce. Se encontró un lingote de cristal azul con cobalto en un barco hundido del siglo XIV a. C.. El cristal azul más antiguo con cobalto es de la dinastía XVIII de Egipto. No se sabe exactamente de dónde sacaban el cobalto en esos tiempos.
El químico sueco George Brandt descubrió el elemento cobalto entre 1730 y 1737. Él demostró que era un elemento nuevo, diferente del bismuto y otros metales. Brandt también descubrió que el cobalto era el que daba el color azul al vidrio, algo que antes se creía que hacía el bismuto. El cobalto fue el primer metal descubierto en la historia reciente, ya que los metales conocidos antes (como el hierro, cobre, plata, oro, etc.) no tienen un descubridor registrado.
El nombre kobalt viene de los mineros. Ellos no apreciaban este mineral porque era difícil de trabajar. Además, los minerales de cobalto suelen contener arsénico. Al intentar fundirlos, se liberaba óxido de arsénico, que es muy tóxico. Esto hacía que los mineros lo vieran como un mineral problemático.
Durante el siglo XIX, gran parte de la producción mundial de azul cobalto (un tinte) y esmalte se hacía en la fábrica noruega Blaafarveværket. Luego, se descubrieron grandes yacimientos de cobalto en Nueva Caledonia en 1864, y más tarde en Ontario, Canadá (1904), y en la provincia de Katanga en el Congo (1914). Estos nuevos descubrimientos cambiaron la forma en que se obtenía el cobalto en el mundo.
En 1938, John Livingood y Glenn Seaborg descubrieron el cobalto-60. La primera máquina de radioterapia que usaba cobalto-60, llamada bomba de cobalto, se usó en Canadá en 1951. Este equipo se puede ver hoy en el Saskatoon Cancer Centre.
Después de la Segunda Guerra Mundial, Estados Unidos buscó asegurarse un buen suministro de cobalto. Encontraron una fuente importante en Idaho, cerca del cañón Blackbird.
La única refinería de cobalto en Iberoamérica se construyó en San Pablo, Brasil, en 1981.
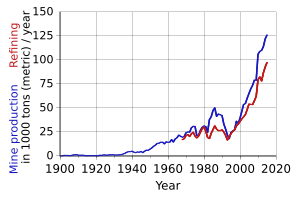
¿Cómo se produce el Cobalto?
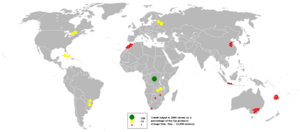
En 2005, la República Democrática del Congo fue el mayor productor de cobalto, con casi el 40% de la producción mundial. La situación política en el Congo puede afectar mucho el precio del cobalto.
Hoy en día, la República Democrática del Congo sigue siendo el mayor productor. Empresas de Gran Bretaña y China controlan gran parte de la producción. Las empresas del Congo solo controlan una pequeña parte.
El proyecto de la Montaña Mukondo en Katanga podría ser la reserva de cobalto más grande del mundo. Se estima que podría producir un tercio del cobalto mundial.
Existen varios métodos para separar el cobalto de otros metales como el cobre y el níquel. Estos métodos dependen de cuánto cobalto hay en el mineral. Uno de ellos es la flotación por espuma, donde se usan sustancias para separar los componentes del mineral. Después, el mineral se calienta (se tuesta) para convertirlo en sulfato de cobalto. Finalmente, este óxido se convierte en metal puro.
| 1. | 3.500.000 | |
| 2. | 1.400.000 | |
| 3. | 600.000 | |
| 4. | 500.000 | |
| 5. | 260.000 | |
| 6. | 250.000 | |
| 7. | 220.000 | |
| 8. | 100.000 | |
| 9. | 80.000 | |
| 10. | 69.000 | |
| 11. | 47.000 | |
| 12. | 13.000 |
Fuente: USGS
¿Para qué se usa el Cobalto?
El cobalto se usa en muchas industrias y para diversas cosas:
- Para crear aleaciones industriales muy fuertes.
- Para dar color azul permanente a vidrios, cerámicas y porcelanas.
- En radiografía industrial para revisar la calidad de los metales y encontrar grietas.
- En superaleaciones para turbinas de gas de aviación y herramientas de corte.
- Para fabricar imanes y cintas magnéticas.
- En la Catálisis del petróleo y en la industria química.
- Para recubrir metales y darles un buen aspecto, dureza y resistencia a la oxidación.
- Como secante en pinturas, barnices y tintas.
- Como base para esmaltes vitrificados.
- En pigmentos como el azul cobalto y el verde cobalto.
- En electrodos de baterías eléctricas.
- En cables de acero para neumáticos.
- El Co-60 se usa como fuente de radiación gamma en tratamientos médicos, para esterilizar alimentos y en radiografía industrial.
Compuestos de Cobalto
El cobalto puede formar muchos compuestos diferentes. Esto se debe a que puede tener varios estados de oxidación. Los óxidos de cobalto, como el CoO y el Co~3~O~4~, son antiferromagnéticos a bajas temperaturas.
Isótopos del Cobalto
Un isótopo es una versión de un elemento con diferente número de neutrones. Se conocen 22 radioisótopos de cobalto. Los más estables son el Co-60, Co-57 y Co-56. Tienen vidas medias de 5,2714 años, 271,79 días y 70,86 días, respectivamente. Los demás isótopos radiactivos duran mucho menos.
El cobalto-60 se usa en tratamientos médicos especiales. Produce dos tipos de rayos gamma. Es una fuente de energía útil, pero después de unos 5 años, aunque ya no se use, sigue siendo muy radiactivo y debe manejarse con cuidado.
¿Por qué es importante el Cobalto para los seres vivos?
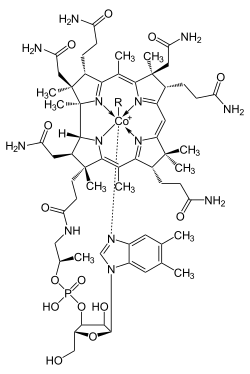
El cobalto es un elemento esencial para todos los animales, incluyendo a los humanos. Es parte de una vitamina muy importante llamada cobalamina (Vitamina B12). Si un animal no tiene suficiente cobalto, puede desarrollar anemia. Sin embargo, es muy raro que los humanos tengan falta de cobalto, ya que se necesita muy poco y se encuentra en varios alimentos.
Las proteínas que usan cobalamina tienen un anillo especial que mantiene unido el cobalto.
Precauciones con el Cobalto
El cobalto metálico en polvo muy fino puede ser inflamable. Los compuestos de cobalto deben manejarse con cuidado porque el metal puede ser ligeramente dañino.
El Co-60 es radiactivo. La exposición a su radiación debe manejarse con mucho cuidado. Si se respira mucho cobalto, puede causar problemas en los pulmones como asma y neumonía, especialmente en personas que trabajan con él.
Los alimentos que contienen partículas de cobalto también pueden ser dañinos, sobre todo los vegetales que crecen en suelos contaminados. Esto puede causar:
- Vómitos y náuseas
- Problemas de visión
- Problemas del corazón
- Daño en la tiroides
El Cobalto en la Tecnología Moderna
El cobalto es muy útil en la tecnología por su estabilidad, dureza, resistencia a la corrosión y a las altas temperaturas. Por eso, es ideal para fabricar dispositivos electrónicos como teléfonos inteligentes, computadoras y tabletas.
En las baterías de estos aparatos, el cobalto se usa en el electrodo positivo (cátodo). Gracias al cobalto, las baterías pueden almacenar mucha más energía, hasta tres veces más, y durar más tiempo. El cobalto ayuda a que el litio en las baterías funcione mejor, aumentando su autonomía.
A medida que buscamos un futuro con menos contaminación, las baterías con cobalto serán más importantes. Ayudarán a que los vehículos eléctricos funcionen y a almacenar la energía renovable.
Un desafío es que la mayoría de los vehículos eléctricos usan baterías grandes con cobalto, y la producción de este metal es limitada. Más de la mitad del cobalto del mundo se encuentra en la República Democrática del Congo, una región que a veces es inestable. Reutilizar las baterías de litio es difícil y no se hace mucho. Los expertos creen que el reciclaje no tendrá un gran impacto hasta dentro de muchos años. Se están investigando nuevas formas de hacer cátodos para baterías sin cobalto.
El cobalto también se usa en imanes de ferrita, que se encuentran en radios, altavoces, microondas y discos duros. Otros imanes que usan cobalto son los de Alnico (con aluminio y níquel), que son muy resistentes y soportan altas temperaturas. Se usan en motores eléctricos y en la industria aeroespacial.
Actualmente, las superaleaciones de cobalto se están usando para fabricar vehículos espaciales y estaciones orbitales.
El Cobalto en Argentina
En Argentina se descubrió un nuevo mineral llamado cobaltomenita, también conocido como cobalto criollo. Fue encontrado por Emile Bertrand en un depósito en Cacheuta, Mendoza. Este mineral se obtiene como un subproducto al procesar minerales de cobre y níquel.
Argentina tiene importantes yacimientos de cobalto en lugares como Las Águilas (San Luis), King Tut (La Rioja) y La Niquelina-Esperanza (Salta).
El cobalto es muy importante en Argentina para la medicina y la agricultura. Dioxitek, una empresa estatal, produce cobalto-60. Argentina es uno de los principales exportadores de cobalto-60 a nivel mundial. Gracias a estas ventas, Dioxitek ha podido invertir en tecnología.
El cobalto-60 es muy útil en la agricultura para conservar alimentos. Ayuda a mantener los productos frescos sin necesidad de usar fumigantes o conservantes químicos. Esto aumenta el valor de los alimentos que Argentina exporta.
La demanda de cobalto ha crecido mucho debido al aumento de los coches eléctricos. En 2017, el precio del cobalto subió un 235%. Cada coche eléctrico necesita entre ocho y doce kilos de cobalto. Se espera que la demanda siga creciendo.
En 2020, Argentina exportó $767 en cobalto, siendo el exportador número 87 del mundo. Francia fue el principal destino. Argentina también importó $1,18 millones en cobalto ese año.
Véase también
 En inglés: Cobalt Facts for Kids
En inglés: Cobalt Facts for Kids
- Cobalto-60