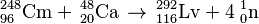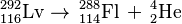Livermorio para niños
Datos para niños Moscovio ← Livermorio → Teneso |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Información general | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | Livermorio, Lv, 116 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie química | Metales del bloque p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 16, 7, p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atómica | 291 u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [Rn] 5f14 6d10 7s2 7p4 (predicción) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
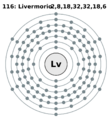
| Electrones por nivel | 2, 8, 18, 32, 32, 18, 6 (predicción) (imagen) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 175 (estimado) pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado(s) de oxidación | 2, 4 (predicción) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos más estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Isótopos del livermorio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El livermorio es un elemento sintético de la tabla periódica. Su símbolo es Lv y su número atómico es 116. Esto significa que cada átomo de livermorio tiene 116 protones en su núcleo.
Su nombre se eligió en honor al Laboratorio Nacional Lawrence Livermore, un importante centro de investigación en Livermore, California, Estados Unidos.
Contenido
El Livermorio: Un Elemento Creado por el Hombre
El livermorio no se encuentra de forma natural en la Tierra. Es un elemento "sintético", lo que significa que ha sido creado por científicos en laboratorios especiales. Es un elemento muy pesado y, como muchos de estos elementos, es inestable y se descompone muy rápido.
¿Cómo se Descubrió el Livermorio?
La historia del descubrimiento del livermorio es un buen ejemplo de cómo funciona la ciencia.
En el año 2000, un grupo de científicos del Laboratorio Nacional Lawrence Berkeley en Estados Unidos anunció que habían logrado crear el elemento 116. Publicaron sus hallazgos en una revista científica. Sin embargo, al intentar repetir el experimento, no pudieron obtener los mismos resultados. Esto llevó a que, en 2002, el director del laboratorio anunciara que los datos originales no eran correctos. Este suceso nos enseña lo importante que es la verificación y la repetición en la ciencia.
Poco después, en junio de 2000, otro equipo de científicos del Instituto Conjunto para la Investigación Nuclear, en Dubna, Rusia, tuvo éxito. Ellos crearon un isótopo del livermorio (llamado 292Lv) al bombardear átomos de curio-248 con iones de calcio-48 usando un ciclotrón (una máquina que acelera partículas).
Este nuevo átomo de livermorio duró muy poco tiempo, solo unos 0,006 segundos, antes de transformarse en otro elemento más ligero, el Flerovio (Fl), mediante un proceso llamado desintegración alfa.
En 2001, el mismo instituto ruso logró crear un segundo átomo de livermorio. Estos experimentos ayudaron a confirmar que el livermorio es un elemento real y que sus propiedades se acercan a lo que los científicos esperaban.
Finalmente, en octubre de 2006, se realizaron más experimentos que confirmaron la existencia del livermorio. Al bombardear átomos de californio-249 con iones de calcio-48, se produjo el elemento 118 (Oganesón), que luego se descompuso rápidamente en livermorio. Esta confirmación fue muy importante para la comunidad científica.
La reacción principal para crear livermorio es:
Este isótopo de livermorio (292Lv) se descompone en 47 milisegundos en un isótopo de flerovio (288Fl):
¿Por qué se llama Livermorio?
Durante un tiempo, el livermorio tuvo un nombre temporal: "Ununhexio". La IUPAC (Unión Internacional de Química Pura y Aplicada), que es la organización encargada de nombrar los elementos, confirmó el nombre definitivo de Livermorio (Lv) el 8 de diciembre de 2011. Se eligió este nombre para honrar al Laboratorio Nacional Lawrence Livermore, donde se realizaron importantes investigaciones sobre este y otros elementos superpesados.
Propiedades del Livermorio
Como el livermorio es muy difícil de producir y se descompone rápidamente, los científicos no han podido medir directamente sus propiedades. Todo lo que sabemos sobre él son predicciones basadas en teorías y en el comportamiento de otros elementos de la tabla periódica.
Estabilidad Nuclear e Isótopos
El livermorio se encuentra cerca de una zona especial en la tabla periódica que los científicos llaman la "isla de estabilidad". Esta isla es un lugar donde se cree que algunos elementos superpesados podrían ser más estables y durar más tiempo de lo normal. Aunque los isótopos de livermorio que conocemos no están exactamente en el centro de esta isla, se acercan a ella. Los isótopos más pesados de livermorio tienden a durar un poco más.
Los elementos superpesados se crean mediante un proceso llamado fusión nuclear. Esto ocurre cuando dos núcleos atómicos se unen para formar uno más grande. Los científicos usan aceleradores de partículas, como los ciclotrones, para chocar átomos y lograr esta fusión.
Propiedades Físicas y Atómicas Predichas
El livermorio pertenece al grupo 16 de la tabla periódica, junto con el oxígeno, el azufre, el selenio, el telurio y el polonio. Se espera que tenga algunas propiedades similares a estos elementos.
Se predice que el livermorio será un metal denso. Su punto de fusión y punto de ebullición deberían ser más altos que los del polonio, pero su punto de ebullición más bajo.
Propiedades Químicas Predichas
Se espera que el livermorio se comporte químicamente de manera similar al polonio. Los científicos predicen que su estado de oxidación más común será +2, y que el estado +4 será menos estable. El estado +6, que es común en otros elementos de su grupo, probablemente no existirá para el livermorio debido a la forma en que sus electrones se organizan a velocidades muy altas (efectos relativistas).
También se cree que el livermorio formaría un compuesto con hidrógeno llamado livermorano (LvH2), que sería el "pariente" más pesado del agua (H2O).
Aplicaciones del Livermorio
Debido a que el livermorio es muy inestable, se descompone rapidísimo y es extremadamente difícil y costoso de producir, no tiene ninguna aplicación práctica en la industria o el comercio. Su único uso actual es en la investigación científica, donde ayuda a los científicos a entender mejor cómo se comportan los elementos superpesados y a explorar los límites de la tabla periódica.
Galería de imágenes
Véase también
 En inglés: Livermorium Facts for Kids
En inglés: Livermorium Facts for Kids