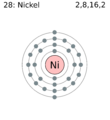
Níquel para niños
Datos para niños Cobalto ← Níquel → Cobre |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Información general | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | Níquel, Ni, 28 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie química | Metales de transición | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 10, 4, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atómica | 58,6934 u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [Ar] 3d8 4s2 [Ar] 3d9 4s1 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Mohs | 5,0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrones por nivel | 2, 8, 16, 2 o 2, 8, 17, 1 (imagen) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | Lustroso metálico | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio medio | 135 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 1,91 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calc) | 149 pm (radio de Bohr) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 121 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio de van der Waals | 163 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado(s) de oxidación | +3, +2, 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Óxido | Levemente básico | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.ª energía de ionización | 737,1 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.ª energía de ionización | 1753 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.ª energía de ionización | 3395 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4.ª energía de ionización | 5300 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Líneas espectrales | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado ordinario | Sólido (ferromagnético) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | 8908 kg/m3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusión | 1728 K (1455 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullición | 2730 K (2457 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de vaporización | 370,4 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de fusión | 17,47 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor | 237 Pa a 1726 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de compresibilidad | 180 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varios | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | Cúbica centrada en las caras | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor específico | 440 J/(kg·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad eléctrica | 14,3 × 106 S/m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 90,7 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Módulo elástico | 200 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de cizalladura | 76 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 4970 m/s a 293,15 K (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos más estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Isótopos del níquel | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Valores en el SI y condiciones normales de presión y temperatura, salvo que se indique lo contrario. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El níquel es un elemento químico con el número atómico 28 y el símbolo Ni. Se encuentra en el grupo 10 de la tabla periódica de los elementos.
Níquel: Un Metal Versátil
El níquel es un metal de transición muy útil. Es de color blanco con un ligero tono amarillo. Este metal es un buen conductor de la electricidad y el calor. Además, es muy dúctil y maleable, lo que significa que se puede estirar, pulir y moldear fácilmente.
Propiedades del Níquel
¿Cómo se ve y se siente?
El níquel tiene un brillo metálico. Es un metal denso, similar al hierro, el iridio y el osmio. A temperatura ambiente, el níquel es ferromagnético, lo que significa que puede ser atraído por un imán.
¿Es resistente a la corrosión?
Sí, el níquel es muy resistente a la corrosión (no se oxida fácilmente). Por eso, se usa a menudo como una capa protectora sobre otros metales. También se mezcla con hierro para hacer acero inoxidable, que es muy fuerte y no se oxida. Algunas aleaciones de níquel, como la aleación Monel, se usan para manejar productos químicos fuertes porque el níquel no reacciona fácilmente con ellos.
Historia del Níquel
El níquel se ha usado desde hace mucho tiempo, ¡aproximadamente desde el siglo IV a. C.! A menudo se encontraba junto al cobre en los minerales. Por ejemplo, en la antigua Siria, se encontraron bronces con más del 2% de níquel.
¿Quién lo descubrió?
En 1751, un científico llamado Axel Frederik Cronstedt estaba tratando de sacar cobre de un mineral llamado niquelina. En cambio, obtuvo un metal blanco que llamó níquel. Los mineros de la región de Hartz en Alemania solían culpar al "viejo Nick" (el diablo) cuando no podían trabajar ciertos minerales de cobre. El mineral que les causaba problemas era la niquelina, o Kupfernickel (que significa "diablo del cobre" en alemán). Así, el metal que Cronstedt descubrió en ese mineral recibió el nombre de níquel.
¿Dónde encontramos Níquel?
El níquel se encuentra en la naturaleza de varias formas. Se halla en meteoritos mezclado con hierro. También se cree que hay mucho níquel en el centro de la Tierra, en su núcleo, junto al hierro.
Producción Mundial
El níquel se extrae de diferentes minerales como la garnierita y la pentlandita. Los países que más níquel producen en el mundo son:
Níquel en los Coches Eléctricos
El níquel es muy importante para las baterías de los coches eléctricos. La producción de níquel para estos vehículos ha crecido mucho. Por ejemplo, Indonesia producía solo el 5% de este tipo de níquel en 2017, pero en 2022 ya producía el 50%. Se espera que para 2027 produzca el 80%.
¿Cómo se obtiene el Níquel?
El níquel se obtiene de los minerales a través de un proceso llamado metalurgia. Primero, los minerales se calientan y se reducen para obtener un metal con más del 75% de pureza. Para algunas aplicaciones, este níquel ya es suficiente.
Para obtener níquel más puro, se usan otros métodos. Uno de ellos es la hidrometalurgia, donde el mineral se disuelve en líquidos y luego se separa el níquel. Otro método es el electrorrefinamiento, que usa electricidad para purificar el níquel.
Usos del Níquel
El níquel es un metal muy demandado y esencial para la industria.
- Aproximadamente el 65% del níquel se usa para fabricar acero inoxidable.
- Otro 12% se usa en superaleaciones de níquel, que son metales muy resistentes.
- El resto se usa en baterías recargables, como catalizador en reacciones químicas, para hacer monedas y en recubrimientos metálicos.
Níquel en Monedas y Joyas
El níquel es muy común en las monedas de muchos países. A veces se usa puro, pero más a menudo se mezcla con cobre para hacer aleaciones como el cuproníquel. La primera moneda de níquel puro fue la de 20 céntimos de Suiza en 1881.
También se usa para hacer "oro blanco" en joyería. El níquel tiene un color blanco que ayuda a que las aleaciones parezcan blancas. Sin embargo, algunas personas pueden tener alergias al níquel. Por eso, en algunos lugares, como la Unión Europea, hay reglas sobre la cantidad de níquel permitida en productos que tocan la piel.
¿Es seguro el Níquel?
Es importante manejar el níquel y sus compuestos con cuidado. Por ejemplo, el gas llamado carbonilo de níquel es muy peligroso. Las personas que trabajan con níquel deben seguir normas de seguridad para evitar problemas de salud. Si eres alérgico al níquel, es mejor evitar el contacto directo con joyas o productos que lo contengan.
Galería de imágenes
-
Microscopía electrónica de un nanocristal de níquel en un nanotubo de carbono.
-
Nódulo de níquel electrolíticamente refinado, con sales de electrolito de níquel verdes y cristalizadas visibles en los poros.
-
Moneda de 5 centavos de peso mexicano acuñada en níquel puro.
Véase también
 En inglés: Nickel Facts for Kids
En inglés: Nickel Facts for Kids