Nivel energético para niños
Un nivel energético es como un escalón en una escalera para las partículas muy pequeñas, como los electrones dentro de un átomo. Imagina que los electrones no pueden estar en cualquier lugar, sino solo en ciertos "pisos" o niveles donde tienen una energía específica. Cada uno de estos "pisos" tiene un valor de energía permitido.
Contenido
Niveles de energía en los átomos
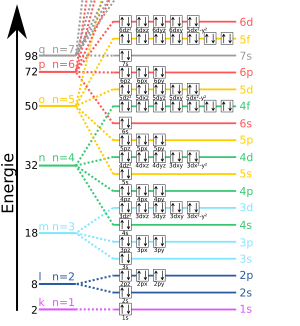
En la química y la teoría de los átomos, sabemos que los electrones que forman un átomo se organizan en "capas" o niveles de energía. Dependiendo de la capa en la que se encuentre un electrón, tendrá una cantidad de energía diferente. Por eso decimos que ocupa una capa de cierto nivel energético.
¿Por qué existen las capas de energía?
La existencia de estas capas se debe a dos razones principales:
- El principio de exclusión de Pauli: Este principio es como una regla que dice que en cada "piso" o capa de energía solo puede haber un número limitado de electrones. Es como si cada asiento en un autobús solo pudiera ser ocupado por una o dos personas, no más.
- Valores de energía permitidos: Los electrones solo pueden tener ciertas cantidades de energía, no cualquiera. Estos valores específicos son como los escalones de una escalera: solo puedes pisar los escalones, no el espacio entre ellos.
¿Cómo cambian los electrones de nivel?
Aunque un electrón no puede tener cualquier tipo de energía, sí puede cambiar de nivel. Si un electrón recibe energía (por ejemplo, de la luz o el calor), puede "saltar" a un nivel de energía más alto. Cuando esto sucede, el átomo se dice que está en un "estado excitado".
Sin embargo, estos estados excitados no duran mucho. Después de un corto tiempo, el electrón "cae" de nuevo a un nivel de energía más bajo. Cuando esto ocurre, el electrón libera la energía extra en forma de pequeñas partículas de luz llamadas fotones. La energía de estos fotones determina el color de la luz que se emite. Por ejemplo, cuando un electrón pasa de un nivel de energía más alto (E1) a uno más bajo (E2), la energía del fotón emitido es la diferencia entre esas dos energías.
¿Qué son los orbitales atómicos?
En la mecánica cuántica, las capas de energía se describen como orbitales atómicos. Un orbital atómico es una zona alrededor del núcleo del átomo donde es más probable encontrar un electrón. No es un camino fijo como el de un planeta alrededor del sol, sino más bien una "nube" de probabilidad. La forma de estas nubes depende de la energía del electrón.
Estos orbitales atómicos son muy importantes porque explican cómo los átomos se unen con otros átomos para formar diferentes sustancias. La forma en que los electrones se organizan en estos orbitales determina cómo reacciona un átomo.
Niveles de energía en las moléculas
Las mismas ideas que usamos para entender los niveles de energía en los átomos también se aplican a las moléculas. Una molécula es un grupo de átomos que se mantienen unidos. Dentro de una molécula, los electrones también tienen niveles de energía específicos, pero calcularlos es mucho más complicado que en un solo átomo.
Las diferentes formas de estudiar la luz y la materia, como la espectroscopia infrarroja o la espectroscopia ultravioleta-visible, nos permiten observar cómo los electrones y los átomos cambian entre estos niveles de energía. Por ejemplo, la espectroscopia infrarroja estudia los cambios en los niveles de energía relacionados con la vibración de las moléculas, mientras que la espectroscopia ultravioleta-visible estudia los cambios en los niveles de energía de los electrones.
Galería de imágenes
Véase también
 En inglés: Energy level Facts for Kids
En inglés: Energy level Facts for Kids