Desintegración alfa para niños
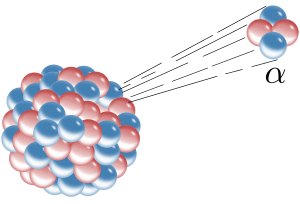
La desintegración alfa o decaimiento alfa es un tipo especial de cambio que ocurre en algunos núcleos atómicos muy pesados. Durante este proceso, un núcleo inestable libera una partícula alfa y se transforma en un nuevo núcleo, que es más ligero.
Una partícula alfa es como el núcleo de un átomo de helio 4. Está formada por dos protones y dos neutrones. Cuando un núcleo pesado emite una de estas partículas, su número másico (la cantidad total de protones y neutrones) disminuye en cuatro unidades, y su número atómico (la cantidad de protones) disminuye en dos unidades. Esto significa que el átomo original se convierte en un elemento químico diferente.
Este tipo de desintegración es común en elementos muy pesados, como el uranio. De hecho, casi todo el helio que encontramos en la Tierra se produce gracias a la desintegración alfa de elementos radiactivos que están en las rocas. Por eso, a veces se encuentra helio en lugares donde hay mucho uranio o torio, o como un subproducto en los pozos de gas natural.
Contenido
Desintegración Alfa: ¿Qué es y cómo funciona?
La desintegración alfa es un proceso natural en el que un núcleo atómico inestable se transforma. Es como si el núcleo "expulsara" una pequeña parte de sí mismo para volverse más estable.
Cómo Ocurre la Desintegración Alfa
Cuando un átomo pesado, como el uranio 238, se desintegra, libera una partícula alfa. Por ejemplo, el uranio 238 se convierte en torio 234 y una partícula alfa.
El Núcleo Atómico y las Partículas Alfa
El núcleo de un átomo es su centro y está hecho de protones y neutrones. Estas partículas se mantienen unidas por una fuerza muy fuerte. Las partículas alfa son muy estables y pueden existir dentro de la estructura de un núcleo pesado.
Cuando una partícula alfa es liberada, tiene una energía de movimiento (energía cinética) que la hace viajar muy rápido, a unos 15.000 kilómetros por segundo.
El Efecto Túnel Cuántico
Imagina que una partícula alfa está atrapada dentro del núcleo, como en una caja. Para escapar, tendría que saltar por encima de una "pared" de energía. Pero la partícula alfa no tiene suficiente energía para saltar esa pared.
Aquí es donde entra en juego un concepto sorprendente de la mecánica cuántica llamado "efecto túnel". Es como si la partícula pudiera "atravesar" la pared en lugar de saltarla. Aunque la probabilidad de que esto ocurra en un solo intento es muy pequeña, la partícula choca contra la pared muchísimas veces por segundo. Con el tiempo, finalmente logra "tunelizar" y escapar del núcleo.
Este efecto fue explicado por científicos como George Gamow en 1928, y fue una gran confirmación de las ideas de la mecánica cuántica.
Usos de la Desintegración Alfa
Las partículas alfa, a pesar de su origen en la desintegración, tienen usos importantes en nuestra vida diaria y en la tecnología:
- Los detectores de humo usan un elemento llamado americio-241, que emite partículas alfa. Estas partículas ionizan el aire, creando una pequeña corriente eléctrica. Si entra humo en el detector, interrumpe esa corriente y activa la alarma.
- El radio-223, que también emite partículas alfa, se usa en medicina para tratar ciertos tipos de cáncer que se han extendido a los huesos.
- La desintegración alfa puede ser una fuente de energía segura para los generadores termoeléctricos de radioisótopos. Estos se usan para dar energía a las sondas espaciales y, en el pasado, a algunos marcapasos cardíacos. Es más fácil protegerse de la radiación alfa que de otros tipos de radiación.
- Los eliminadores de estática a menudo usan polonio-210, un emisor alfa, para ionizar el aire y ayudar a que la electricidad estática se disipe más rápido.
Seguridad y Partículas Alfa
Las partículas alfa son relativamente pesadas y tienen una carga positiva. Esto significa que no viajan muy lejos y pierden su energía rápidamente al chocar con otros átomos.
- La radiación alfa externa no es peligrosa para nosotros. Unos pocos centímetros de aire o la capa exterior de nuestra piel pueden detener las partículas alfa. Tocar una fuente de partículas alfa generalmente no causa daño.
- Sin embargo, si una fuente de partículas alfa entra en el cuerpo (por ejemplo, al inhalarlas o ingerirlas), puede ser muy peligroso. Dentro del cuerpo, las partículas alfa pueden depositar mucha energía en un área pequeña, lo que puede dañar las células.
- Una fuente natural de radiación alfa es el radón, un gas radiactivo que se encuentra en el suelo y en algunas rocas. Si inhalamos radón, sus productos de desintegración pueden quedar atrapados en los pulmones y emitir partículas alfa, lo que podría dañar las células pulmonares.
- Se cree que la científica Marie Curie pudo haber desarrollado una enfermedad grave debido a su exposición prolongada a altas dosis de radiación ionizante, ya que trabajó mucho con el radio, que se desintegra en radón y otros elementos radiactivos.
Historia de la Desintegración Alfa
Las partículas alfa fueron descubiertas por primera vez por Ernest Rutherford en 1899, mientras investigaba la radiactividad. En 1907, se confirmó que estas partículas eran núcleos de helio (iones He2+).
En 1928, George Gamow desarrolló la teoría que explicaba cómo las partículas alfa podían escapar del núcleo a través del "efecto túnel cuántico". Su teoría demostró que la desintegración alfa es una consecuencia natural de las leyes de la mecánica cuántica.
Galería de imágenes