Sulfato de cobre(II) para niños
Datos para niños
Sulfato de cobre(II) |
||
|---|---|---|
 Sulfato de cobre anhidro
|
||
 Cristales grandes de CuSO
4·5H2O |
||
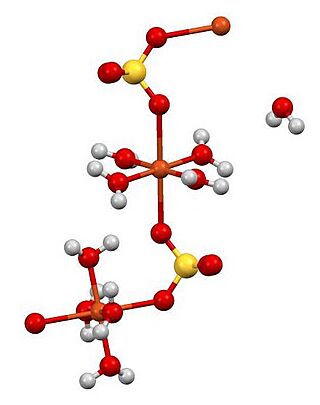 Estructura del sulfato de cobre (II) pentahidratado.
|
||
| Nombre IUPAC | ||
| Tetraoxidosulfato de cobre(2+) | ||
| General | ||
| Otros nombres | Vitriolo azul, arena azul, piedra azul, caparrosa azul , vitriolo romano, calcantita (este es la designación para el mineral natural del compuesto), piedra lipe, sulfato cúprico. | |
| Fórmula semidesarrollada | CuSO4 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 7758-98-7 | |
| Número RTECS | GL8800000 | |
| ChEBI | 23414 | |
| ChemSpider | 22870 | |
| DrugBank | DB06778 | |
| PubChem | 24462 | |
| UNII | KUW2Q3U1VV | |
| KEGG | C18713 | |
|
InChI
InChI=InChI=1S/Cu.H2O4S/c;1-5(2,3)4/h;(H2,1,2,3,4)/q+2;/p-2
Key: ARUVKPQLZAKDPS-UHFFFAOYSA-L |
||
| Propiedades físicas | ||
| Apariencia | Pentahidratado: Cristales azules Anhidro: Polvo blanco grisáceo |
|
| Densidad | 3603 kg/m³; 3,603 g/cm³ | |
| Masa molar | 158,881 g/mol | |
| Punto de fusión | 383 K (110 °C) | |
| Punto de ebullición | 923 K (650 °C) | |
| Estructura cristalina |
pentahidratado: triclínico anhidro: ortorrómbico |
|
| Propiedades químicas | ||
| Acidez | 0,005 pKa | |
| Solubilidad en agua | 20,7 g/100 ml (20 °C) | |
| Termoquímica | ||
| ΔfH0sólido | –769,98 kJ/mol | |
| S0sólido | 109,05 J·mol–1·K–1 | |
| Compuestos relacionados | ||
| Otros aniones | Citrato de cobre(II) Cloruro de cobre(II) Ioduro de cobre(II) Óxido de cobre(II) |
|
| Otros cationes | Sulfato de níquel(II) Sulfato de zinc Sulfato de bario Sulfato de sodio Sulfato de aluminio Sulfato de amonio |
|
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El sulfato de cobre(II), también llamado sulfato cúprico, es un compuesto inorgánico que se presenta como un sólido cristalino. Su fórmula química es CuSO4(H2O)x. La letra "x" indica que puede tener entre 0 y 5 moléculas de agua unidas.
La forma más común es el sulfato de cobre(II) pentahidratado (cuando x = 5), que tiene un color azul brillante y una estructura cristalina llamada triclínica. Cuando no tiene agua (x = 0), se le llama forma anhidra, es de color blanco o gris pálido y tiene una estructura rómbica. Este compuesto también se conoce con nombres antiguos como vitriolo azul, arena azul, piedra azul o calcantita (que es su nombre como mineral natural).
El sulfato de cobre pentahidratado pierde sus moléculas de agua al calentarse. Cuatro de ellas se van a 110 °C, y la quinta a 150 °C. Así se forma el sulfato de cobre anhidro, que se descompone si se calienta por encima de los 200 °C.
Cuando el sulfato de cobre se disuelve en agua, libera calor (es una reacción exotérmica). Forma un complejo acuoso que tiene una forma especial llamada geometría molecular octaédrica.
El sulfato de cobre se usa principalmente en la agricultura y la ganadería. También es un ingrediente para fabricar otros compuestos de cobre. Se utiliza en recubrimientos metálicos, para teñir telas y para proteger la madera. La forma sin agua se usa para detectar la humedad. Es muy útil como fungicida (para combatir hongos), plaguicida (para plagas) y bactericida (para bacterias). Además, es un material popular para experimentos educativos, como la creación de cristales.
Es importante saber que el sulfato de cobre es tóxico e irritante y puede ser peligroso para el medio ambiente.
Contenido
- Historia del sulfato de cobre
- Cómo se obtiene el sulfato de cobre
- Características del sulfato de cobre
- Usos del sulfato de cobre
- Usos en agricultura y ganadería
- Uso en medicina
- Uso en el tratamiento de aguas y acuarios
- Usos en minería y metalurgia
- Uso químico
- Usos en petróleo, carbón, caucho sintético, plásticos y adhesivos
- Usos en la construcción
- Usos en diseño, decoración, artes y pinturas
- Uso en electrónica
- Usos en textiles y cuero
- Uso en pirotecnia
- Uso didáctico
- Otros usos
- Seguridad al usar sulfato de cobre
- Identificación de peligros (SFGA, NFPA)
- Prevención de riesgos
- Primeros auxilios
- Medidas contra incendios
- Medidas en caso de derrames
- Manipulación y almacenamiento seguro
- Vías de exposición y límites
- Protección personal y controles
- Estabilidad y reactividad
- Información sobre toxicidad
- Información ecológica
- Eliminación del sulfato de cobre
- Transporte del sulfato de cobre
- Obtención
- Galería de imágenes
- Véase también
Historia del sulfato de cobre
Los sulfatos, como el sulfato de cobre, se formaron en la Tierra primitiva cuando ácidos como el sulfúrico disolvieron ciertas rocas en el agua subterránea. Así se crearon minerales naturales como la calcantita.
Desde hace mucho tiempo, incluso antes del siglo IV a.C., el sulfato de cobre ha sido utilizado por los seres humanos. En el Antiguo Egipto, se usaba como mordiente en el proceso de teñido de telas, una práctica que aún se mantiene hoy en día.
Los antiguos griegos, alrededor del 400 a.C., ya lo usaban en ungüentos y medicinas. Por ejemplo, Hipócrates lo recetaba para problemas pulmonares. En el siglo XVIII, se usaba en el mundo occidental para tratar algunas afecciones.
Aunque el sulfato de cobre no ha demostrado ser beneficioso para la salud y es tóxico, en algunas partes de África y Asia todavía se valora para curar heridas y problemas de la piel. En Occidente, se encuentra en pequeñas cantidades en algunos alimentos para bebés y en suplementos de vitaminas y minerales.
Desde 1838, este compuesto se ha usado para proteger la madera. A principios del siglo XX, se descubrió que ayudaba a controlar el crecimiento de algas, y desde entonces se aplica para reducir sus poblaciones.
Historia en la agricultura
El sulfato de cobre ha tenido un uso muy importante en la agricultura. En 1761, se descubrió que si se remojaban semillas en una solución suave de sulfato de cobre, se evitaba que crecieran hongos en ellas. En 1807, se vio que remojar semillas de cereales en esta solución y luego secarlas con cal ayudaba a controlar una enfermedad del trigo llamada "carbón volador". Esto se convirtió en una práctica común.
Gracias a los compuestos de cobre, enfermedades como el tizón se controlaron tan bien que ya no causan grandes pérdidas económicas.
El mayor avance para las sales de cobre en la agricultura ocurrió en la década de 1880. Un científico francés llamado Millardet notó que las vides que estaban cubiertas con una mezcla de sulfato de cobre y cal para proteger las uvas de los transeúntes, también estaban libres de mildiú velloso. Esta observación llevó a Millardet a crear el famoso caldo bordelés en 1885, una mezcla que se usó para fumigar cultivos y protegerlos de enfermedades.
Poco después, apareció la mezcla borgoñesa, similar al caldo bordelés, pero hecha con sulfato de cobre y carbonato de sodio.
Pronto se demostró que pequeñas cantidades de sulfato de cobre, aplicadas correctamente, podían prevenir muchas enfermedades de las plantas. Desde entonces, los fungicidas de sulfato de cobre son esenciales y se usan miles de toneladas cada año en todo el mundo.
Cómo se obtiene el sulfato de cobre
El sulfato de cobre se puede comprar fácilmente, por lo que no suele prepararse en laboratorios pequeños. A nivel industrial, se produce haciendo reaccionar ácido sulfúrico con compuestos de cobre(II), como el Óxido de cobre(II) o el carbonato de cobre.
La forma más común de producirlo es haciendo que el sulfato de cobre pentahidratado se separe de soluciones concentradas de cobre. Esto ocurre después de extraer el cobre de minerales oxidados. Las reacciones químicas son:
Precipitación: <chem>Cu2+(aq) + SO4^2- (aq) -> CuSO4(s)</chem>
Hidratación: <chem>CuSO4(s) + H2O -> CuSO4.5H2O(s)</chem>
Estas reacciones suceden en ese orden durante el proceso.
Método de obtención de Okers
Otro método para obtener sulfato de cobre es la reacción desarrollada por Okers:
<chem>2Cu + 2H2SO4 + O2 -> 2CuSO4 + 2H2O</chem>
Los mejores resultados con esta reacción se obtienen a 25°C, usando mucho aire y una concentración de ácido sulfúrico del 25%.
Características del sulfato de cobre
Sulfato de cobre comercial
El sulfato de cobre que se vende suele ser 98% puro y puede contener un poco de agua. El sulfato de cobre sin agua tiene 39.81% de cobre y 60.19% de sulfato. La forma azul, con agua, tiene 25.47% de cobre, 38.47% de sulfato (12.82% de azufre) y 36.06% de agua. Se vende en diferentes tamaños de cristales: grandes (10–40 mm), pequeños (2–10 mm), "nieve" (menos de 2 mm) y polvo (menos de 0.15 mm).
Propiedades químicas
El sulfato de cobre(II) pentahidratado se descompone antes de derretirse. Pierde agua en varias etapas al calentarse: dos moléculas a 63 °C, otras dos a 109 °C y la última a 200 °C. A 650 °C, se descompone en óxido de cobre(II) (CuO) y trióxido de azufre (SO3).
El sulfato de cobre reacciona con ácido clorhídrico concentrado para formar tetraclorocuprato(II):
<chem>Cu2+ + 4Cl- -> CuCl4^2-</chem>
Cristalografía
La mayoría de los compuestos de cobre (II) son de color azul o verde. Un ejemplo es el complejo azul oscuro que forma el cobre con el amoníaco. En la estructura del sulfato de cobre pentahidratado, cada ion Cu2+ está rodeado por átomos de oxígeno en una forma especial. Cuatro de ellos provienen de moléculas de agua, y dos de grupos sulfato. Una quinta molécula de agua conecta otros iones. Al calentar, el agua se pierde en tres fases:
<chem>CuSO4.5H2O -> CuSO4.3H2O -> CuSO4.H2O -> CuSO4</chem>
Solubilidad
El sulfato de cobre se disuelve en agua. La cantidad que se disuelve aumenta con la temperatura. Por ejemplo, a 20 °C, se disuelven 20.7 gramos en 100 ml de agua.
Usos del sulfato de cobre

El sulfato de cobre tiene muchos usos:
- Como alguicida en el tratamiento de aguas.
- En la fabricación de alimentos para animales y abonos.
- Como pesticida y para teñir telas.
- En la industria del cuero y para hacer pigmentos.
- En baterías eléctricas y recubrimientos metálicos.
- Como preservante de la madera.
- En procesos de grabado y litografía.
- En la industria del petróleo y el caucho sintético.
- En la industria del acero y el tratamiento del asfalto.
- Como colorante cerámico y en preparados medicinales.
Usos en agricultura y ganadería
Agricultura
En agricultura, se usa en abonos y fertilizantes. Por ejemplo, es un nutriente para el arroz y ayuda a producir más látex en los árboles de caucho. Como se disuelve bien en agua, se puede aplicar de muchas maneras, como riego o pulverización. También se usa para hacer pesticidas, fungicidas y bactericidas. Algunos hongos, como Botrytis cinerea, pueden resistir el cobre, pero el caldo bordelés, que contiene sulfato de cobre, sigue siendo efectivo.
También se usa como herbicida para controlar plantas acuáticas no deseadas y raíces cerca de tuberías de agua.
Como fungicida
Los fungicidas de cobre son muy buenos para proteger las plantas de los hongos. Lo ideal es aplicar una capa protectora de caldo bordelés o mezcla borgoñesa en las plantas antes de que aparezca la enfermedad. Así, las esporas de los hongos mueren al entrar en contacto con el cobre. Es importante aplicar el fungicida en el momento adecuado y de forma regular.
El sulfato de cobre también se usa para crear otros fungicidas, como el polvo de cobre-cal tribásico. Hay que tener cuidado de no usar mezclas demasiado concentradas, ya que pueden dañar las plantas.
El caldo bordelés
El caldo bordelés es una mezcla de sulfato de cobre(II) (CuSO4) e hidróxido de calcio (Ca(OH)2) en agua. Se usa para controlar hongos en uvas, melones y otras frutas. Se prepara mezclando una solución de sulfato de cobre con una suspensión de cal apagada.
La concentración se describe con tres números: peso de sulfato de cobre, peso de cal y volumen de agua. Por ejemplo, una mezcla al 1% es 1:1:100 (1 kg de sulfato de cobre, 1 kg de cal, 100 litros de agua). Para que se adhiera mejor, se puede añadir melaza.
El caldo borgoñés
La mezcla borgoñesa es similar al caldo bordelés y también sirve para controlar hongos en plantas. Se prepara disolviendo sulfato de cobre y carbonato de sodio por separado en agua y luego mezclándolos. El caldo borgoñés es menos propenso a obstruir los equipos y se adhiere mejor a las hojas.
Otras soluciones fungicidas
Existen otras mezclas fungicidas con sulfato de cobre, como el caldo de jabón (sulfato de cobre, jabón en polvo y agua) y una técnica propuesta por Mr. Audoynand (sulfato de cobre, amoníaco y agua de lluvia). Es importante usar agua no muy dura para evitar problemas con el jabón.
Efectividad de los fungicidas de sulfato de cobre
Los fungicidas de sulfato de cobre son muy efectivos contra al menos 300 enfermedades de plantas causadas por hongos y bacterias. La tabla original muestra una lista detallada de plantas y las enfermedades que pueden controlar.
Como insecticida
El sulfato de cobre se usaba para eliminar las bromelias, que son lugares donde se reproducen los mosquitos. Hoy en día, es un ingrediente para fabricar otros insecticidas, como el arsenito de cobre.
Esterilización de suelos: componente Cheshunt
El componente Cheshunt era una mezcla de sulfato de cobre y carbonato de amonio que se usaba en jardinería para prevenir el marchitamiento de las plantas jóvenes causado por hongos.
Ganadería
En la ganadería, el sulfato de cobre se usa para:
- Fabricar alimentos para animales que evitan la falta de cobre.
- Ayudar al crecimiento y engorde de cerdos y pollos.
- Prevenir la fragilidad ósea y la anemia en el ganado lechero.
- Combatir la podredumbre del pie en ovejas y vacas.
- Actuar como bactericida en baños para ovejas.
- Prevenir la erisipela en cerdos y la diarrea en terneros.
Para la falta de cobre en animales
Para corregir la falta de cobre en el ganado, se puede tratar el suelo donde pastan los animales o darles suplementos que contengan sulfato de cobre.
Estimulación del crecimiento de cerdos y pollos
Añadir hasta un 0.1% de sulfato de cobre a la dieta de cerdos y pollos puede aumentar su apetito y hacer que crezcan más rápido, mejorando cómo aprovechan su alimento.
Para la gotera esofágica
En animales rumiantes jóvenes, el sulfato de cobre puede ayudar a que la leche pase directamente al estómago correcto, evitando problemas de digestión. En ovejas, es muy efectivo para esto.
Control de deficiencias en suelos
El sulfato de cobre ayuda a corregir la falta de cobre en los suelos. Si un suelo tiene menos de dos partes de cobre por millón, se considera deficiente. El uso de ciertos fertilizantes puede reducir los niveles de cobre en el suelo, afectando a las plantas y a los animales que las comen.
Para corregir esto, se pueden añadir compuestos de cobre, como el sulfato de cobre, directamente al suelo o mezclados con fertilizantes. Esto puede tener un efecto duradero por más de diez años.
Uso en medicina
En medicina, el sulfato de cobre se ha usado como antídoto para el fósforo y para tratar la anemia. También se usa en preparados medicinales como el agua de alibour. Puede ser un micronutriente mineral y un catalizador en la producción de medicamentos.
Se utiliza para detectar la anemia: una gota de sangre se deja caer en una solución de sulfato de cobre. Si la sangre se hunde rápido, tiene suficiente hemoglobina; si no, podría haber anemia.
El sulfato de cobre ayuda a prevenir el hongo del pie de atleta en las piscinas si se mezcla con el hormigón de los baños públicos. También se usó para controlar las larvas de mosquitos que transmiten la malaria.
Aunque en la antigua Grecia se creía que el cobre tenía propiedades curativas, el sulfato de cobre no ha demostrado beneficios para la salud y es tóxico. Sin embargo, en algunas culturas de África y Asia se sigue usando para problemas de piel. En Occidente, se encuentra en pequeñas cantidades en algunos alimentos y suplementos.
Uso en el tratamiento de aguas y acuarios
Purificación de agua
El sulfato de cobre se usa en piscinas y estanques agrícolas para eliminar las algas, actuando como alguicida. También previene el pie de atleta en piscinas al mezclarse con el hormigón.
Además de ser alguicida, es bactericida. En cantidades adecuadas, no daña a los peces.
Acuariofilia
En acuarios, se usa como alguicida, antibacteriano y antifúngico. También es un medicamento para muchos peces de agua dulce o salada. Ayuda a eliminar caracoles y mejillones de las tuberías.
Es crucial no usar demasiado sulfato de cobre, ya que es muy tóxico para los ambientes acuáticos y sus seres vivos. Por ejemplo, puede estresar a los peces si se usa en exceso.
Actúa contra parásitos externos como los "ichs" (Cryptocaryon irritans) y Oodinium. También contra crustáceos parásitos como Argulus. Antes era efectivo contra el platelminto Dactylogyrus, pero este se ha vuelto resistente.
Cómo usar y eliminar el sulfato de cobre en acuarios
Aunque es seguro en las cantidades correctas, el sulfato de cobre no debe usarse en acuarios con tiburones, invertebrados o arrecifes. Es bueno tener un medidor de cobre. Las algas pueden absorber el cobre, y luego liberarlo al morir.
Para preparar una solución de tratamiento, se mezclan 21 gramos de sulfato de cobre con 21 gramos de ácido cítrico en 1 pinta de agua destilada. Se usa 1 gota por cada galón de agua del acuario (0.15 ppm). El ácido cítrico ayuda a que el cobre se disuelva y se mantenga estable.
Los niveles seguros están entre 0.15 ppm y 0.20 ppm. Concentraciones más altas pueden dañar a los peces. El carbón activado no elimina el cobre del agua; solo se puede eliminar cambiando el agua o usando un producto especial llamado E.D.T.A.
Usos en minería y metalurgia
Industria metalúrgica
El sulfato de cobre se usa en baños para recubrimientos metálicos (galvanizados), en la fabricación de circuitos impresos y para obtener cobre puro. También da un acabado azul-negro al acero.
Minería
Se utiliza en la minería para separar metales como el plomo, el zinc y el cobalto de los minerales. Es un activador en procesos metalúrgicos para sulfuros de zinc, hierro, cobalto y níquel.
Uso químico
El sulfato de cobre es un catalizador importante. Ayuda a purificar gases y a precipitar sustancias en soluciones. También se usa para obtener otros compuestos de cobre.
Como reactivo analítico
Se usa en pruebas químicas como las soluciones de Fehling y Benedict para detectar azúcares. También en el reactivo de Biuret para analizar proteínas. En la prueba de la llama, los iones de cobre producen una luz azul-verde intensa.
Para síntesis orgánica
La sal sin agua se usa para eliminar el agua en ciertas reacciones químicas. La sal con agua, mezclada con permanganato de potasio, se usa para transformar alcoholes.
En la producción de rayón
Al reaccionar con hidróxido de amonio, forma el reactivo de Schweizer, que se usaba para disolver la celulosa en la fabricación de rayón.
En la espectroscopía de absorción visible y ultravioleta
El sulfato de cobre se ha usado para estudiar cómo las sustancias absorben la luz, lo que ayuda a entender la Ley de Beer-Lambert. Esta ley explica cómo la intensidad de la luz disminuye al pasar por una solución.
Usos en petróleo, carbón, caucho sintético, plásticos y adhesivos
Petróleo
Se usa para crear catalizadores en el procesamiento de petróleo y para purificar aceites.
Caucho sintético
Se emplea para fabricar catalizadores usados en la producción de caucho.
Adhesivos
Es un conservante para pegamentos y un aditivo para hacerlos más resistentes al agua. También se usa en pegamentos para libros para protegerlos de insectos.
Carbón
El sulfato de cobre es un activador en la fabricación de carbón activado y mejora la combustión del coque (un tipo de combustible).
Usos en la construcción
Se añade al hormigón para hacerlo más resistente al agua, desinfectante y para darle color. El hormigón con sulfato de cobre se usa en piscinas por sus propiedades antisépticas. También puede retrasar el endurecimiento del hormigón.
Protege techos y otros materiales de construcción contra líquenes y mohos. Controla el crecimiento de raíces de árboles en alcantarillas. Además, es un conservante para la madera y se usa para preparar otros protectores de madera.
Combate la podredumbre de la madera causada por hongos si se añade al yeso.
Usos en diseño, decoración, artes y pinturas
Pinturas y pigmentos
Es un ingrediente para fabricar pinturas que evitan el crecimiento de organismos marinos y para hacer secadores de barnices. También se usa para preparar pigmentos como el cromato de cobre.
Colorantes artificiales y alimentarios
Se usa en la preparación de colorantes y como catalizador. Colorea vidrio, cemento, yeso y cerámica. También puede cambiar el color de metales como el zinc y el aluminio. En alimentos, se usa en la clorofila (E140i) como colorante.
Arte
El sulfato de cobre se puede usar como colorante en obras de arte, especialmente en vidrio y cerámica. El artista Roger Hiorns creó una obra llamada Seizure llenando un apartamento abandonado con una solución de sulfato de cobre, que luego cristalizó cubriendo las superficies.
Grabado
Se utiliza para grabar planchas de zinc o cobre en el grabado artístico y para hacer diseños en joyería de cobre.
Tintorería
Se usa como mordiente en la tintura de telas, especialmente para resaltar tonos verdes. También es un ingrediente en tintas para marcar ropa.
Teñido
Se emplea como ingrediente en tintes para el cabello.
Uso en electrónica
Una solución de sulfato de cobre se usa como parte de resistencias líquidas. También es un electrolito en el refinamiento y recubrimiento de cobre, en la fabricación de polvo de cobre y en el chapado de aluminio.
Se usa para recubrir alambres de acero con cobre antes de estirarlos y para limpiar alambres de cobre antes de esmaltarlos. También prepara superficies de hierro y acero para marcarlas.
Galvanoplastia
La galvanoplastia es un proceso para cubrir un material con una capa delgada de otro metal, como el cobre sobre el hierro. El sulfato de cobre se usa como electrolito. Los iones de cobre se adhieren al hierro, y los iones sulfato reaccionan con el cobre para crear más sulfato de cobre, manteniendo el equilibrio eléctrico.
Determinación de la resistividad de las rocas
En laboratorios, se usa una solución de sulfato de cobre para medir la resistividad eléctrica de las rocas, lo que ayuda a entender sus propiedades.
Usos en textiles y cuero
Textiles
El sulfato de cobre es un ingrediente para hacer telas resistentes a la putrefacción, como las de los sacos de arena. Se usa como mordiente en la impresión de telas y en la producción de rayón. También ayuda a fijar los colores en los tintes.
Industria del cuero
Se usa como mordiente para teñir el cuero y como reactivo en el proceso de curtido.
Uso en pirotecnia
El sulfato de cobre se utiliza en fuegos artificiales para crear un color azul-verde. Es importante controlar la temperatura para que el color sea intenso sin que el compuesto se descomponga.
Aunque se usaba mucho antes, no es la sal de cobre más segura para pirotecnia porque puede oxidarse y reaccionar con otros químicos. Es mejor usarlo con perclorato de potasio, pero las mezclas deben usarse de inmediato y no almacenarse. El carbonato de cobre es una opción más segura.
Uso didáctico
Debido a que es fácil de conseguir, el sulfato de cobre se usa a menudo en experimentos educativos, especialmente para mostrar cómo se forman los cristales.
Otros usos
Como repelente
El sulfato de cobre puede repeler animales y parásitos. Por ejemplo, se aplica en la corteza de los árboles para alejar a los conejos.
Como molusquicida (para caracoles y babosas)
Cantidades muy pequeñas de sulfato de cobre en el agua pueden controlar caracoles acuáticos que transmiten enfermedades. Se usa para eliminar babosas y caracoles que pueden albergar parásitos que causan enfermedades en países tropicales.
Imprenta
Es un aditivo en pastas y pegamentos para libros para proteger el papel de insectos. También es un ingrediente en tintas de impresión.
Conservante
Se usa para proteger postes y construcciones de madera, cajas de frutas, redes de pesca y cueros. También conserva pegamentos y pulpa de madera. Se usa en soluciones para conservar muestras de plantas y en papel para envolver frutas y evitar que se pudran.
Seguridad al usar sulfato de cobre
Es muy importante manejar el sulfato de cobre con cuidado, ya que puede ser perjudicial.
- Piel: Si entra en contacto prolongado con la piel, puede causar irritación, enrojecimiento, dolor o picazón. Si esto ocurre, lava la zona con mucha agua.
- Ojos: Puede irritar los ojos, causando enrojecimiento, visión borrosa e inflamación. Si entra en los ojos, lávalos con agua abundante durante al menos 15 minutos.
- Inhalación: Inhalar el polvo puede causar tos y dolor de garganta, y podría afectar los pulmones. Si alguien lo inhala accidentalmente, llévalo a un lugar con aire fresco y busca ayuda médica.
- Ingestión: Es perjudicial si se ingiere. Puede causar dolor de estómago, sensación de ardor, diarrea, náuseas y vómitos. Si esto sucede, enjuaga la boca con agua y bebe uno o dos vasos de agua, pero no intentes vomitar. Busca ayuda médica de inmediato.
La dosis más pequeña que ha causado efectos en humanos es de 11 mg por cada kilogramo de peso corporal. Si se ingiere, el cuerpo suele intentar vomitarlo. Pero si se queda en el estómago, los síntomas pueden ser serios. Después de ingerir entre 1 y 12 gramos, pueden aparecer síntomas como sabor metálico, dolor en el pecho, náuseas, vómitos, dolor de cabeza y problemas para orinar. En casos graves, puede afectar órganos importantes.
Siempre busca asistencia médica si hay contacto o ingestión. Mantén el sulfato de cobre fuera del alcance de los niños. Evita que el polvo se disperse. Es muy soluble en agua, por lo que puede extenderse fácilmente en el medio ambiente y es muy peligroso para los organismos acuáticos.
Identificación de peligros (SFGA, NFPA)
El sulfato de cobre se clasifica como:
- Nocivo si se ingiere.
- Causa irritación en la piel.
- Causa irritación grave en los ojos.
- Muy peligroso para el medio ambiente acuático, con efectos duraderos.
Se usan pictogramas de seguridad para indicar estos peligros. La palabra de advertencia es: Atención.
Consejos de seguridad (Frases P)
- P273: Evita que se libere al medio ambiente.
- P280: Usa guantes, ropa, gafas y máscara de protección.
- P301 + P330 + P331: SI SE INGIERE: Enjuaga la boca. NO provoques el vómito.
- P302 + P352: SI ENTRA EN CONTACTO CON LA PIEL: Lava con mucha agua.
- P305 + P351 + P338: SI ENTRA EN CONTACTO CON LOS OJOS: Enjuaga con agua cuidadosamente durante varios minutos. Si usas lentes de contacto, quítalas si es fácil. Sigue lavando.
- P312: Si te sientes mal, llama a un centro de información toxicológica o a un médico.
Prevención de riesgos
Evita que el polvo se disperse. Usa ventilación o protección respiratoria. Ponte guantes de protección y gafas o una máscara. No comas, bebas ni fumes mientras trabajas. Lávate las manos antes de comer.
Primeros auxilios
- Inhalación: Lleva a la persona al aire libre y que descanse. Si no respira, hazle respiración artificial. Si se siente mal, busca ayuda médica.
- Contacto con la piel: Lava la piel con mucha agua y jabón durante al menos 15 minutos. Quítate la ropa contaminada. Si la irritación persiste, consulta a un médico.
- Contacto con los ojos: Abre bien los párpados y enjuaga con agua limpia y fresca durante 10 a 15 minutos. Si usas lentes de contacto, quítalas. Si la irritación persiste, consulta a un oculista.
- Ingestión: NO provoques el vómito. Dale a beber uno o dos vasos de agua y enjuágale la boca si está consciente. Llama a un médico.
Medidas contra incendios
El sulfato de cobre no es inflamable, pero si hay un incendio cerca, puede liberar humos y gases irritantes. Usa el medio de extinción adecuado (agua pulverizada, espuma, polvo seco, dióxido de carbono). Evita que el agua usada para apagar el fuego llegue a los desagües. Se descompone a partir de 150 °C y a más de 400 °C emite óxidos de cobre y azufre.
Medidas en caso de derrames
- Para el personal: Usa equipo de protección personal, incluyendo un respirador. Evita el contacto con la piel, ojos y ropa. No inhales el polvo.
- Para el medio ambiente: Evita que el producto llegue a desagües, ríos o aguas subterráneas. Si hay un derrame grande, avisa a las autoridades.
- Limpieza: Recoge el sulfato de cobre derramado con una pala y ponlo en recipientes cerrados para su eliminación. Si es necesario, humedece el polvo para que no se disperse.
Manipulación y almacenamiento seguro
Guarda el sulfato de cobre en su envase original, en un lugar fresco, seco, ventilado y lejos de la luz solar directa, el calor y sustancias incompatibles (como ácidos y bases). Mantenlo fuera del alcance de niños y personal no autorizado.
Vías de exposición y límites
El sulfato de cobre puede entrar al cuerpo al inhalar el polvo o al ingerirlo. Una exposición corta puede irritar gravemente los ojos y la piel, y el polvo puede irritar las vías respiratorias. La ingestión puede afectar la sangre, los riñones y el hígado.
Una exposición prolongada o repetida al polvo puede afectar los pulmones y el hígado.
Límites de exposición en el trabajo
Existen límites de seguridad para la cantidad de sulfato de cobre en el aire en los lugares de trabajo, para proteger a las personas que lo manipulan.
Protección personal y controles
Asegúrate de que haya estaciones para lavar los ojos y duchas de seguridad cerca de donde se trabaja. Es importante tener buena ventilación.
- Protección de ojos/cara: Usa gafas de protección con protección lateral.
- Protección de la piel: Usa guantes adecuados (de nitrilo, caucho natural, neopreno o PVC) y ropa protectora.
- Protección respiratoria: Si hay polvo, usa un filtro de partículas (P2). En usos a gran escala, se necesita un respirador aprobado.
- Control ambiental: Evita que el producto llegue a desagües o aguas superficiales y subterráneas.
Estabilidad y reactividad
El sulfato de cobre es estable en condiciones normales. Es higroscópico, lo que significa que absorbe humedad del aire y tiende a apelmazarse. Pierde agua lentamente a partir de 30 °C.
- Reacciones peligrosas: Reacciona fuertemente con acetileno y lejía fuerte.
- Condiciones a evitar: Calor, temperaturas elevadas, humedad y ambientes alcalinos. Se descompone entre 150 y 560 °C.
- Materiales incompatibles: Puede reaccionar con magnesio para producir gas hidrógeno inflamable. No es compatible con agentes reductores, agua, polvos de metal y ciertos pesticidas.
- Productos de descomposición peligrosos: Al quemarse, puede liberar óxidos de azufre y óxidos de cobre.
Información sobre toxicidad
Parámetros toxicológicos
La dosis letal media (LD50) por vía oral en ratas es de 481 a 482 mg/kg para la forma anhidra y 960 mg/kg para la pentahidratada. Por contacto con la piel, es mayor a 2.000 mg/kg en ratas.
Efectos toxicológicos
- Causa irritación en la piel y los ojos.
- No se clasifica como causante de mutaciones, cáncer o problemas de reproducción.
- Las personas con problemas en ojos, piel o pulmones pueden ser más sensibles a este producto.
Síntomas por contacto o ingestión
- Ingestión: Puede causar diarrea, vómitos, náuseas, dolor de estómago y sensación de ardor. Si no se vomita de inmediato, puede haber efectos más graves en el cuerpo, como daño en órganos.
- Contacto con los ojos: Irritación, dolor, enrojecimiento y visión borrosa.
- Inhalación: Irritación de las vías respiratorias, tos, dolor de garganta y dificultad para respirar.
- Contacto con la piel: Irritación, enrojecimiento y dolor.
Riesgos especiales
Puede liberar gases perjudiciales a altas temperaturas. Es sensible a la luz.
Información ecológica
Es muy perjudicial para los organismos acuáticos y puede tener efectos negativos duraderos en el medio ambiente acuático.
Parámetros de toxicidad para seres vivos
Es tóxico para peces (LC50 de 0.1-2.5 mg/L para trucha arcoíris), pulgas de agua (EC50 de 0.24 mg/L) y algas. Es menos tóxico para aves y gusanos.
Efectos en el medio ambiente
- Degradación: No se degrada fácilmente en el ambiente.
- Persistencia: Puede permanecer en el ambiente.
- Bioacumulación: Podría acumularse en los seres vivos.
- Movilidad en el suelo: Se absorbe fuertemente en los suelos, pero puede moverse en el agua, especialmente en suelos ácidos.
- Movilidad en el aire: Las concentraciones en el aire son muy bajas.
Eliminación del sulfato de cobre
El sulfato de cobre y sus envases deben eliminarse como residuos peligrosos, siguiendo las normativas locales e internacionales. NO debe liberarse al medio ambiente ni tirarse por el desagüe. Los residuos deben clasificarse y llevarse a centros de tratamiento especializados.
Transporte del sulfato de cobre
Se clasifica como una "Materia sólida potencialmente peligrosa para el medio ambiente". Se transporta bajo regulaciones especiales para materiales peligrosos, con etiquetas que indican su riesgo para el medio ambiente acuático.
Obtención
Los principales países que producen sulfato de cobre son México, Brasil, Chile, Rusia, Taiwán, Italia, Perú y China. En España y Portugal, se encuentra en minas del suroeste de la península ibérica, como las Minas de Tharsis y Riotinto.
Galería de imágenes
Véase también
 En inglés: Copper(II) sulfate Facts for Kids
En inglés: Copper(II) sulfate Facts for Kids
- Sulfato de cobre(II) pentahidratado
- Sal Ácida
- Sulfato
- Cobre
- Química inorgánica
- Nomenclatura
- Aluminio