Sólido para niños
El sólido (del latín solĭdus) es uno de los estados de la materia. Se caracteriza porque mantiene su forma y su volumen, y opone resistencia a que los cambien. Sus partículas están muy juntas y ordenadas. Las moléculas de un sólido tienen una gran unión entre sí y forman figuras bien definidas.
Varias ramas de la ciencia estudian los sólidos:
- La física del estado sólido investiga los materiales condensados, como líquidos y sólidos con muchos átomos en contacto.
- La mecánica de sólidos deformables estudia cómo se comportan los materiales cuando se les aplica una fuerza, como la deformación.
- La ciencia de materiales se enfoca en las propiedades de los sólidos, su estructura y cómo cambian de fase.
- La química del estado sólido se dedica a crear nuevos materiales.
Cuando la presión es constante y la temperatura es baja, los cuerpos se presentan en forma sólida. Sus partículas se unen formando estructuras que suelen ser cristalinas. Esto permite que el sólido soporte fuerzas sin deformarse visiblemente.
El sólido más ligero que se conoce es el aerogel, un material artificial muy poroso, con una densidad de 3 miligramos por centímetro cúbico. El vidrio tiene una densidad de 1.9 gramos por centímetro cúbico. El sólido más denso es un metal llamado osmio (Os), con una densidad de 22.6 gramos por centímetro cúbico.
Contenido
¿Cómo son los sólidos por dentro?
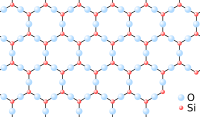
Los átomos, moléculas o iones que forman los sólidos pueden estar organizados en un patrón que se repite, o de forma irregular. Los materiales con un patrón regular se llaman cristales. A veces, este orden se extiende por todo el material, como en los diamantes, donde cada diamante es un solo cristal grande.
La mayoría de los objetos sólidos que podemos ver y tocar no están hechos de un solo cristal. En cambio, están formados por muchos cristales pequeños, llamados cristalitos. Estos pueden ser muy pequeños o bastante grandes. A estos materiales se les llama policristales. Casi todos los metales y muchas cerámicas son policristalinos.
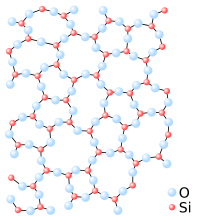
En otros materiales, los átomos no tienen un orden a largo plazo. Estos sólidos se llaman sólidos amorfos. Ejemplos de sólidos amorfos son el poliestireno y el vidrio.
Si un sólido es cristalino o amorfo depende del material y de cómo se formó. Los sólidos que se enfrían lentamente suelen ser cristalinos. Los que se enfrían rápido son más propensos a ser amorfos. La forma específica de cristal que adopta un sólido también depende del material y de su formación.
Muchos objetos comunes, como un cubito de hielo, son iguales en toda su composición. Pero otros materiales están hechos de varias sustancias diferentes. Por ejemplo, una roca es una mezcla de varios minerales. La madera es un material natural hecho de fibras de celulosa y lignina. En la ciencia de los materiales, se pueden crear materiales compuestos con más de un componente para obtener propiedades específicas.
Propiedades de los sólidos
Los sólidos tienen características especiales que los distinguen:
- Elasticidad: Un sólido puede volver a su forma original después de ser estirado o doblado. Un resorte es un buen ejemplo de esta propiedad.
- Fragilidad: Algunos sólidos se rompen fácilmente en muchos pedazos. Son quebradizos.
- Dureza: Es la resistencia de un material a ser rayado, penetrado o deformado. El diamante es un sólido muy duro.
- Forma definida: Los sólidos tienen una forma propia y son rígidos. No fluyen como los líquidos o los gases, a menos que estén bajo presiones extremas.
- Alta densidad: Los sólidos suelen ser densos porque sus moléculas están muy juntas, lo que los hace más "pesados" para su tamaño.
- Flotación: Algunos sólidos flotan si su densidad es menor que la del líquido en el que se colocan.
- Inercia: Es la resistencia de un sólido a cambiar su estado de reposo o movimiento.
- Tenacidad: Es la capacidad de un material para resistir que se formen o extiendan grietas en él.
- Maleabilidad: Es la propiedad de algunos materiales de poder ser convertidos en láminas delgadas sin romperse.
- Ductilidad: Es la propiedad de los sólidos de poder estirarse para formar hilos.
- Rigidez: Algunos sólidos resisten más que otros a ser doblados o torcidos.
- Deformación: Algunos sólidos pueden cambiar de forma sin romperse.
- Aleabilidad: Es la capacidad de algunos materiales para mezclarse y formar aleaciones, que son nuevos materiales con mejores características.
- Calor específico: Es la cantidad de energía necesaria para aumentar la temperatura de una sustancia en un grado Celsius.
Tipos de sólidos
Las fuerzas que unen los átomos en un sólido pueden ser de varios tipos. Por ejemplo, en la sal común (cloruro de sodio), los iones de sodio y cloro se unen por enlaces iónicos. En el diamante, los átomos comparten electrones y forman enlaces covalentes. En los metales, los electrones se comparten en un enlace metálico. Algunos sólidos, como muchos compuestos orgánicos, se mantienen unidos por fuerza de van der Waals, que es una fuerza débil entre moléculas. Las diferencias en estos enlaces dan lugar a los distintos tipos de sólidos.
Metales
Los metales son generalmente fuertes, densos y buenos conductores de la electricidad y el calor. La mayoría de los elementos de la tabla periódica son metales.
Las mezclas de dos o más elementos donde el principal es un metal se llaman aleaciones. Desde hace mucho tiempo, los humanos han usado metales para muchas cosas. Su fuerza y durabilidad los hacen útiles en la construcción de edificios, vehículos, herramientas, tuberías y vías de tren. El hierro y el aluminio son los metales estructurales más usados y los más abundantes en la corteza terrestre. El hierro se usa mucho en forma de acero, una aleación con carbono que lo hace más duro.
Como los metales conducen bien la electricidad, son importantes en aparatos eléctricos y para llevar corriente eléctrica a largas distancias. Por eso, las redes eléctricas usan cables de metal. En casa, el cobre se usa para el cableado por su buena conducción. La alta conductividad térmica de los metales también los hace útiles para utensilios de cocina.
El estudio de los metales y sus aleaciones es clave en la química, la física y la ciencia de materiales.
Los sólidos metálicos se mantienen unidos por una gran cantidad de electrones compartidos y libres, lo que se conoce como "enlace metálico". En un metal, los átomos pierden fácilmente sus electrones externos, formando iones positivos. Estos electrones libres se mueven por todo el sólido, que se mantiene unido por la atracción entre los iones y la nube de electrones. La gran cantidad de electrones libres hace que los metales sean buenos conductores de electricidad y calor. También impiden el paso de la luz, haciendo que los metales sean opacos, brillantes y lustrosos.
Minerales
Los minerales son sólidos naturales que se forman por procesos geológicos bajo mucha presión. Para ser un mineral verdadero, una sustancia debe tener una estructura cristalina y propiedades físicas uniformes. Los minerales pueden ser desde elementos puros hasta silicatos muy complejos.
Una roca es una mezcla de diferentes minerales y no tiene una composición química específica. La mayoría de las rocas en la corteza terrestre están hechas de cuarzo, feldespato, mica y otros minerales. Algunos minerales son comunes, mientras que otros son muy raros. El grupo más grande de minerales son los silicatos, que están hechos principalmente de silicio y oxígeno, con otros metales.
Cerámica
Los sólidos cerámicos están hechos de compuestos inorgánicos, generalmente óxidos de elementos químicos. Son resistentes a los químicos y pueden soportar altas temperaturas, entre 1000 y 1600 °C. Algunas excepciones son los nitruros, boruros y carburos.
Las materias primas tradicionales para la cerámica incluyen minerales de arcilla, como la caolinita. Materiales más modernos son el óxido de aluminio (alúmina), el carburo de silicio y el carburo de tungsteno. Estos últimos son muy valorados por su resistencia a la abrasión y se usan en equipos de trituración en minería.
La mayoría de los materiales cerámicos, como la alúmina, se forman a partir de polvos finos. Esto crea una estructura policristalina con muchos puntos que dispersan la luz, por lo que suelen ser opacos. Sin embargo, la tecnología actual permite producir cerámicas transparentes para usos como láseres de alta potencia. La cerámica avanzada también se usa en medicina y en la industria electrónica.
La Cerámica técnica es la ciencia de crear materiales y dispositivos cerámicos. Esto se logra aplicando calor o mediante reacciones químicas a bajas temperaturas. Incluye la purificación de materias primas, la producción de compuestos, la formación de componentes y el estudio de sus propiedades.
Mecánicamente, los materiales cerámicos son frágiles, duros y fuertes a la compresión, pero débiles a la cizalla y la tensión. La Dureza indica cuánta energía puede absorber un material antes de romperse. La tenacidad a la fractura describe la capacidad de un material para resistir el crecimiento de grietas. La fractura frágil es común en la mayoría de las cerámicas.
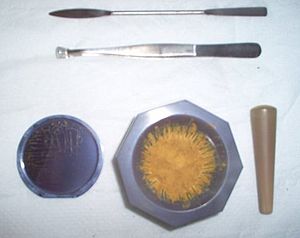
Un ejemplo de aplicación de la cerámica es el zirconia, que se usa para fabricar cuchillos y otras herramientas de corte por su extrema dureza. Cerámicas como la alúmina y el carburo de silicio se usan en chalecos antibala para detener disparos. Las piezas de nitruro de silicio se usan en rodamientos de bolas cerámicos, donde su dureza los hace resistentes al desgaste. Las cerámicas también son resistentes a los químicos y se pueden usar en ambientes húmedos donde los rodamientos de acero se oxidarían.
Otro ejemplo es la investigación de Toyota en los años 80 para crear un motor cerámico que pudiera funcionar a más de 3300 °C sin sistema de refrigeración. Esto reduciría el peso y aumentaría la eficiencia del combustible. En un motor de metal, gran parte de la energía se pierde como calor para evitar que las piezas se derritan. También se están desarrollando piezas cerámicas para turbinas. Sin embargo, fabricar piezas cerámicas con la precisión y durabilidad necesarias es difícil y costoso.
Vitrocerámica
Los materiales vitrocerámicos tienen propiedades tanto de los vidrios no cristalinos como de los materiales cristalinos y cerámicos. Se forman como vidrio y luego se cristalizan parcialmente con calor. Esto crea fases amorfas y cristalinas, donde los granos cristalinos están dentro de una fase no cristalina.
La vitrocerámica se usa para utensilios de cocina y placas de cocina. Son muy resistentes al choque térmico (cambios bruscos de temperatura) y casi no dejan pasar líquidos. Su coeficiente de expansión térmica puede ser cercano a cero, lo que les permite soportar cambios rápidos de temperatura de hasta 1000 °C.
La vitrocerámica también puede formarse naturalmente cuando un rayo cae sobre granos de cuarzo en la arena de las playas. El calor extremo del rayo (unos 2500 °C) crea estructuras huecas y ramificadas llamadas fulguritas al fundir la arena.
Sólidos orgánicos
La química orgánica estudia los compuestos químicos de carbono e hidrógeno, que también pueden contener nitrógeno, oxígeno y halógenos (como flúor, cloro, bromo y yodo), o fósforo y azufre. Ejemplos de sólidos orgánicos son la madera, la cera de parafina, el naftaleno y muchos polímeros y plásticos.
Madera
La madera es un material orgánico natural hecho principalmente de fibras de celulosa incrustadas en una matriz de lignina. Las fibras son fuertes a la tensión, y la lignina resiste la compresión. Por eso, la madera ha sido un material de construcción importante desde que los humanos empezaron a construir refugios. La madera usada en construcción se conoce como madera o madera. Además de ser un material estructural, la madera también se usa para moldes de hormigón.
Los materiales derivados de la madera se usan mucho para envases (como el cartón) y papel, que se hacen de pulpa refinada.
Polímeros
Una propiedad importante del carbono es que puede formar compuestos cuyas moléculas individuales se unen entre sí, creando cadenas o redes. Este proceso se llama polimerización, y las cadenas o redes son polímeros. El compuesto original se llama monómero. Hay dos grupos principales de polímeros: los artificiales (polímeros industriales o sintéticos, como los plásticos) y los naturales (biopolímeros).
Los monómeros pueden tener diferentes grupos químicos que afectan las propiedades de los compuestos orgánicos, como su capacidad para disolverse, su reactividad química, su dureza, densidad, resistencia, transparencia o color. En las proteínas, estas diferencias permiten que el polímero adopte una forma biológicamente activa.
Los humanos han usado polímeros orgánicos naturales, como ceras y goma laca, durante siglos. La celulosa, un polímero vegetal, da resistencia a las fibras y cuerdas naturales. A principios del siglo XIX, el caucho natural era muy usado. Los polímeros son las materias primas (resinas) que se usan para fabricar lo que llamamos plásticos. Los plásticos son el producto final, creado al añadir uno o más polímeros o aditivos a una resina y darle una forma final.
Algunos polímeros comunes son el polietileno, el polipropileno, el cloruro de polivinilo, el poliestireno, los nilones, el poliéster, los acrílicos, el poliuretano, el policarbonato y la silicona. Los plásticos se clasifican en "básicos", "especiales" y "de ingeniería".
Material compuesto

Los materiales compuestos contienen dos o más partes diferentes, una de las cuales suele ser cerámica. Por ejemplo, una base continua y partículas o fibras cerámicas dispersas en ella.
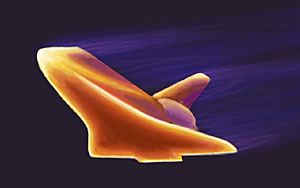
Los materiales compuestos se usan en muchas aplicaciones, desde elementos estructurales como el hormigón reforzado con acero, hasta las baldosas térmicas que protegen la superficie del Transbordador espacial de la NASA del calor de la reentrada en la atmósfera terrestre. Un ejemplo es el Carbono Reforzado (RCC), un material gris claro que soporta temperaturas de hasta 1510 °C y protege la punta y los bordes de las alas del transbordador. El RCC es un material compuesto hecho de grafito y resina, que se convierte en carbono y luego se recubre con carburo de silicio para resistir la oxidación.
En casa, podemos ver materiales compuestos en las carcasas de plástico de televisores o teléfonos móviles. Estas carcasas suelen ser un compuesto de un plástico como el acrilonitrilo butadieno estireno (ABS) al que se le añade carbonato de calcio, talco, fibras de vidrio o fibras de carbono para darle resistencia o volumen.
El material base rodea y soporta los materiales de refuerzo, manteniendo sus posiciones. Los refuerzos aportan sus propiedades especiales para mejorar las de la base. Esta combinación crea materiales con propiedades que no se encuentran en los materiales individuales, y la gran variedad de materiales permite diseñar la combinación perfecta.
Semiconductores
Los semiconductores son materiales que tienen una resistencia eléctrica (y conductividad) intermedia entre la de los metales (conductores) y la de los aislantes (no metales). Se encuentran en la tabla periódica en una línea diagonal que va desde el boro hacia abajo a la derecha.
Los dispositivos hechos con materiales semiconductores son la base de la electrónica moderna, incluyendo la radio, los ordenadores, los teléfonos, etc. Ejemplos de dispositivos semiconductores son el transistor, las células solares, los diodos y los circuitos integrados. Los paneles solares fotovoltaicos son grandes dispositivos semiconductores que transforman la luz directamente en energía eléctrica.
En un conductor metálico, la corriente es el "flujo de electrones". Pero en los semiconductores, la corriente puede ser transportada por los electrones o por "agujeros de electrones" con carga positiva. Los materiales semiconductores más comunes son el silicio, el germanio y el arseniuro de galio.
Nanomateriales
Muchos sólidos tradicionales muestran propiedades diferentes cuando se reducen a tamaños muy pequeños, llamados nanométricos. Por ejemplo, las nanopartículas de oro, que normalmente son amarillas, y las de silicio, que son grises, se vuelven rojas. Las nanopartículas de oro se derriten a temperaturas mucho más bajas (unos 300 °C para un tamaño de 2.5 nanómetros) que las piezas grandes de oro (1064 °C). Los nanocables metálicos son mucho más fuertes que los metales grandes.
La gran superficie de las nanopartículas las hace muy útiles en el campo de la energía. Por ejemplo, los metales de platino pueden mejorar los catalizadores de combustible para coches. También se están desarrollando óxidos cerámicos para pilas de combustible de óxido sólido (SOFC). Las nanopartículas de litio, litio-titanato y tantalio se usan en baterías de iones de litio. Se ha demostrado que las nanopartículas de silicio aumentan mucho la capacidad de almacenamiento de estas baterías. Los nanocables de silicio se mueven sin degradarse y podrían usarse en baterías con tiempos de almacenamiento muy largos. Las nanopartículas de silicio también se usan en nuevas células de energía solar. Al colocar puntos cuánticos de silicio en una célula solar, el voltaje aumenta hasta un 60% porque la luz entrante fluoresce antes de ser capturada. Aquí, la superficie de las nanopartículas es clave para absorber la mayor cantidad de radiación.
Biomateriales
Muchos materiales naturales (o biológicos) son compuestos complejos con propiedades mecánicas notables. Estas estructuras complejas, que han evolucionado durante millones de años, inspiran a los científicos a diseñar nuevos materiales. Sus características principales son su estructura organizada en niveles, su capacidad de realizar múltiples funciones y de autocurarse. La autoorganización es también una característica fundamental de muchos materiales biológicos y de cómo se forman las estructuras desde el nivel molecular. Así, el autoensamblaje está surgiendo como una nueva estrategia en la creación de biomateriales de alto rendimiento.
Véase también
 En inglés: Solid Facts for Kids
En inglés: Solid Facts for Kids
- Estado de agregación de la materia
- Cambio de estado
- Propiedades intensivas y extensivas
- Licuefacción de gases
- Materia granular
- Gel
- Solidificación