Naftalina para niños
Datos para niños
Naftalina |
||
|---|---|---|
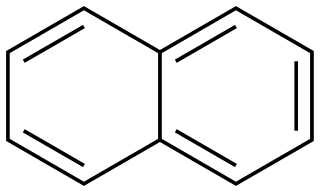 Estructura química
|
||
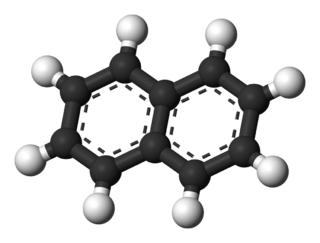 Estructura tridimensional
|
||
| Nombre IUPAC | ||
| biciclo [4.4.0]deca-1,3,5,7,9- | ||
| General | ||
| Fórmula molecular | C10H8 | |
| Identificadores | ||
| Número CAS | 91-20-3 | |
| Número RTECS | QJ0525000 | |
| ChEBI | 16482 | |
| ChEMBL | CHEMBL16293 | |
| ChemSpider | 906 | |
| PubChem | 931 | |
| UNII | 2166IN72UN | |
| KEGG | C00829 | |
|
c1ccc2ccccc2c1
|
||
|
InChI
InChI=1S/C10H8/c1-2-6-10-8-4-3-7-9(10)5-1/h1-8H
Key: UFWIBTONFRDIAS-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Apariencia | Sólido. Cristales blancos/hojuelas | |
| Olor | Fuerte olor a alquitrán | |
| Densidad | 1140 kg/m³; 1,14 g/cm³ | |
| Masa molar | 128,17052 g/mol | |
| Punto de fusión | 353 K (80 °C) | |
| Punto de ebullición | 491 K (218 °C) | |
| Presión de vapor | 8,64 Pa (20 °C) 23,6 Pa (30 °C) 0,93 kPa (80 °C) 2,5 kPa (100 °C) |
|
| Estructura cristalina | Monoclínica | |
| Viscosidad | 0,964 cP (80 °C) 0,761 cP (100 °C) 0,217 cP (150 °C) |
|
| Índice de refracción (nD) | 1,5898 | |
| Conductividad térmica | 98 kPa: 0,122 W/mK (372,22 K) 0,117 W/mK (400,22 K) 0,115 W/mK (418,37 K) 0,105 W/mK (479,72 K) |
|
| Constante de Henry (kH) | 0,42438 L·atm/mol | |
| Propiedades químicas | ||
| Solubilidad en agua | 19 mg/L (10 °C) 31,6 mg/L (25 °C) 43,9 mg/L (34,5 °C) 80,9 mg/L (50 °C) 238,1 mg/L (73,4 °C) |
|
| log P | 3,34 | |
| Termoquímica | ||
| ΔfH0sólido | 78,53 kJ/mol | |
| S0sólido | 167,39 J·mol–1·K–1 | |
| Capacidad calorífica (C) | 165,72 J/mol·K | |
| Peligrosidad | ||
| SGA |     |
|
| Punto de inflamabilidad | 356 K (83 °C) | |
| NFPA 704 |
2
2
0
|
|
| Temperatura de autoignición | 798 K (525 °C) | |
| Frases R | R22, R40, R50/53 | |
| Frases S | S2, S36/37, S46, S60, S61 | |
| Límites de explosividad | 5,9% | |
| Riesgos | ||
| Riesgos principales | Inflamable, sensibilizante, puede causar problemas de salud a largo plazo. En polvo puede formar mezclas explosivas con el aire | |
| LD50 | 2000 mg/kg (ratas, oral) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
La naftalina (cuyo nombre científico es naftaleno) es una sustancia química que tiene la fórmula C10H8. Es un sólido de color blanco que se convierte en gas fácilmente, un proceso llamado sublimación. Se forma de manera natural cuando se queman ciertos materiales, como el alquitrán de hulla o la madera. También se le conoce como alquitrán blanco.
La naftalina tiene un olor muy fuerte que a algunas personas les puede parecer desagradable. Se ha usado en bolas y escamas para mantener alejadas a las polillas de la ropa y otros objetos.
Existen compuestos parecidos a la naftalina, como la 1-metilnaftalina y la 2-metilnaftalina. La 1-metilnaftalina es un líquido transparente, mientras que la 2-metilnaftalina es un sólido. Ambos tienen un olor que se puede detectar incluso en cantidades muy pequeñas en el aire o en el agua.
Contenido
¿Cómo se descubrió la naftalina?
A principios de la década de 1820, dos científicos, trabajando por separado, encontraron un sólido blanco con un olor fuerte. Este sólido aparecía al destilar el alquitrán de hulla. En 1821, un químico llamado John Kidd estudió estas observaciones. Describió muchas de las características de esta sustancia y cómo se podía producir. Kidd le dio el nombre de naphthaline (naftalina). Este nombre viene de la palabra "nafta", que se usaba para referirse a mezclas líquidas de hidrocarburos que son volátiles e inflamables, como el alquitrán de hulla.
La fórmula química de la naftalina fue descubierta por Michael Faraday en 1826. Más tarde, en 1866, Emil Erlenmeyer propuso que la naftalina tenía una estructura de dos anillos de benceno unidos. Esta idea fue confirmada tres años después por Carl Gräbe.
¿De dónde se obtiene la naftalina?
La mayor parte de la naftalina que se produce hoy en día se obtiene del alquitrán de hulla. El alquitrán de hulla es un subproducto que se obtiene al calentar carbón en ausencia de aire.
Desde los años 60 hasta los 90, también se producía mucha naftalina a partir de partes más pesadas del petróleo durante su refinado. Sin embargo, en la actualidad, la naftalina que viene del petróleo es solo una pequeña parte de la producción total.
El alquitrán de hulla puede contener hasta un 10% de naftalina. En las fábricas, el alquitrán de hulla se destila para obtener un aceite que tiene aproximadamente un 50% de naftalina. Este aceite se limpia para quitarle otras sustancias y luego se destila de nuevo para separar la naftalina. La naftalina que se obtiene de este proceso suele tener una pureza de alrededor del 95%.
La naftalina que se obtiene del petróleo suele ser más pura que la del alquitrán de hulla. Si se necesita una naftalina aún más pura, se puede limpiar más usando un proceso llamado recristalización. Así se consigue una naftalina con un 99% de pureza. Cada año se produce aproximadamente un millón de toneladas de naftalina en el mundo.
¿Cómo es la estructura de la naftalina?
Una molécula de naftalina está formada por la unión de dos anillos de benceno. En química, cuando se dice que los anillos están "fusionados", significa que comparten dos o más átomos. Por eso, la naftalina se clasifica como un hidrocarburo aromático policíclico (HAP).
A diferencia del benceno, los enlaces entre los átomos de carbono en la naftalina no son todos iguales. Algunos enlaces son un poco más cortos (alrededor de 1,36 Å) y otros son un poco más largos (aproximadamente 1,42 Å). Esta diferencia se ha comprobado con técnicas especiales como la difracción de rayos X.
La naftalina puede reaccionar con otras sustancias de forma similar al benceno, pero a veces lo hace en condiciones más suaves. Por ejemplo, la naftalina puede reaccionar con cloro incluso sin un catalizador, mientras que el benceno sí lo necesita.
Una característica interesante de la naftalina es que puede pasar directamente de estado sólido a estado gaseoso sin convertirse en líquido. Este proceso se llama sublimación.
¿Para qué se utiliza la naftalina?
El uso principal de la naftalina (C10H8) es en la fabricación de plásticos, especialmente el cloruro de polivinilo (PVC).
Además, la naftalina se usa como un material base para crear otros compuestos químicos. Estos compuestos se utilizan luego para fabricar:
- Diferentes tipos de colorantes.
- Resinas sintéticas.
- Negro de humo (un pigmento).
- Materiales para ciertos usos especiales.
Como ya mencionamos, la naftalina en forma de bolas es muy conocida por su uso como repelente de polillas. También, la 2-metilnaftalina, un compuesto similar, se utiliza para producir vitamina K.
Existe la idea de que la naftalina puede mejorar el octanaje de la gasolina. Esto es parcialmente cierto, ya que sus componentes son muy volátiles y pueden ayudar a mejorar el octanaje. Sin embargo, en la industria, no es práctico usar naftalina para esto porque es un hidrocarburo aromático policíclico y se considera un contaminante que puede ser peligroso. Por eso, se prefieren otros aditivos para mejorar el octanaje de la gasolina.
Véase también
 En inglés: Naphthalene Facts for Kids
En inglés: Naphthalene Facts for Kids


