Tricloruro de fósforo para niños
Datos para niños
Tricloruro de fósforo |
||
|---|---|---|
 |
||
 |
||
| Nombre IUPAC | ||
| tricloruro de fósforo | ||
| General | ||
| Otros nombres | Cloruro de fósforo (III) Cloruro fosforoso |
|
| Fórmula estructural | 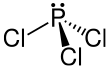 |
|
| Fórmula molecular | PCl3 | |
| Identificadores | ||
| Número CAS | 7719-12-2 | |
| Número RTECS | TH3675000 | |
| ChEBI | 30334 | |
| ChemSpider | 22798 | |
| PubChem | 24387 | |
| UNII | M97C0A6S8U | |
|
ClP(Cl)Cl
|
||
|
InChI
InChI=1S/Cl3P/c1-4(2)3
Key: FAIAAWCVCHQXDN-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Apariencia | líquido incoloro | |
| Densidad | 1574 kg/m³; 1,574 g/cm³ | |
| Masa molar | 137,33 g/mol | |
| Punto de fusión | 179,6 K (−94 °C) | |
| Punto de ebullición | 349,3 K (76 °C) | |
| Índice de refracción (nD) | 1,516 (14 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | Hidrólisis | |
| Momento dipolar | 0,97 D | |
| Termoquímica | ||
| ΔfH0líquido | −319,7 kJ/mol | |
| Peligrosidad | ||
| NFPA 704 |
0
4
2
W
|
|
| Frases R | R14, R26/28, R35, R48/20 | |
| Frases S | S1/2, S7/8, S26, S36/37/39, S45 | |
| Riesgos | ||
| LD50 | 550 mg/kg | |
| Más información | ICSC 0696 | |
| Compuestos relacionados | ||
| Cloruros de fósforo | Pentacloruro de fósforo Oxicloruro de fósforo Tetracloruro de difosfóro |
|
| Otros compuestos | Trifluoruro de fósforo Tribromuro de fósforo Triyoduro de fósforo |
|
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
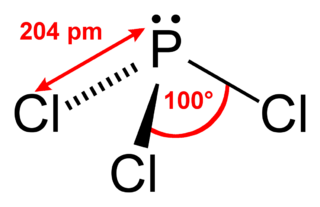
El tricloruro de fósforo es un compuesto químico formado por fósforo y cloro. Su fórmula química es PCl3. Este compuesto tiene una forma especial, como una pirámide con tres lados, llamada piramidal trigonal.
Es uno de los cloruros de fósforo más importantes. Se utiliza mucho en la industria para fabricar otros compuestos que contienen fósforo. Estos compuestos tienen una gran variedad de usos en nuestra vida diaria.
En el PCl3, el fósforo se encuentra en un estado particular (+3) y los átomos de cloro en otro estado (−1). Esto ayuda a entender cómo reacciona este compuesto.
Contenido
¿Cómo reacciona el tricloruro de fósforo?
El tricloruro de fósforo puede cambiar y formar otros compuestos de fósforo. Esto ocurre cuando se "oxida", es decir, cuando gana oxígeno o pierde electrones.
Por ejemplo, puede convertirse en pentacloruro de fósforo (PCl5) o oxicloruro de fósforo (POCl3). Si se le aplica una descarga eléctrica junto con gas hidrógeno, puede formar un cloruro de fósforo menos común, el tetracloruro de difósforo (P2Cl4).
Reacciones con otras sustancias
El PCl3 es muy útil para crear compuestos organofosforados. Estos son compuestos que combinan carbono y fósforo.
- Con agua: El tricloruro de fósforo reacciona muy rápido y libera calor al mezclarse con agua. Forma ácido fosforoso (H3PO3) y cloruro de hidrógeno (HCl).
:PCl3 + 3 H2O → H3PO3 + 3 HCl
- Con alcoholes: También reacciona con alcoholes o fenoles para formar ésteres de fosfito. Por ejemplo, con el fenol, se produce el fosfito de trifenilo.
:3 PhOH + PCl3 → P(OPh)3 + 3 HCl Si no hay una base (como una amina), la reacción con alcoholes puede producir ácido fosfónico y un cloruro de alquilo. :PCl3 + 3 C2H5OH → 3 C2H5Cl + H3PO3
- Con aminas y tioles: Las aminas (R2NH) forman compuestos como P(NR2)3, y los tioles (RSH) forman P(SR)3. Una reacción importante con aminas y formaldehído se usa para crear aminofosfonatos. Estos se usan para evitar la acumulación de sarro en el tratamiento de agua. El herbicida glifosato también se fabrica así.
- Con reactivos especiales: El PCl3 se usa con reactivos de Grignard y organolitio para hacer fosfinas orgánicas, como la trifenilfosfina.
:3 PhMgBr + PCl3 → Ph3P + 3 MgBrCl
¿Cómo se fabrica el tricloruro de fósforo?
Cada año se producen más de 330.000 toneladas de tricloruro de fósforo en el mundo. Se fabrica en la industria haciendo reaccionar cloro con fósforo blanco disuelto en tricloruro de fósforo. El PCl3 que se forma se va retirando continuamente.
- P4 + 6 Cl2 → 4 PCl3
La fabricación de tricloruro de fósforo está bajo un control internacional estricto. En los laboratorios, a veces se usa fósforo rojo en lugar de fósforo blanco, porque es menos peligroso.
¿Para qué se usa el tricloruro de fósforo?
El PCl3 es muy importante porque es el punto de partida para fabricar muchos otros compuestos.
- Derivados importantes: Se usa para producir pentacloruro de fósforo (PCl5), oxicloruro de fósforo (POCl3) y cloruro de tiofosforilo (PSCl3). Estos, a su vez, se usan en la fabricación de productos para la agricultura (como herbicidas e insecticidas), plastificantes, aditivos para el petróleo y sustancias que ayudan a evitar incendios (retardantes de llamas).
- Productos específicos: Por ejemplo, el oxicloruro de fósforo (POCl3) se usa para hacer fosfato de trifenilo y fosfato de tricresilo. Estos se emplean como retardantes de llamas y plastificantes para el cloruro de polivinilo (PVC). También se usan para crear insecticidas como el diazinon.
- En química orgánica: El PCl3 es clave para la reacción de Wittig, que es un método importante para crear alquenos. También se usa para convertir alcoholes en cloruros de alquilo y ácidos carboxílicos en cloruros de acilo.
Precauciones importantes
El tricloruro de fósforo es una sustancia muy peligrosa. Incluso una pequeña cantidad en el aire puede ser muy dañina en pocos minutos. Por eso, se clasifica como muy peligroso y corrosivo. Es fundamental manejarlo con mucho cuidado y seguir todas las normas de seguridad.
Véase también
 En inglés: Phosphorus trichloride Facts for Kids
En inglés: Phosphorus trichloride Facts for Kids


