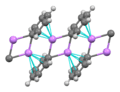Organolitio para niños
Un reactivo de organolitio es un tipo especial de compuesto organometálico. Esto significa que tiene un enlace directo entre un átomo de carbono y un átomo de litio. Como el litio es un elemento muy "generoso" con sus electrones, el carbono en este enlace se vuelve muy "negativo" o "rico en electrones", actuando como un carbanión. Por eso, los compuestos de organolitio son muy potentes y útiles en química. Son como imanes muy fuertes que atraen a otras partes de las moléculas.
Contenido
- ¿Cómo se preparan los reactivos de organolitio?
- ¿Cómo son los reactivos de organolitio?
- ¿Para qué se usan los reactivos de organolitio?
- Galería de imágenes
- Véase también
¿Cómo se preparan los reactivos de organolitio?
Muchos de los reactivos de organolitio más comunes se pueden comprar ya hechos. Pero también se pueden preparar en un laboratorio usando diferentes métodos. Aquí te explicamos algunos de ellos.
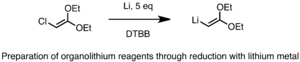
Reacción con litio metálico
Una forma de fabricar estos reactivos a gran escala es haciendo reaccionar un halocarbono (un compuesto de carbono con un halógeno como cloro o bromo) con litio en su forma metálica.
|
1 |
|
({{{3}}}) |
Esta reacción libera mucho calor. A veces se añade un poco de sodio para que la reacción sea más rápida. También se puede usar litio en polvo muy fino con algunos catalizadores (sustancias que aceleran la reacción sin consumirse).
También se pueden usar otros compuestos de organolitio ya existentes para crear nuevos. Esto se hace mediante una reacción de intercambio, donde el litio se cambia por un halógeno en otra molécula.
Metalación: Intercambio de litio e hidrógeno
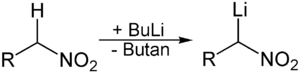
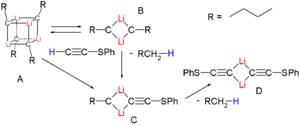
Otro método para preparar reactivos de organolitio es el proceso de metalación. Aquí, un compuesto de organolitio (como el n-butil-litio) "arranca" un átomo de hidrógeno de otra molécula. Al hacerlo, se forma el nuevo compuesto de organolitio que queremos y se libera un alcano (como el butano).
Esta reacción funciona mejor cuando el hidrógeno que se va a quitar es "más ácido" que otros hidrógenos en la molécula.
Por ejemplo, es muy común usar este método para hacer reactivos de alquinil-litio, porque los hidrógenos al final de los alquinos son muy fáciles de quitar.
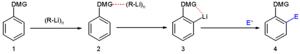
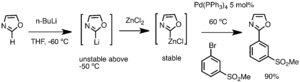
En compuestos con anillos (como los aromáticos), la posición donde se une el litio puede ser dirigida por otros grupos que ya estén en la molécula. Estos grupos tienen electrones libres que ayudan a que el litio se acerque a un hidrógeno específico, facilitando su extracción.
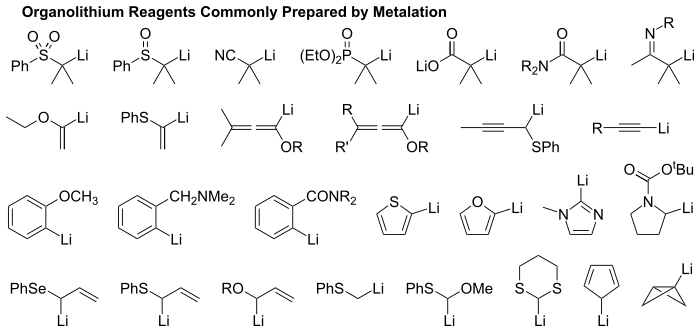
En la siguiente imagen puedes ver algunos ejemplos de compuestos de organolitio que se pueden obtener por metalación:
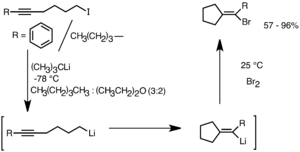
Intercambio de halógeno por litio
Un tercer método es el intercambio de halógeno por litio. En esta reacción, un átomo de halógeno en una molécula se intercambia por un átomo de litio de otro compuesto de organolitio.
|
2 |
|
({{{3}}}) |
Esta reacción es muy útil para crear nuevos reactivos de organolitio. Es muy rápida y a menudo se realiza a temperaturas muy bajas (entre -60 y -120 °C).
Transmetalación: Intercambio con otros metales
Los reactivos de organolitio también se pueden preparar a partir de otros compuestos que ya tienen un metal, como los compuestos de organocobre o organoestaño.
|
Error al representar (MathML con SVG o PNG como alternativa (recomendado para navegadores modernos y herramientas de accesibilidad): respuesta no válida («Math extension can not find Restbase URL. Please specify $wgMathFullRestbaseURL.») del servidor «invalid»:): {\displaystyle \ce{R-M} + \textit{n-}\ce{BuLi -> {R-Li} +}\ \textit{n-}\ce{BuM}} |
|
(3) |
Una ventaja de este método es que los productos secundarios no suelen reaccionar con los nuevos compuestos de organolitio, lo que facilita el proceso.
¿Cómo son los reactivos de organolitio?
Aunque a veces se representan como una sola molécula (RLi), en realidad los reactivos de organolitio suelen agruparse formando "racimos" o "polímeros". La forma de estos grupos depende de la parte orgánica de la molécula y de otras sustancias presentes. El litio tiende a unirse a varios átomos de carbono, y cada carbono a varios átomos de litio.
El enlace carbono-litio
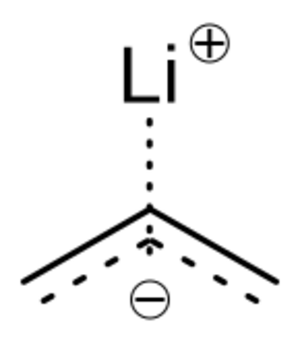
El enlace entre el carbono y el litio es muy especial. Como el litio es menos "electronegativo" que el carbono (es decir, atrae menos los electrones), el carbono "jala" la mayoría de los electrones del enlace. Esto hace que el enlace sea muy polar, casi como si el carbono tuviera una carga negativa y el litio una positiva. Esto es lo que los hace tan reactivos.
En algunos tipos de organolitios, como los alil-litios, el litio se une a una parte más grande de la molécula de carbono, no solo a un punto específico.
Estructura en estado sólido
Los compuestos de organolitio se agrupan debido a las fuerzas eléctricas entre sus partes con carga opuesta. También influye cómo se unen a las moléculas de los disolventes o a otros aditivos.
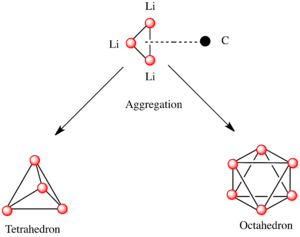
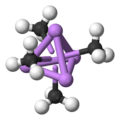
Una forma común de estos grupos es un átomo de carbono con carga negativa que interactúa con un triángulo de tres átomos de litio. En los organolitios más simples, estos triángulos se unen para formar estructuras más grandes, como tetraedros (pirámides de cuatro caras) u octaedros (figuras de ocho caras).
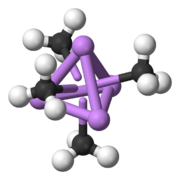
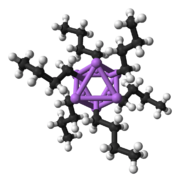
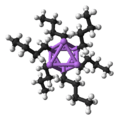
Por ejemplo, el metillitio forma grupos de cuatro moléculas (tetrámeros) que parecen un cubo. Otros, como el n-butil-litio, forman grupos de seis moléculas (hexámeros).
Si se añaden sustancias como el dietiléter o el THF, los grupos de organolitio pueden separarse en unidades más pequeñas, lo que los hace más solubles y reactivos.
Estructura en disolución
Es importante saber cómo se comportan los reactivos de organolitio cuando están disueltos, ya que es así como se usan en las reacciones. A veces, su estructura en disolución es diferente a la que tienen en estado sólido.
Por ejemplo, el metil-litio es un tetrámero en THF, mientras que el n-butil-litio puede ser un hexámero en benceno o un tetrámero en THF.
La espectroscopia RMN es una herramienta muy útil para estudiar cómo se agrupan los organolitios en disolución.
Los reactivos de organolitio también pueden reaccionar con los disolventes que se usan, especialmente los éteres. La siguiente tabla muestra cuánto tiempo duran algunos compuestos de organolitio en diferentes disolventes y temperaturas:
| Disolvente/ Temperatura |
n-butillitio ( n-BuLi ) |
s-butillitio ( s-BuLi ) |
t-butillitio ( t-BuLi ) |
metillitio (MeLi ) |
CH2=C(OEt)-Li | CH2=C(SiMe3)-Li |
|---|---|---|---|---|---|---|
| THF/-20 °C | 40 min, 360 min | |||||
| THF/20 °C | >15 h | 17 h | ||||
| THF/35 °C | 10 min | |||||
| THF/TMEDA/-20 °C | 3300 min | |||||
| THF/TMEDA/ 0 °C | 340 min | |||||
| THF/TMEDA/20 °C | 40 min | |||||
| Éter/-20 °C | 480 min | |||||
| Éter/0 °C | 61 min | |||||
| Éter/20 °C | 153 h | <30 min | 17 days | |||
| Éter/35 °C | 31 h | |||||
| Éter/TMEDA/ 20 °C | 603 min | |||||
| DME/-70 °C | 120 min | 11 min | ||||
| DME/-20 °C | 110 min | 2 min | <<2 min | |||
| DME/0 °C | 6 min |
¿Para qué se usan los reactivos de organolitio?
Los reactivos de organolitio son muy útiles en química porque son extremadamente reactivos. El carbono en el enlace carbono-litio actúa como un "imán" negativo, lo que los convierte en excelentes "nucleófilos" (buscan partes positivas de otras moléculas) y "bases" (quitan hidrógenos).
Son tan reactivos que no pueden estar en contacto con agua, oxígeno o dióxido de carbono. Por eso, deben manejarse en un ambiente especial, como bajo una atmósfera de nitrógeno o argón.
Se usan para:
- Construir nuevas moléculas.
- Quitar hidrógenos de otras moléculas (desprotonación).
- Iniciar reacciones de polimerización (crear cadenas largas de moléculas).
- Preparar otros compuestos con metales.
Uso como nucleófilo: Construyendo moléculas
Como nucleófilos, los reactivos de organolitio pueden unirse a enlaces dobles o triples de carbono, formando nuevas moléculas.
Reacciones de carbolitiación
Esta es una de las reacciones más importantes de los organolitios. Se usan para iniciar la polimerización aniónica, que es un proceso para crear plásticos y otros materiales. Por ejemplo, el n-butil-litio se usa para iniciar la polimerización del estireno o el butadieno.
También se pueden usar para formar anillos dentro de las moléculas (ciclación intramolecular). Esto es útil para crear estructuras complejas.
Adición a compuestos con grupo carbonilo
Los organolitios se usan mucho para añadir partes de moléculas a compuestos que tienen un grupo carbonilo (un átomo de carbono unido a un oxígeno con un doble enlace, como en las cetonas o aldehídos). Esto ayuda a formar alcoholes y otras moléculas.
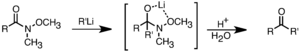
Los organolitios son mejores que otros reactivos similares (como los reactivos de Grignard) para reaccionar con ácidos carboxílicos y formar cetonas. También son muy buenos para reaccionar con las amidas de Weinreb para obtener cetonas.
También reaccionan con el dióxido de carbono para formar ácidos carboxílicos.
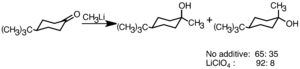
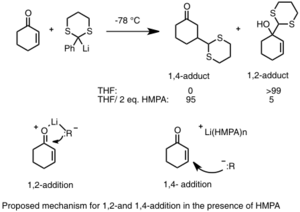
En algunas reacciones, los organolitios pueden unirse a diferentes lugares de una molécula. Los químicos pueden controlar dónde se unen usando aditivos especiales.
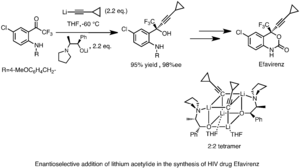
Los organolitios también se usan para crear moléculas con una forma específica (enantioselectiva), lo cual es muy importante en la fabricación de medicamentos. Un ejemplo es la síntesis de Efavirenz, un medicamento importante.
Otras reacciones generales de los compuestos de organolitio incluyen:
- Reacción con sales de ácido carboxílico para dar cetonas.
- Reacción con ésteres para dar alcoholes terciarios.
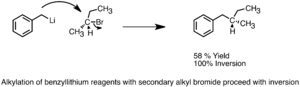
Reacciones tipo SN2
Los organolitios pueden actuar como nucleófilos en reacciones SN2, donde reemplazan un halógeno en una molécula. Aunque son muy reactivos, a veces pueden tener reacciones secundarias.
Reacciones en compuestos de aril-litio
Los compuestos de aril-litio (con anillos aromáticos) son muy útiles para añadir diferentes grupos a estos anillos. Se pueden usar para añadir grupos alquilo, bromo, yodo o para formar ácidos carboxílicos.
Como base: Quitadores de hidrógeno
Los compuestos de organolitio simples (como n-BuLi, sec-BuLi, t-BuLi) son bases muy fuertes. Esto significa que pueden quitar átomos de hidrógeno de casi cualquier compuesto, excepto los alcanos.
Cuantos más grupos alquilo tenga el organolitio, más fuerte será como base. Por ejemplo, el terc-butil-litio es una de las bases más fuertes que se pueden comprar.
Algunas bases de litio muy usadas son las dialquilamidas de litio (LiNR2), como la diisopropilamida de litio (LDA). Estas son muy buenas para formar "enolatos", que son importantes en muchas reacciones.
Desprotonación de iones de organofosfonio
Los reactivos de Wittig, que se usan para crear nuevos enlaces carbono-carbono, se forman quitando un hidrógeno de sales de fosfonio con una base fuerte como el butil-litio. ![\mathrm{[Ph_3P^+ CH_2R]X^- + C_4H_9Li \longrightarrow Ph_3P=CHR + LiX + C_4H_{10}}](/images/math/2/2/f/22f3236dda9623c6ecd03e08ca2d7e88.png)
Metalación
La metalación, o intercambio de litio-hidrógeno, ocurre cuando un organolitio quita un protón (hidrógeno) de otra molécula, formando un nuevo organolitio.
|
4 |
|
({{{3}}}) |
Los butillitios son los reactivos más comunes para esto. La posición donde se quita el hidrógeno depende de qué tan "ácido" sea ese hidrógeno.
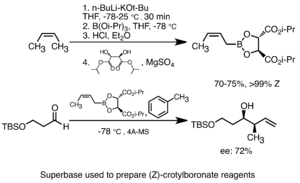
Superbases
Si se añade un alcóxido de potasio al alquil-litio, su fuerza como base aumenta mucho. Estas "superbases" son muy reactivas y selectivas.
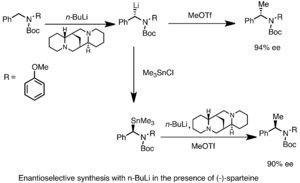
Metalación asimétrica
Se pueden obtener organolitios con una forma específica (enantioméricamente enriquecidos) usando la metalación asimétrica. Esto requiere la presencia de una molécula "quiral" (que no se puede superponer con su imagen en el espejo), como la (-)-esparteína.
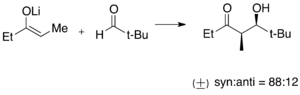
Formación de enolatos
Los enolatos de litio se forman quitando un hidrógeno de un carbono cercano a un grupo carbonilo. Son muy usados para crear nuevos enlaces carbono-carbono, como en la condensación aldólica.
Generalmente, se usan bases fuertes que no actúan como nucleófilos, como las amidas de litio (LDA, LiHMDS).
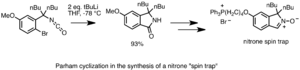
Intercambio halógeno-litio
El intercambio de halógenos por litio es clave en la ciclización de Parham. En esta reacción, un halógeno en un anillo aromático se cambia por litio, y luego el carbono con litio ataca a otra parte de la molécula para formar un nuevo anillo. Esto es muy útil para crear heterociclos (anillos con átomos diferentes de carbono).
Transmetalación: Creando otros compuestos organometálicos
Una de las utilidades más importantes de los organolitios es que sirven como punto de partida para crear otros compuestos organometálicos. Esto se hace reaccionando los organolitios con haluros de otros metales, como el cloruro de zinc para obtener compuestos de organocinc.
También se usan para formar reactivos de organocobre (como el reactivo de Gilman) o incluso reactivos de Grignard. Además, se pueden preparar compuestos de Organoestaño, organosilicio, organoboro, organofósforo y organoazufre a partir de organolitios.
Otras reacciones
- Reacción con oximas para dar aminas.
- Reacción con isonitrilos para dar aldiminas de litio, que luego se pueden convertir en aldehídos.
- Reacción con ciertos epóxidos para dar alquenos.
Galería de imágenes
Véase también
 En inglés: Organolithium reagent Facts for Kids
En inglés: Organolithium reagent Facts for Kids