Fosfato para niños
Datos para niños
Fosfato |
||
|---|---|---|
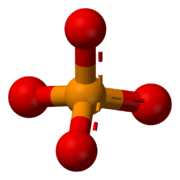
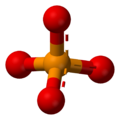
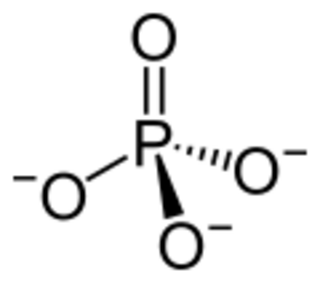 Anión fosfato
|
||
| General | ||
| Otros nombres | Ortofosfato; Tetraoxofosfato(V); anión fosfato | |
| Fórmula molecular | PO3− 4 |
|
| Identificadores | ||
| Número CAS | 14265-44-2 | |
| ChEBI | 26020 | |
| ChemSpider | 1032 | |
| PubChem | 1061 | |
| Propiedades físicas | ||
| Masa molar | 94,9714 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
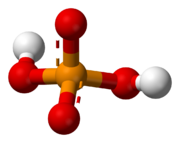
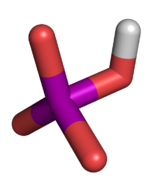
En el mundo de la química, un fosfato es una sustancia que proviene del ácido fosfórico. Puede ser un anión (una partícula con carga eléctrica negativa), una sal, un grupo funcional (una parte de una molécula) o un éster (un tipo de compuesto orgánico). Todos los fosfatos tienen algo en común: un átomo de fósforo rodeado por cuatro átomos de oxígeno, formando una figura llamada tetraedro.
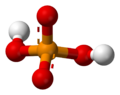
También se les llama ortofosfatos porque vienen de la forma más común del ácido fosfórico, el ácido ortofosfórico (H3PO4). La palabra "fosfato" también incluye a las sales que se forman cuando el ácido fosfórico se neutraliza solo en parte. Estas son el fosfato monoácido (HPO42-) y el fosfato diácido (H2PO4-).
Los ortofosfatos son muy importantes en la bioquímica (la química de los seres vivos), la biogeoquímica (cómo los elementos químicos se mueven en la Tierra) y la ecología (el estudio de los ecosistemas). También son clave para la agricultura y la industria. En las células, añadir o quitar grupos fosfato (procesos llamados fosforilación y desfosforilación) son pasos esenciales para el funcionamiento del metabolismo. Los fosfatos pueden unirse para formar cadenas llamadas polifosfatos, que son como una reserva de energía para las células. Cuando se liberan, proporcionan la energía necesaria para muchas reacciones químicas dentro de los seres vivos.
|
Contenido
¿Cómo son los fosfatos químicamente?
El ion fosfato tiene una masa de 94,97 gramos por cada mol (una unidad de cantidad de sustancia). Está formado por un átomo central de fósforo y cuatro átomos de oxígeno a su alrededor, con forma de tetraedro.
El ácido ortofosfórico es un ácido que puede perder tres protones (partículas con carga positiva). Por eso, cuando se mezcla con una base, puede neutralizarse de tres maneras diferentes, dando lugar a tres tipos de fosfatos:
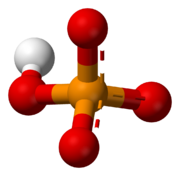
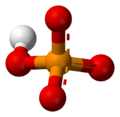
- Fosfatos diácidos o dihidrógeno fosfatos (H2PO4-): Cuando se disuelven en agua, estas sales hacen que la solución sea un poco ácida.
- Fosfatos monoácidos o hidrógeno fosfatos (HPO42-): Cuando se disuelven en agua, estas sales hacen que la solución sea básica.
- Fosfatos neutros o simplemente ortofosfatos (PO43-): También hacen que la solución sea básica al disolverse en agua.
¿Son solubles los fosfatos?
La mayoría de los fosfatos que contienen metales alcalinos (como el sodio o el potasio) y los de amonio se disuelven bien en agua a temperatura ambiente. Sin embargo, los fosfatos de otros metales, como los alcalinotérreos, suelen ser poco solubles o casi insolubles. Los fosfatos que tienen hidrógenos (como los fosfatos de hidrógeno y dihidrógeno) suelen ser un poco más solubles que los que no los tienen.
Los fosfatos pueden unirse para formar iones más grandes, como el pirofosfato (P2O7)4− y el trifosfato (P3O10)5−. También existen los iones metafosfato, que son cadenas largas y se encuentran en muchos compuestos.
¿Dónde encontramos fosfatos en la naturaleza?
Los ortofosfatos (PO43-) son muy comunes en la naturaleza. Se encuentran principalmente en minerales como la apatita y en depósitos de fosforita. La fosforita es una roca sedimentaria que contiene muchos minerales de fosfato, incluyendo restos de animales o de excrementos de aves (conocido como guano).
Los fosfatos y otros compuestos relacionados con el fósforo son parte esencial de los seres vivos. Forman estructuras como los huesos y los dientes, y participan en muchísimas reacciones químicas dentro de las células, sirviendo como una reserva de energía. Por eso, los fosfatos son indispensables para la vida.
¿Por qué son importantes los fosfatos en la agricultura?
Debido a su importancia para los seres vivos, los fosfatos son un ingrediente clave en los abonos minerales. Si no hay suficiente fosfato en el suelo, las plantas no pueden crecer bien.
El fosfato que se encuentra en la naturaleza, como el fosfato tricálcico, no se disuelve fácilmente en agua, lo que dificulta que las plantas lo absorban. Por eso, para hacer fertilizantes, los fosfatos naturales se transforman en formas más solubles. Por ejemplo, se usa ácido sulfúrico para convertir el fosfato tricálcico en superfosfato de cal:
- <chem>Ca3(PO4)2 + 2H2SO4 -> Ca(H2PO4)2 + 2CaSO4</chem>
En los métodos modernos, a veces se usa ácido fosfórico en lugar de ácido sulfúrico para obtener un fertilizante más concentrado llamado superfosfato triple:
- <chem>Ca3(PO4)2 + 4H3PO4 -> 3Ca(H2PO4)2 </chem>
Fosfatos en el agua
Los fosfatos también están presentes en las aguas residuales. Se pueden eliminar en parte usando métodos químicos que los hacen precipitar, o se retienen en los fangos activos de las plantas de tratamiento. Estos fangos luego pueden usarse para hacer abonos orgánicos.
El papel de los fosfatos en los seres vivos
En los sistemas biológicos, el fosfato se encuentra como un ion libre en solución, al que llamamos fosfato inorgánico (Pi). Esto lo diferencia del fosfato que está unido a otras moléculas. A un pH normal en el cuerpo, el fosfato inorgánico es una mezcla de iones HPO42− y H2PO4−.
El fosfato inorgánico se puede obtener cuando el pirofosfato (PPi) se descompone con agua:
- <chem>P2O7^4- + H2O <=> 2HPO4^2-</chem>
Sin embargo, los fosfatos son más conocidos por formar parte de moléculas como el AMP, el ADP y el ATP. Estas moléculas son como la "moneda de energía" de las células. Cuando el ATP o el ADP se descomponen, liberan fosfato y mucha energía, que las células usan para realizar sus funciones vitales. Por eso, se les llama fosfatos de alta energía.
Además de su función energética, añadir o quitar grupos fosfato a las proteínas es una forma muy importante en que las células regulan su metabolismo. El fosfato también es un componente clave de los nucleótidos, que son las unidades básicas que forman el ADN y otros ácidos nucleicos. También se encuentra en algunos lípidos que forman las membranas de las células.
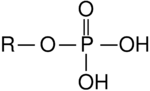
¿Qué son los fosfatos orgánicos?
Los fosfatos orgánicos son un tipo de ésteres del ácido fosfórico. Son moléculas más complejas que otros fosfatos. Se pueden fabricar haciendo reaccionar un compuesto llamado O=PCl3 con ciertos alcoholes. Algunos de estos ésteres pueden ser perjudiciales para el sistema nervioso, y están relacionados con algunos insecticidas. Sin embargo, otros se usan para hacer que los plásticos como el PVC sean más blandos.
¿Para qué se usan los trifosfatos?
Los trifosfatos (2-O3P-O-PO2--O-PO32-) se usan en los detergentes para "ablandar" el agua. Lo hacen atrapando el calcio y evitando que forme depósitos. Con el tiempo, los trifosfatos se transforman en ortofosfatos, que pueden contribuir a la eutrofización de las aguas superficiales (un exceso de nutrientes que causa un crecimiento descontrolado de algas). Por esta razón, se busca reemplazar los trifosfatos en los detergentes por otras sustancias que no tengan este efecto negativo.
Producción mundial de fosfato
A continuación, se muestra la producción mundial de fosfato en 2019, en miles de toneladas por año:
| 1. | 95,0 | |
| 2. | 35,5 | |
| 3. | 23,0 | |
| 4. | 13,1 | |
| 5. | 9,2 | |
| 6. | 6,5 | |
| 7. | 5,0 | |
| 8. | 4,7 | |
| 9. | 4,6 | |
| 10. | 4,1 |
Galería de imágenes
Véase también
 En inglés: Phosphate Facts for Kids
En inglés: Phosphate Facts for Kids