Electrolito para niños
Un electrolito es una sustancia especial que contiene partículas cargadas llamadas iones libres. Gracias a estos iones, los electrolitos pueden conducir la electricidad. La mayoría de las veces, los electrolitos se encuentran en disolución (como cuando disuelves sal en agua), por eso también se les llama disoluciones iónicas. Pero también pueden existir como líquidos fundidos o incluso como sólidos.
Imagina que aplicas electricidad a una disolución de electrolitos. Los iones positivos (llamados cationes) se moverán hacia el lado con más electrones, y los iones negativos (llamados aniones) irán hacia el lado con menos electrones. Este movimiento de iones en direcciones opuestas es lo que crea una corriente eléctrica.
Algunos gases, como el cloruro de hidrógeno, también pueden funcionar como electrolitos si están muy calientes o bajo poca presión. Además, ciertas moléculas grandes, como el ADN o algunas proteínas, pueden formar electrolitos cuando se disuelven, y se les llama "polielectrolitos".
En nuestro cuerpo, los electrolitos son muy importantes. El sodio, el potasio, el cloruro, el calcio, el magnesio y el fosfato son ejemplos de electrolitos que tenemos en nuestros fluidos.
En la medicina, es necesario reponer los electrolitos cuando una persona ha vomitado o tenido diarrea por mucho tiempo, o cuando suda mucho por hacer ejercicio intenso. Por eso existen bebidas especiales con electrolitos para niños enfermos o para atletas.
En la ciencia, los electrolitos son clave en las pilas y baterías.
Contenido
¿De dónde viene la palabra "electrolito"?
La palabra electrolito viene de dos palabras del Griego antiguo: ēlectro-, que se refiere a la electricidad, y lytos, que significa "capaz de soltarse o desatarse". Esto describe muy bien cómo los iones se "sueltan" en una disolución.
Un poco de historia
En 1884, un científico llamado Svante Arrhenius explicó que las sales sólidas, cuando se disuelven en agua, se separan en partículas cargadas. A estas partículas, Michael Faraday ya las había llamado "iones" años antes. Faraday pensaba que los iones solo se formaban durante la electrólisis (cuando se usa electricidad para separar sustancias). Pero Arrhenius propuso que los iones ya estaban presentes en las disoluciones de sales, incluso sin electricidad. Por su trabajo, Arrhenius ganó el Premio Nobel de Química en 1903.
¿Cómo funcionan los electrolitos?
Los electrolitos suelen ser ácidos, bases o sales disueltos en agua. Cuando una sal, como la sal común (cloruro de sodio o NaCl), se pone en agua, sus partes se separan. Esto sucede porque las moléculas de agua interactúan con la sal y la "disuelven" en iones.
Por ejemplo, cuando el cloruro de sodio se disuelve en agua, ocurre esto: NaCl (sólido) → Na+ (ión sodio) + Cl- (ión cloruro)
También hay sustancias que reaccionan con el agua para producir iones. Por ejemplo, el dióxido de carbono reacciona con el agua y forma iones.
En resumen, un electrolito es un material que, al disolverse en agua (o al fundirse), produce una disolución que puede conducir la electricidad.
Si una sustancia se disocia mucho en iones libres, se dice que es un electrolito fuerte. Si la mayoría de la sustancia no se separa en iones, es un electrolito débil.
¿Por qué son importantes los electrolitos en nuestro cuerpo?
En nuestro cuerpo, los electrolitos principales son el sodio (Na+), potasio (K+), calcio (Ca2+), magnesio (Mg2+), cloruro (Cl−), hidrógeno fosfato (HPO42−) y bicarbonato (HCO3−).
Todos los seres vivos necesitan un equilibrio muy preciso de electrolitos dentro y fuera de sus células. Este equilibrio es vital para:
- Mantener el cuerpo bien hidratado.
- Regular el pH de la sangre.
- Permitir que los nervios y los músculos funcionen correctamente.
- Ayudar en la respiración.
Nuestro cuerpo tiene varios sistemas para controlar los niveles de electrolitos. Por ejemplo, los riñones y ciertas hormonas ayudan a mantener este equilibrio.
Los músculos y las neuronas son como los "tejidos eléctricos" del cuerpo. Se activan gracias al movimiento de electrolitos a través de las membranas de las células. Si no tenemos suficientes electrolitos clave, como calcio, sodio y potasio, podemos sentir debilidad muscular o tener calambres.
Los desequilibrios graves de electrolitos, como la deshidratación o la sobrehidratación, pueden causar problemas serios en el corazón y el cerebro, y necesitan atención médica rápida.
¿Cómo se miden los electrolitos?
Los niveles de electrolitos se pueden medir con un examen de sangre o de orina. Los más comunes que se miden son el sodio y el potasio.
Bebidas deportivas y electrolitos
Las bebidas deportivas a menudo contienen electrolitos. En la terapia de rehidratación oral, estas bebidas tienen sales de sodio y potasio que ayudan a reponer el agua y los electrolitos que el cuerpo pierde al hacer ejercicio, sudar, o por diarrea y vómito.
Sin embargo, para la mayoría de los niños, el agua es la mejor bebida durante el ejercicio normal. Las bebidas deportivas suelen tener mucha azúcar, lo que no es bueno para el consumo diario y puede afectar los dientes. Para problemas de diarrea o vómitos, existen sobres medicinales de rehidratación que son más adecuados.
También se pueden hacer bebidas con electrolitos en casa, usando las cantidades correctas de azúcar, sal y agua. El agua de coco natural también contiene electrolitos, pero es importante asegurarse de que no tenga azúcar añadida.
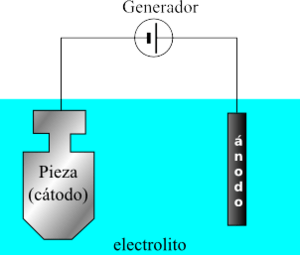
Electrolitos en la electroquímica
Cuando se coloca un electrodo en un electrolito y se aplica voltaje, el electrolito conduce la electricidad. Los electrones no pasan directamente a través del electrolito. En cambio, ocurren reacciones químicas en los electrodos: una reacción consume electrones en un lado (el cátodo) y otra produce electrones en el otro lado (el ánodo).
Los iones en el electrolito se mueven para equilibrar las cargas que se forman alrededor de los electrodos, permitiendo que las reacciones continúen y que la electricidad siga fluyendo.
Por ejemplo, en una disolución de sal común en agua:
- En el cátodo, el agua reacciona y produce gas dihidrógeno y iones hidróxido.
- En el ánodo, el agua reacciona y produce gas dioxígeno y iones hidrógeno.
Los iones de sodio positivos se mueven hacia el cátodo, y los iones de cloruro negativos se mueven hacia el ánodo, ayudando a que la corriente fluya.
Electrolitos secos
Los electrolitos secos son como geles con una estructura cristalina flexible.
¿Qué es un no electrolito?
Un no electrolito es una sustancia que, cuando se disuelve en agua, se separa en sus moléculas, pero estas moléculas no tienen carga eléctrica. Por ejemplo, el azúcar (sacarosa) se disuelve en agua, pero sus moléculas son neutras. Por eso, las disoluciones de no electrolitos no conducen la electricidad.
Ver también
Véase también
 En inglés: Electrolyte Facts for Kids
En inglés: Electrolyte Facts for Kids

