Pentacloruro de antimonio para niños
Datos para niños
Pentacloruro de antimonio |
||
|---|---|---|
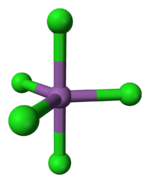 Modelo en 3 dimensiones
|
||
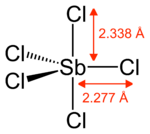 Fórmula estructural
|
||
En muestra
|
||
| Nombre IUPAC | ||
|
Pentacloruro de antimonio Cloruro de antimonio (V) |
||
| General | ||
| Otros nombres | Cloruro antimónico, Percloruro de antimonio. | |
| Fórmula estructural | 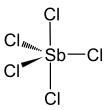 |
|
| Fórmula molecular | SbCl5 | |
| Identificadores | ||
| Número CAS | 7647-18-9 | |
| Número RTECS | CC5075000 | |
| ChemSpider | 10613049 | |
| PubChem | 90479165 24294, 90479165 | |
| UNII | 0S9308207L | |
|
InChI
InChI=InChI=1S/5ClH.Sb/h5*1H;/q;;;;;+5/p-5
Key: VMPVEPPRYRXYNP-UHFFFAOYSA-I |
||
| Propiedades físicas | ||
| Apariencia | líquido incoloro o amarillo rojizo (vaporoso), aceitoso. | |
| Olor | picante y desagradable. | |
| Densidad | 2336 kg/m³; 2,336 g/cm³ | |
| Masa molar | 295,7480791 g/mol | |
| Punto de fusión | 2,8 °C (276 K) | |
| Punto de ebullición | 140 °C (413 K) | |
| Presión de vapor | 0,16 kPa (25 °C); 4 kPa (40 °C); 7,7 kPa (100 °C) | |
| Viscosidad | 2,034 cP (29.4 °C) | |
| Índice de refracción (nD) | 1,59255 | |
| Propiedades químicas | ||
| Solubilidad en agua | reacciona. | |
| Solubilidad | soluble en alcohol, en HCl, en ácido tartárico, en CHCl3, en CS2, y en CCl4. | |
| Momento dipolar | 0 D | |
| Termoquímica | ||
| ΔfH0gas | - 437,2 kJ/mol | |
| S0gas, 1 bar | 295 J·mol–1·K | |
| Capacidad calorífica (C) | 120,9 J/mol·K (gas) | |
| Peligrosidad | ||
| SGA |   |
|
| Punto de inflamabilidad | 350 K (77 °C) | |
| NFPA 704 |
2
3
1
W
|
|
| Frases H | H314, H411. | |
| Frases P | P273, P280, P305+351+338, P310. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El pentacloruro de antimonio es un compuesto químico con la fórmula SbCl5. Es un líquido que puede ser incoloro o tener un tono amarillo rojizo. Tiene un olor fuerte y desagradable.
Este compuesto es muy corrosivo, lo que significa que puede dañar otros materiales. Por eso, se guarda en recipientes especiales de vidrio o PTFE (un tipo de plástico muy resistente).
Contenido
¿Cómo se prepara el pentacloruro de antimonio?
El pentacloruro de antimonio se fabrica haciendo pasar gas cloro a través de tricloruro de antimonio que está derretido. Es una reacción química donde se combinan estas dos sustancias.
- Fórmula de la preparación: SbCl3 + Cl2 → SbCl5
Cuando el pentacloruro de antimonio está en estado gaseoso, sus átomos se organizan de una forma especial llamada bipiramidal trigonal, que parece una doble pirámide unida por sus bases.
¿Cómo reacciona el pentacloruro de antimonio?
Este compuesto es muy reactivo, especialmente con el agua.
Reacción con el agua
Cuando el pentacloruro de antimonio entra en contacto con el agua, reacciona para formar pentóxido de antimonio y ácido clorhídrico. El ácido clorhídrico es una sustancia muy fuerte y corrosiva.
- Fórmula de la reacción con agua: 2 SbCl5 + 5 H2O → Sb2O5 + 10 HCl
También puede unirse al agua de otras maneras, formando compuestos con una o cuatro moléculas de agua.
¿Qué es un ácido de Lewis?
El pentacloruro de antimonio se comporta como un ácido de Lewis. Esto significa que puede aceptar pares de electrones de otras sustancias. Se usa en química para ayudar a que otras reacciones ocurran.
¿Para qué se usa el pentacloruro de antimonio?
El pentacloruro de antimonio tiene algunas aplicaciones importantes en la industria química:
- Catalizador: Se utiliza como catalizador en la polimerización. Un catalizador es una sustancia que acelera una reacción química sin consumirse en el proceso. La polimerización es el proceso de unir muchas moléculas pequeñas para formar una grande, como en la fabricación de plásticos.
- Cloración: También se usa para añadir átomos de cloro a otros compuestos orgánicos en un proceso llamado cloración.
¿Qué precauciones hay que tener con el pentacloruro de antimonio?
El pentacloruro de antimonio es una sustancia peligrosa y debe manejarse con mucho cuidado.
- Corrosivo: Es muy corrosivo y puede causar quemaduras graves en la piel y los ojos.
- Sensible a la humedad: Debe mantenerse alejado del calor y la humedad. Cuando entra en contacto con la humedad del aire, libera cloruro de hidrógeno en forma de gas, que es muy irritante y corrosivo.
- Daño a materiales: Debido a su naturaleza corrosiva, puede dañar incluso herramientas de acero inoxidable si hay humedad. No se debe usar con plásticos comunes, ya que puede derretirlos o quemarlos.
Véase también
 En inglés: Antimony pentachloride Facts for Kids
En inglés: Antimony pentachloride Facts for Kids


