Ozono para niños
Datos para niños
Ozono |
||
|---|---|---|
 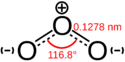   |
||
 |
||
| Nombre IUPAC | ||
| Trioxígeno | ||
| General | ||
| Fórmula estructural | Ver imagen | |
| Fórmula molecular | O3 | |
| Identificadores | ||
| Número CAS | 10028-15-6 | |
| ChEBI | 25812 | |
| ChEMBL | CHEMBL2447938 | |
| ChemSpider | 23208 | |
| DrugBank | DB12510 | |
| PubChem | 24823 | |
| UNII | 66H7ZZK23N | |
|
InChI
InChI=InChI=1S/O3/c1-3-2
Key: CBENFWSGALASAD-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Apariencia | Azul pálido | |
| Densidad | 2,14 kg/m³; 0,00214 g/cm³ | |
| Masa molar | 47,998 g/mol | |
| Punto de fusión | 80,7 K (−192 °C) | |
| Punto de ebullición | 161 K (−112 °C) | |
| Viscosidad | N/A | |
| Índice de refracción (nD) | 1,2226 (líquido) | |
| Propiedades químicas | ||
| Solubilidad en agua | 0,105 g/100 mL (0 °C) | |
| Termoquímica | ||
| ΔfH0sólido | 142,3 kJ/mol | |
| S0sólido | 237,7 J·mol–1·K–1 | |
| Riesgos | ||
| Riesgos principales | Exposición mayor de 0,05 PPM | |
| Ingestión | Irritación y dolor de la garganta y/o inflamación estomacal (en dosis altas) | |
| Inhalación | >0,05 PPM por 8 horas | |
| Piel | No reacciona | |
| Ojos | Irritación a más de 0,05 PPM | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
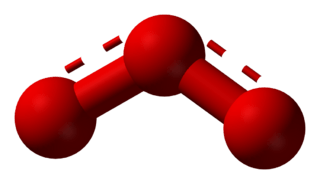
El ozono (O3) es una sustancia especial, ya que su molécula está formada por tres átomos de oxígeno. Normalmente, el gas oxígeno que respiramos tiene solo dos átomos (O2). El ozono se forma cuando los dos átomos de una molécula de oxígeno se separan y cada uno se une a otra molécula de oxígeno (O2), creando así una nueva molécula de ozono (O3).
A temperatura y presión normales, el ozono es un gas con un olor particular. Generalmente no tiene color, pero si hay mucha cantidad, puede verse un poco azulado. Si se respira en grandes cantidades, puede irritar los ojos o la garganta. El ozono que se encuentra cerca del suelo, llamado ozono troposférico, puede empeorar problemas respiratorios y causar irritación de garganta o dolor de cabeza.
Contenido
Descubrimiento del Ozono
El ozono fue el primer tipo de un mismo elemento químico (llamado alótropo) que fue descubierto por la ciencia. No se sabe con certeza quién lo descubrió primero, ya que varias personas contribuyeron a su conocimiento.
En 1785, el químico neerlandés Martinus van Marum notó un olor extraño al hacer experimentos con chispas eléctricas sobre agua. Él pensó que era por las reacciones eléctricas, pero en realidad había creado ozono sin saberlo.
Mucho tiempo después, en 1839, Christian Friedrich Schönbein sintió el mismo olor fuerte y lo reconoció como el que a menudo se percibe después de una tormenta eléctrica con rayos. Él logró separar este gas y lo llamó «ozono», que viene de la palabra griega ozein, que significa 'tener olor'. Por eso, a Schönbein se le considera generalmente el descubridor del ozono. La fórmula del ozono, O3, fue confirmada en 1867 por Schönbein, después de que Jacques-Louis Soret la determinara en 1865.
Durante mucho tiempo, el ozono se consideró bueno para la salud, especialmente en lugares altos o cerca del mar. Se creía que el aire marino era más saludable por su contenido de ozono, pero en realidad, el olor que causaba esta creencia venía de otras sustancias producidas por algas.
¿Cómo se produce el ozono artificialmente?
Existen varias maneras de crear ozono en laboratorios o fábricas, cada una con sus usos específicos.
Método de Efecto Corona
- Este es el método más común. Consiste en pasar una corriente eléctrica de alto voltaje a través de una corriente de oxígeno.
- La electricidad rompe las moléculas de oxígeno (O2) en átomos individuales.
- Estos átomos de oxígeno se unen rápidamente a otras moléculas de oxígeno (O2) para formar moléculas de ozono (O3).
- Es un método eficiente que se usa para purificar agua, tratar aguas residuales y desinfectar el aire.
Lámparas de Luz Ultravioleta
- La luz ultravioleta (UV) con mucha energía puede romper las moléculas de oxígeno, liberando átomos que luego se unen para formar ozono.
- Este método es menos eficiente que el efecto corona, pero es útil cuando se necesita una cantidad pequeña de ozono.
- Por ejemplo, se usa para esterilizar equipos médicos.
Otros Métodos de Producción
- El ozono también puede producirse en pequeñas cantidades como un subproducto de la destilación del agua.
- Otro método es la hidrólisis, que es la separación del agua usando electricidad. En este proceso, se producen átomos de oxígeno que luego forman ozono. Este método es más nuevo y se investiga como una forma eficiente y amigable con el ambiente para producir ozono.
Usos del Ozono
El ozono se puede producir artificialmente con un aparato llamado generador de ozono.
Se usa en la industria para crear algunos productos químicos, pero su uso principal es como desinfectante para limpiar el aire y el agua. Su característica más importante es que es un oxidante muy fuerte. También es muy importante en la atmósfera de la Tierra.
En la naturaleza, el ozono se forma durante las tormentas eléctricas. Cuando un rayo o relámpago pasa por el aire, la energía rompe las moléculas de oxígeno (O=O). Los átomos de oxígeno que se liberan se unen a otras moléculas de oxígeno, formando ozono (O3).
Limpieza de Agua y Aire
La Organización Mundial de la Salud (OMS) dice que el ozono es el desinfectante más eficaz contra todo tipo de microorganismos.
Se usó por primera vez para purificar agua en 1893 en Holanda. Hoy en día, hay miles de plantas de tratamiento de agua que usan ozono. Su uso se ha vuelto muy popular en industrias y hogares.
Las ventajas de usar ozono para el agua son:
- Elimina los malos olores y sabores del agua.
- No deja residuos químicos.
- Se puede usar con otros tratamientos.
- No cambia el nivel de acidez (pH) del agua.
- No le da color al agua.
Una gran ventaja es que el ozono se convierte en oxígeno, sin dejar sustancias dañinas en el agua.
Las ventajas de usar ozono para el aire son:
- Elimina virus, bacterias y hongos en el aire, ayudando a prevenir enfermedades que se transmiten por el aire, como la gripe o la Legionela.
- Elimina los malos olores.
- No deja residuos.
Por estas razones, usar ozono para desinfectar el aire es mejor que otros productos, porque es muy efectivo y se convierte rápidamente en oxígeno. El ozono es una forma muy activa de oxígeno que, incluso en pequeñas cantidades, puede limpiar el aire.
Ozono en la Atmósfera
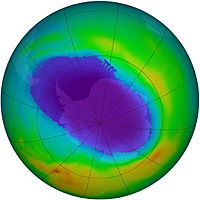
El ozono se encuentra en diferentes partes de la atmósfera: en la troposfera (la capa más cercana a la Tierra) y en la estratosfera (una capa más alta). La mayor concentración de ozono está en la estratosfera, a unos 25 kilómetros de altura, en lo que conocemos como la capa de ozono.
En la atmósfera, el ozono ayuda a limpiar el aire y, lo más importante, actúa como un filtro que nos protege de los rayos ultravioleta dañinos del Sol. Sin este filtro, la vida fuera del agua sería casi imposible. Por eso, la "capa de ozono" es tan vital.
El ozono natural es un gas de color azul pálido con un olor fuerte y característico. Se vuelve líquido a -111.9 °C y se congela a -193 °C.
El ozono en grandes cantidades y por mucho tiempo puede ser perjudicial para la salud. El ozono que se produce por la quema de combustibles y la actividad industrial a menudo se mezcla con dióxido de nitrógeno. A este ozono se le conoce como "ozono malo".
Ozono Estratosférico: El Ozono Bueno
El ozono se forma de manera natural en la estratosfera, creando la capa de ozono. Allí, la radiación ultravioleta del Sol rompe las moléculas de oxígeno (O2) en dos átomos. Estos átomos, que son muy activos, se unen a otras moléculas de O2 para formar ozono (O3).
Al mismo tiempo, el ozono también se destruye por la misma radiación ultravioleta. Así, se mantiene un equilibrio: el ozono se forma y se destruye constantemente, y en este proceso, absorbe la mayor parte de la radiación ultravioleta dañina. De esta forma, la capa de ozono actúa como un escudo que impide que esta radiación peligrosa llegue a la superficie de la Tierra.
Sin embargo, este equilibrio se ve afectado por sustancias contaminantes, como los compuestos clorofluorocarbonados (CFC). Estos compuestos suben a la atmósfera superior y aceleran la destrucción del ozono, más rápido de lo que se puede regenerar. Esto ha causado el agujero en la capa de ozono. Los científicos Mario Molina (México), Frank Sherwood Rowland (Estados Unidos) y Paul J. Crutzen (Países Bajos) descubrieron esto y ganaron el Premio Nobel de Química en 1995.
Para saber cuánto ozono hay en la atmósfera, se usan instrumentos en satélites, como el GOMOS en el satélite Envisat.
Ozono Troposférico: El Ozono Malo
También se le llama ozono ambiental. Es un gas sin color que se forma cerca del suelo por reacciones químicas entre gases de los vehículos y la industria (óxidos de nitrógeno y compuestos orgánicos volátiles) y la luz solar. Es una parte importante del esmog fotoquímico, esa neblina contaminante que a veces vemos en las ciudades.
Este ozono se encuentra en la parte más baja de la atmósfera. Cuando hay suficiente concentración, puede dañar la salud de las personas y la vegetación. Por ejemplo, puede causar tos, irritación en la garganta y los ojos, y dificultades para respirar. Por eso, en muchos lugares hay normas para controlar la cantidad de ozono en el aire.
Su formación comienza con la emisión de dióxido de nitrógeno (NO2) e hidrocarburos. Estos compuestos reaccionan con el calor y la luz del sol para producir ozono.
El ozono troposférico, junto con otros contaminantes, forma una neblina visible en zonas muy contaminadas, conocida como smog fotoquímico o smog de verano. Esto ocurre más a menudo en los meses cálidos, cuando hay más sol.
¿Es el Ozono Peligroso?
El ozono en la estratosfera nos protege de la radiación ultravioleta. Pero el ozono es un oxidante muy potente y, si se inhala, puede irritar las vías respiratorias. Aunque es raro que el ozono natural esté en concentraciones peligrosas para las personas, es un compuesto muy reactivo.
El límite seguro de exposición al ozono es de 0.1 partes por millón (ppm) durante ocho horas. A concentraciones más altas, puede causar problemas como fatiga, mareos o dificultad para dormir.
El ozono reacciona con las proteínas y grasas de nuestro cuerpo, especialmente en las membranas de las células. En concentraciones muy altas, también puede irritar la piel y los ojos.
A largo plazo, la exposición al ozono puede causar dolores de cabeza, irritación de nariz y garganta, opresión en el pecho y congestión pulmonar en personas que trabajan expuestas a él.
Es importante no confiar solo en el olor para detectar fugas de ozono en la industria, porque incluso pequeñas fugas pueden hacer que nuestro sentido del olfato se acostumbre y no las detecte. Por eso, se deben usar detectores especiales.
Después de usar ozono artificialmente, antes de liberarlo al ambiente, debe pasar por un equipo que lo convierta de nuevo en oxígeno para evitar cualquier peligro.
¿Qué hacer si alguien se ve afectado por el ozono?
Si una persona se siente mal por el ozono, se deben seguir estos pasos:
- Llevar a la persona a un lugar con aire fresco y sin contaminación.
- Mantener a la persona en reposo.
- Si tiene problemas para respirar, darle oxígeno con el equipo adecuado y por alguien capacitado.
- Si la respiración es débil o se detiene, iniciar la respiración asistida (boca a boca o boca a nariz).
- Buscar ayuda médica de inmediato.
- El tratamiento para la exposición al ozono se enfoca en los síntomas, e incluye reposo, medicamentos para el dolor y antibióticos si el médico los receta.
Galería de imágenes
Véase también
 En inglés: Ozone Facts for Kids
En inglés: Ozone Facts for Kids