Nitrito de sodio para niños
Datos para niños
Nitrito de sodio |
||
|---|---|---|
 |
||
 |
||
| General | ||
| Otros nombres | Nitrito sódico E 250 |
|
| Fórmula molecular | NaNO2 | |
| Identificadores | ||
| Número CAS | 7632-00-0 | |
| Número RTECS | RA1225000 | |
| ChEBI | 78870 | |
| ChEMBL | CHEMBL93268 | |
| ChemSpider | 22689 | |
| PubChem | 24269 | |
| UNII | M0KG633D4F | |
| KEGG | D05865 | |
|
InChI
InChI=InChI=1S/HNO2.Na/c2-1-3;/h(H,2,3);/q;+1/p-1
Key: LPXPTNMVRIOKMN-UHFFFAOYSA-M |
||
| Propiedades físicas | ||
| Apariencia | polvo blanco | |
| Densidad | 2168 kg/m³; 2,168 g/cm³ | |
| Masa molar | 68,9953 g/mol | |
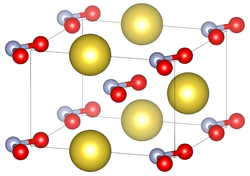
| Estructura cristalina | Ortorrómbico | |
| Propiedades químicas | ||
| Solubilidad en agua | 82 g/100 ml (20 °C) | |
| Familia | nitritos | |
| Peligrosidad | ||
| NFPA 704 |
0
3
1
OX
|
|
| Frases R | R8, R25, R50 | |
| Frases S | S1/2, S45, S61 | |
| Riesgos | ||
| Más información | MSDS Externo | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
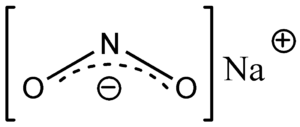
El nitrito de sodio es un compuesto químico que se forma con sodio y nitrógeno. Su fórmula es NaNO2. Es muy conocido por su uso en la industria alimentaria, especialmente en la de la carne. Allí se usa para conservar alimentos y para que mantengan su color. En las etiquetas de los productos, lo puedes encontrar con el código E 250.
Es importante saber que su uso está regulado. Esto se debe a que, en ciertas condiciones, puede formar otras sustancias llamadas nitrosaminas.
Contenido
¿Qué es el Nitrito de Sodio?
El nitrito de sodio es un polvo de color blanco que parece cristal. Se disuelve fácilmente en agua. Aunque no se quema fácilmente, si se calienta a temperaturas muy altas (como 1000 °C), puede reaccionar de forma fuerte liberando oxígeno.
Propiedades Químicas y Físicas
- Fórmula: NaNO2
- Densidad: 2,17 gramos por centímetro cúbico (g/cm³)
- Masa molar: 68,9953 gramos por mol (g/mol)
- Punto de fusión: 271 °C
- Solubilidad: Se disuelve en agua.
Este compuesto es un buen agente oxidante en ambientes húmedos. También ayuda a detener el crecimiento de algunas bacterias dañinas, como la clostridium botulinum, que causa una enfermedad llamada botulismo.
Sabías que algunas bacterias en tu flora intestinal pueden producir nitritos. Esto ocurre cuando comes ciertos alimentos que contienen nitratos, como la remolacha, las espinacas o el apio.
Usos del Nitrito de Sodio
El nitrito de sodio se usa principalmente para conservar alimentos y para mantener el color de los productos de carne.
En la Industria Alimentaria
- Se mezcla con otras sales para crear las llamadas sales de curado. Estas sales incluyen nitritos y nitratos de sodio y de potasio (E249).
- Ayuda a prevenir que los alimentos se echen a perder por bacterias, especialmente el botulismo.
- Se usa en el proceso de salazón de carnes, como el jamón y las cecinas, y también en pescados.
- Mejora el sabor y el color de los alimentos. Por ejemplo, la carne tratada con nitrito de sodio tiene un color rojo-púrpura cuando está cruda. Esto se debe a una reacción química con la mioglobina de la carne. Al cocinarla, el color cambia a un rosado característico.
Otros Usos Importantes
- Fabricación de tintes: Se usa para hacer tintes especiales llamados azoicos.
- Industria química: Es útil en la fabricación de caucho y en la creación de otras sustancias, como el óxido nítrico.
- Química analítica: Se emplea como un reactivo en laboratorios para analizar sustancias.
- Protección de materiales: Actúa como un anticorrosivo para las estructuras de hormigón armado, ayudando a protegerlas.
- Medicina: En algunos casos, se usa como medicamento inyectable. Puede ayudar a modificar la hemoglobina en la sangre y se utiliza para tratar ciertas situaciones médicas, como un vasodilatador.
¿Cómo se Prepara el Nitrito de Sodio?
La preparación del nitrito de sodio es un proceso químico. Se basa en una reacción donde el nitrato se transforma en nitrito usando un elemento como el plomo.
Para hacerlo, se calienta nitrato sódico en un recipiente hasta que se derrite. Luego, se añade poco a poco plomo raspado. Se sigue calentando hasta que el plomo se haya transformado. Después, se deja enfriar. El producto se lava varias veces con agua caliente y se filtra. Finalmente, se neutraliza con ácido nítrico y se deja que se formen cristales, que luego se lavan con alcohol.
Nitrito de Sodio y la Salud
Las autoridades de salud han estudiado el nitrito de sodio. A finales de los años 1970, algunos estudios en animales de laboratorio mostraron que el nitrito de sodio, usado como aditivo en alimentos, podría estar relacionado con ciertos riesgos para la salud.
Esto se debe a que, bajo ciertas condiciones, el nitrito de sodio puede reaccionar en los alimentos y formar sustancias llamadas nitrosaminas. Estas sustancias se pueden generar, por ejemplo, al freír carne a altas temperaturas. También se ha visto que las cantidades de nitrosaminas pueden aumentar en algunos alimentos, como el pescado, cuando se congelan.
Se ha descubierto que consumir vitamina C (que es un antioxidante) puede ayudar a reducir la formación de nitrosaminas en la carne. Por esta razón, el uso del nitrito de sodio como conservante está regulado en muchos países, incluyendo España, donde se establecen cantidades máximas permitidas en los alimentos.
Véase también
 En inglés: Sodium nitrite Facts for Kids
En inglés: Sodium nitrite Facts for Kids
- Nitrito de potasio