Molécula para niños
Una molécula es un grupo de al menos dos átomos que están unidos fuertemente entre sí. Estos átomos forman una unidad estable y eléctricamente neutra. Piensa en una molécula como un pequeño equipo de átomos que trabajan juntos.
En química orgánica y bioquímica, el término "molécula" se usa de forma más amplia para incluir los compuestos orgánicos y las biomoléculas, que son muy importantes para la vida.
Antes, se pensaba que una molécula era la parte más pequeña de una sustancia que podía existir por sí misma y mantener todas sus propiedades. Según esa idea, incluso un solo átomo de un gas noble (como el helio) podría considerarse una molécula, aunque no esté unido a otros átomos.
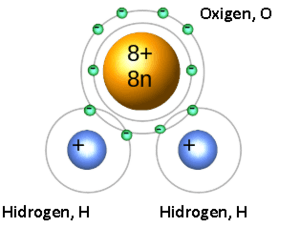
Una molécula puede estar hecha de átomos del mismo elemento químico, como el oxígeno que respiramos (O2), o de átomos de diferentes elementos, como el agua (H2O). Los átomos que se unen por enlaces más débiles, como los enlaces de hidrógeno, no suelen considerarse parte de una sola molécula.
Las moléculas son muy comunes en las sustancias orgánicas y en los seres vivos. También forman la mayor parte de los océanos y de la atmósfera. Sin embargo, muchas sustancias sólidas, como la mayoría de los minerales de la corteza de la Tierra, no están formadas por moléculas individuales. En los cristales, como la sal de mesa o el diamante, los átomos se repiten en un patrón regular, pero no forman moléculas separadas. Lo mismo ocurre con los metales.
Casi toda la química orgánica y gran parte de la química inorgánica se dedican a crear y estudiar cómo reaccionan las moléculas. La bioquímica y la biología molecular estudian a los seres vivos a nivel molecular. También se investiga cómo las moléculas interactúan entre sí, lo que explica propiedades como la solubilidad (si algo se disuelve en agua) o el punto de ebullición (a qué temperatura hierve).
Las moléculas rara vez están completamente solas, excepto en gases muy dispersos. Generalmente, interactúan entre sí, por ejemplo, en el hielo, donde las moléculas de agua forman una red cristalina, o en el agua líquida, donde sus interacciones cambian rápidamente. Las fuerzas que las unen son las fuerzas de Van der Waals y los puentes de hidrógeno.
Contenido
¿Qué es la ciencia molecular?
La ciencia que estudia las moléculas se llama química molecular o física molecular. La química molecular se enfoca en cómo las moléculas interactúan para formar y romper enlaces químicos. La física molecular se ocupa de la estructura y las propiedades de las moléculas. Ambas están muy relacionadas.
En estas ciencias, una molécula es un sistema estable de dos o más átomos unidos. A veces, los iones poliatómicos (moléculas con carga eléctrica) también se consideran moléculas. El término "molécula inestable" se usa para grupos de átomos que duran muy poco tiempo, como los radicales o los iones moleculares.
Historia y origen de la palabra "molécula"
La palabra "molécula" viene del latín moles, que significa 'masa', y el sufijo diminutivo -ula, que significa 'pequeña'. Así, "molécula" significa 'masa pequeña'.
La definición de molécula ha cambiado con el tiempo a medida que hemos aprendido más sobre cómo están hechas las cosas. Al principio, se definía como la parte más pequeña de una sustancia pura que mantenía sus propiedades. Sin embargo, esta definición no funcionaba bien para sustancias como las rocas, las sales o los metales, que están formadas por grandes redes de átomos o iones, no por moléculas separadas.
¿Cómo se definen las moléculas?
Una molécula es la parte más pequeña de una sustancia química que mantiene sus propiedades. A partir de ella, se puede reconstruir la sustancia sin que ocurran reacciones químicas. Esta definición es útil para sustancias que realmente están hechas de moléculas.
Las moléculas que son "lábiles" (inestables) pueden deshacerse en poco tiempo. Si duran muy poco, como el tiempo de unas pocas vibraciones, se consideran un estado de transición y no una molécula completa.
Las entidades que son como moléculas pero tienen una carga eléctrica se llaman iones poliatómicos o iones moleculares. Las sales que tienen iones poliatómicos se consideran materiales moleculares.
Las moléculas están formadas por átomos unidos por enlaces químicos. Son la porción más pequeña de materia que aún conserva las propiedades de la materia original.
Tipos de moléculas
Las moléculas se pueden clasificar en:
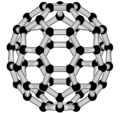
- Moléculas discretas: Son aquellas que tienen un número fijo y definido de átomos. Pueden ser del mismo elemento (como el dinitrógeno o el fullereno) o de diferentes elementos (como el agua).
-
Molécula de agua, muy importante en la vida y en la industria.
- Macromoléculas o polímeros: Son moléculas muy grandes formadas por la repetición de unidades más simples. Tienen un peso muy alto.
-
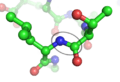
Enlace peptídico que une los péptidos para formar proteínas.
-
Representación de un fragmento lineal de polietileno, el plástico más usado.
¿Cómo se describen las moléculas?
La forma de describir una molécula depende de su complejidad.
- La fórmula molecular es útil para moléculas sencillas, como H2O para el agua o NH3 para el amoniaco. Muestra los símbolos de los elementos y cuántos átomos de cada uno hay.
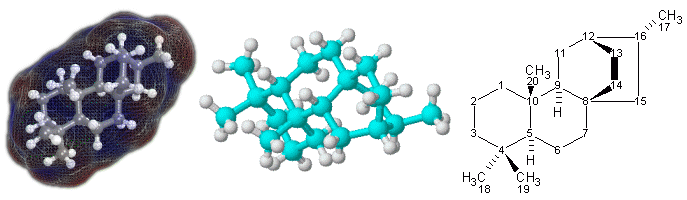
- Para moléculas más complejas, como las que se encuentran en química orgánica, se usan fórmulas estructurales o fórmulas esqueletales. Estas muestran cómo están organizados los átomos en el espacio.
- Cuando se quieren mostrar muchas propiedades o se trata de sistemas muy complejos como proteínas, ADN o polímeros, se usan modelos tridimensionales (físicos o en computadora). En las proteínas, por ejemplo, se describe su estructura en varios niveles: primaria, secundaria, terciaria y cuaternaria, que explican cómo se pliegan y organizan.
Moléculas y la teoría cuántica
Las leyes de la física clásica no podían explicar por qué las moléculas existen y son estables. Según esas leyes, los electrones deberían perder energía y caer hacia el núcleo atómico. Sin embargo, la mecánica cuántica nos dio el primer modelo que explicaba por qué los átomos son estables y cómo se comportan.
En la mecánica cuántica, una molécula se describe como un sistema de electrones y núcleos. Las interacciones entre ellos se explican con un concepto llamado "hamiltoniano cuántico". Este nos ayuda a entender las energías que el sistema puede tener y cómo se distribuyen los electrones en los orbitales moleculares. A partir de esto, podemos predecir las propiedades químicas de la molécula.
Una simplificación importante en el estudio de las moléculas es la aproximación de Born-Oppenheimer. Como los núcleos de los átomos son mucho más pesados que los electrones, se asume que los núcleos están casi fijos mientras los electrones se mueven. Esto simplifica mucho los cálculos y ayuda a entender por qué las moléculas son estables y no se desintegran.
Galería de imágenes
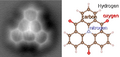
-
Imagen de una molécula de PTCDA tomada con un microscopio de fuerza atómica (AFM).
-
Imagen de microscopía de túnel de barrido de moléculas de pentaceno.
Véase también
 En inglés: Molecule Facts for Kids
En inglés: Molecule Facts for Kids
- Compuesto químico
- Nanotecnología
- Número de Avogadro
- Volumen molar
- Sólidos moleculares