Física del estado sólido para niños
La física del estado sólido es una parte de la física de la materia condensada que se dedica a estudiar los sólidos. Los sólidos son materiales que tienen una forma y volumen definidos, como una roca o un trozo de metal. Esta rama de la física investiga las propiedades de estos materiales usando herramientas como la mecánica cuántica (que estudia el mundo muy pequeño de los átomos), la cristalografía (que analiza cómo se organizan los átomos en los cristales), el electromagnetismo (que trata la electricidad y el magnetismo) y la metalurgia física (que estudia los metales).
La física del estado sólido es muy importante porque es la base de la ciencia de materiales. Gracias a ella, se han podido desarrollar tecnologías clave como los transistores y los materiales semiconductores, que son esenciales para la microelectrónica en nuestros dispositivos electrónicos.
La mayoría de las investigaciones en esta área se centran en los cristales. Esto se debe a que los átomos en un cristal se repiten de forma ordenada, lo que facilita mucho los cálculos matemáticos. Además, los materiales cristalinos suelen tener propiedades eléctricas, magnéticas, ópticas o mecánicas muy útiles para la ingeniería.
Para entender cómo se comportan los electrones en los sólidos, los científicos usan la Ecuación de Schrödinger, que es una herramienta de la mecánica cuántica. Una idea fundamental es el teorema de Bloch, que describe cómo se mueven los electrones en un material con una estructura atómica repetitiva. Aunque los átomos de un cristal se mueven un poco, esta idea es una excelente aproximación que ha permitido grandes avances en el estudio de los sólidos.
Contenido
- ¿Qué son los sólidos y cómo se forman?
- Historia de la física del estado sólido
- ¿Cómo se organizan los átomos en los sólidos?
- ¿Cómo se mueven los electrones en los sólidos?
- Conductividad eléctrica en sólidos
- Temas importantes en física del estado sólido
- Investigaciones modernas en física del estado sólido
- Galería de imágenes
- Véase también
¿Qué son los sólidos y cómo se forman?
Los cuerpos sólidos están hechos de átomos que están muy juntos y unidos por fuerzas fuertes. Estas fuerzas son las que dan a los sólidos sus propiedades especiales, como su dureza, cómo conducen el calor o la electricidad, y cómo reaccionan a la luz o a los imanes.
Una característica importante de muchos sólidos es su estructura cristalina. Esto significa que sus átomos están organizados en patrones que se repiten regularmente, como si formaran un edificio con bloques iguales. La forma en que los átomos se unen puede variar:
- Algunos sólidos, como la sal común, se mantienen unidos por enlaces iónicos. Esto ocurre por la atracción entre iones con cargas opuestas.
- En otros, como el diamante, los átomos comparten electrónes, formando enlaces covalentes muy fuertes.
- Sustancias como el neón se unen por fuerzas de Van der Waals, que son atracciones débiles entre átomos o moléculas neutras.
- Los metales se mantienen unidos por un "gas electrónico", que son electrones libres compartidos por todos los átomos. Esto les da muchas de sus propiedades, como la capacidad de conducir electricidad.
Historia de la física del estado sólido
La investigación sobre las propiedades de los sólidos ha existido por siglos. Sin embargo, la física del estado sólido como un campo de estudio independiente surgió en la década de 1940. En Estados Unidos, se creó una división especial dentro de la Sociedad Americana de Física para los físicos que trabajaban en la industria.
En Europa, también se formaron grandes grupos de físicos del estado sólido después de la Segunda Guerra Mundial. Tanto en Estados Unidos como en Europa, este campo creció mucho gracias a las investigaciones sobre semiconductores (materiales clave para la electrónica), la superconductividad (cuando los materiales conducen electricidad sin resistencia) y otros fenómenos.
Durante la Guerra Fría, la investigación en física del estado sólido a menudo iba más allá de los sólidos. Por eso, en las décadas de 1970 y 1980, algunos físicos crearon el campo de la física de la materia condensada. Este campo estudia no solo sólidos, sino también líquidos, gases especiales y otras formas complejas de materia, usando técnicas similares. Hoy en día, la física del estado sólido se considera una parte de la física de la materia condensada, enfocada en los sólidos con estructuras cristalinas regulares.
¿Cómo se organizan los átomos en los sólidos?
La física del estado sólido nos ayuda a entender las propiedades mecánicas, térmicas, eléctricas, magnéticas y ópticas de los sólidos.
La forma en que la materia existe (sólido, líquido o gas) depende de la presión y la temperatura. Estas condiciones también influyen en cómo se organiza la estructura interna de un sólido. Cada elemento químico tiene sus propias condiciones para cambiar de fase.
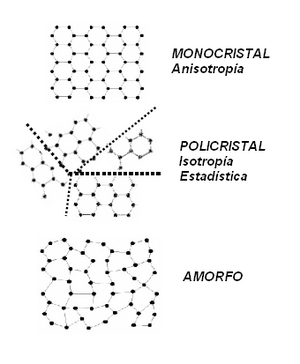
Según cómo se ordenan los átomos en el espacio, podemos clasificar los sólidos en:
- Monocristal: Los átomos están muy ordenados y se repiten en un patrón perfecto en todo el material. Un ejemplo es un cristal de cuarzo. Estos materiales pueden tener propiedades diferentes si los miras en distintas direcciones (se dice que son anisótropos).
- Policristal: Está formado por muchas pequeñas regiones, cada una de las cuales es un monocristal, pero estas regiones están orientadas de forma diferente entre sí. La mayoría de los metales son policristalinos. Sus propiedades suelen ser las mismas en todas las direcciones (se dice que tienen isotropía estadística).
- Amorfos: No tienen una estructura ordenada de átomos. Sus átomos están distribuidos al azar, como en el vidrio o el plástico.
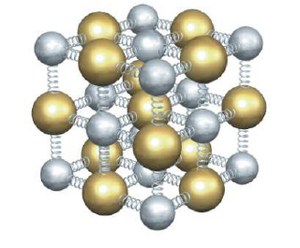
Imagina que los átomos en un sólido están conectados por pequeños "muelles". La energía dentro del sólido viene de la energía de esos muelles y del movimiento de los átomos. La presión mide cuánto se comprimen los átomos, y la temperatura mide la energía de movimiento de los átomos. Esto nos ayuda a entender por qué un material puede ser sólido y si formará una estructura cristalina.
Un mismo elemento puede formar diferentes estructuras cristalinas bajo distintas condiciones. Por ejemplo, el carbono puede cristalizar como grafito (el material de las minas de lápiz) o como diamante (una de las sustancias más duras). Sus propiedades son muy diferentes, ¡pero ambos están hechos de carbono!
Para que se formen cristales, a menudo se calienta el material a una temperatura de cristalización (por ejemplo, unos 200 °C). Luego, se enfría lentamente. Este enfriamiento lento permite que los átomos se organicen de forma ordenada y formen un cristal. Si el enfriamiento es muy rápido, los átomos no tienen tiempo de organizarse, y el material se vuelve amorfo.
En la naturaleza, los policristales son más comunes que los monocristales perfectos.
Existen 14 tipos básicos de estructuras cristalinas, llamadas redes de Bravais. Estas redes describen cómo se organizan los átomos en el espacio. Por ejemplo, el fósforo cristaliza en una estructura cúbica, el hierro en una cúbica centrada en el cuerpo (bcc) y la plata en una cúbica centrada en las caras (fcc).
Para estudiar la estructura interna de un cristal, los científicos usan la difracción de rayos X. Cuando los fotónes (partículas de luz) inciden en el cristal, se desvían de una manera específica que revela la posición de los átomos. La ley de Bragg describe este fenómeno y es fundamental para entender la estructura de los cristales.
Estas propiedades de los sólidos cristalinos se usan en la tecnología. Por ejemplo, los CD-RW y DVD-RW graban información cambiando la estructura de su material entre amorfa y cristalina.
¿Cómo se mueven los electrones en los sólidos?
El comportamiento de los electrones en los sólidos se rige por la mecánica cuántica. Esto significa que:
- Los electrones no pueden tener cualquier nivel de energía; solo pueden tener energías específicas, como si fueran escalones. Un grupo de niveles de energía muy cercanos se llama "banda de energía".
- No todas las bandas de energía están ocupadas por igual. Algunas tienen más electrones, otras están casi vacías, y algunas pueden estar completamente vacías.
Bandas de energía
El modelo de Drude intentó explicar cómo los materiales conducen electricidad, pero no era suficiente para entender los semiconductores. Por eso, surgió el modelo de bandas energéticas. Este modelo explica la conductividad de los materiales basándose en cómo se distribuyen los electrones en diferentes "bandas" de energía.
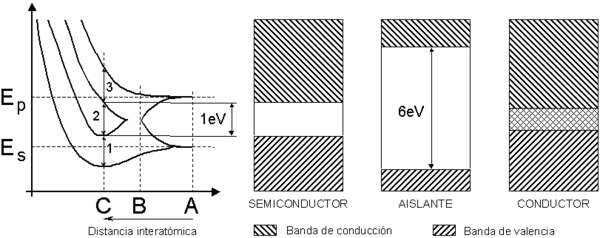
Imagina un cristal de silicio. Cuando los átomos de silicio están separados, sus electrones tienen ciertos niveles de energía. Pero cuando los átomos se unen para formar un cristal, sus niveles de energía se combinan y forman bandas. Las tres bandas principales son:
- Banda de valencia: Contiene los electrones que están fuertemente unidos a los átomos.
- Banda prohibida: Es un espacio donde los electrones no pueden tener energía.
- Banda de conducción: Si los electrones llegan a esta banda, pueden moverse libremente y conducir electricidad.
La probabilidad de que los electrones ocupen una banda u otra se describe con la estadística de Fermi-Dirac, y un concepto clave es la energía de Fermi.
Conductividad eléctrica en sólidos
Un sólido conduce electricidad cuando su banda de conducción está parcialmente llena de electrones. También puede conducir si su banda de conducción está vacía, pero se superpone con la banda de valencia, permitiendo que los electrones se muevan fácilmente.
Temas importantes en física del estado sólido
- Electrónica de estado sólido
- Sólido amorfo
- Estructura cristalina
- Defecto cristalino
- Cuasicristal
- Modelo de electrón libre
- Cristalografía de rayos X
- Estructura electrónica
- Banda prohibida
- Banda de conducción
- Masa efectiva
- Hueco de electrón
- Energía de Fermi
- Banda de valencia
- Transporte electrónico
- Modelo de Drude
- Conducción eléctrica
- Efecto Hall
- Superconductividad
- Características mecánicas
- Elasticidad
- Fonón (vibraciones de redes cristalinas)
- Características ópticas
- Óptica cristalina
Investigaciones modernas en física del estado sólido
Algunos de los temas de investigación actuales en física del estado sólido incluyen:
- Superconductividad de alta temperatura
- Cuasicristales
- Vidrio de espín
- Materiales con propiedades electrónicas complejas
- Materiales monocapa (materiales extremadamente delgados, de una sola capa de átomos)
- Nanomateriales (materiales muy pequeños, a escala nanométrica)
Galería de imágenes
Véase también
 En inglés: Solid-state physics Facts for Kids
En inglés: Solid-state physics Facts for Kids
- Física de la materia condensada
- Metalografía
- Teoría de bandas