Cromato de potasio para niños
Datos para niños
Cromato de potasio |
||
|---|---|---|
 |
||
 |
||
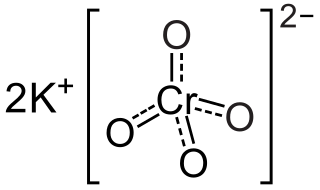
| Nombre IUPAC | ||
| Cromato(VI) de potasio | ||
| General | ||
| Fórmula estructural | K2CrO4 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | [7789-00-6] | |
| Número RTECS | GB2940000 | |
| ChEBI | 75249 | |
| ChemSpider | 22999 | |
| PubChem | 24597 | |
| UNII | 5P0R38CN2X | |
|
InChI
InChI=InChI=1S/Cr.2K.4O/q;2*+1;;;2*-1
Key: XMXNVYPJWBTAHN-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Apariencia | Amarillo intenso | |
| Densidad | 2730 kg/m³; 2,73 g/cm³ | |
| Masa molar | 194,1896 g/mol | |
| Punto de fusión | 1248 K (975 °C) | |
| Punto de ebullición | 1273 K (1000 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | 637 g/l a 20 °C en agua | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El cromato de potasio, con la fórmula química K2CrO4, es un tipo de sal que contiene potasio y cromo. Es conocido por su color amarillo brillante y por ser un oxidante fuerte.
Contenido
Cromato de Potasio: Un Compuesto Químico Interesante
El cromato de potasio es un compuesto químico que se usa en diferentes áreas. Su fórmula nos dice que está hecho de dos átomos de potasio (K), un átomo de cromo (Cr) y cuatro átomos de oxígeno (O).
¿Qué es el Cromato de Potasio?
Este compuesto es una sal ternaria, lo que significa que está formado por tres tipos de elementos. El cromo en esta sal tiene un "estado de oxidación" de +6, lo que lo hace un oxidante muy potente. Esto significa que puede quitar electrones a otras sustancias en reacciones químicas.
¿Para qué se Usa el Cromato de Potasio?
Una de las aplicaciones más importantes del cromato de potasio es en los laboratorios de química.
Usos como Indicador Químico
Se utiliza como un "indicador" en un tipo de experimento llamado valoración argentométrica. En este proceso, se busca saber cuánto cloruro hay en una muestra.
- Se añade una solución de nitrato de plata (AgNO3) a la muestra.
- Los cloruros reaccionan con la plata y forman un sólido llamado cloruro de plata (AgCl), que se precipita (se asienta en el fondo).
- El cromato de potasio se añade a la solución. No reacciona hasta que todos los cloruros se han precipitado.
- Una vez que todos los cloruros han reaccionado, el cromato de potasio reacciona con la plata restante.
- Esta reacción forma un precipitado de color anaranjado rojizo, lo que indica que la reacción de los cloruros ha terminado. Es muy fácil de ver.
Propiedades Físicas del Cromato de Potasio
El cromato de potasio es un sólido que se presenta en forma de cristales.
Apariencia y Solubilidad
- Tiene un color amarillo limón muy llamativo.
- Es muy estable, lo que significa que no cambia fácilmente.
- Se disuelve muy bien en agua.
Densidad y Puntos de Fusión/Ebullición
- Su densidad es de 2,73 g por cm³.
- Tiene un punto de fusión muy alto, de 975 °C. Esto significa que necesita mucho calor para derretirse.
- Su punto de ebullición es de 1000 °C, lo que indica que se necesita aún más calor para que se convierta en gas.
¿Cómo se Fabrica el Cromato de Potasio?
El cromato de potasio se puede obtener a través de una reacción química.
Proceso de Síntesis
Se produce al hacer reaccionar carbonato de potasio con dicromato de potasio. La reacción se ve así:
- Error al representar (Falta el ejecutable <code>texvc</code>. Véase math/README para configurarlo.): \mathrm{K_2CO_3 + K_2Cr_2O_7 \rightarrow 2 \ K_2CrO_4 + CO_2}
En esta reacción, se forma cromato de potasio (K2CrO4) y también se libera dióxido de carbono (CO2).
Reacciones Químicas del Cromato
El ion cromato (CrO42-) es muy reactivo.
Reacciones con Iones Metálicos
Puede unirse a muchos iones de metal diferentes, como el bario (Ba2+), el plomo (Pb2+) o el mercurio (Hg22+). Cuando se une a ellos, forma nuevos compuestos que se precipitan.
- Por ejemplo, con el bario:
: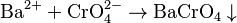 Esto forma cromato de bario, que es un sólido.
Esto forma cromato de bario, que es un sólido.
- Y con la plata:
: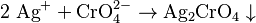 Esto forma cromato de plata, que también es un sólido.
Esto forma cromato de plata, que también es un sólido.
Precauciones al Usar Cromato de Potasio
Es muy importante manejar el cromato de potasio con mucho cuidado.
Seguridad en el Manejo
- Es un compuesto que puede ser muy dañino si se ingiere o se inhala.
- Debido a que es un oxidante fuerte, puede reaccionar de forma muy rápida y enérgica con otras sustancias.
- Si entra en contacto con ciertos compuestos orgánicos, puede causar reacciones intensas.
- Por estas razones, siempre se deben seguir las normas de seguridad en el laboratorio cuando se trabaja con él.
Véase también
 En inglés: Potassium chromate Facts for Kids
En inglés: Potassium chromate Facts for Kids
- Dicromato
- Dicromato de potasio
- Dicromato de amonio

