ADN no codificante para niños
Las secuencias de ADN no codificante son partes del ácido desoxirribonucleico (ADN) de un organismo que no contienen las instrucciones para fabricar proteínas. Aunque no producen proteínas, estas partes del ADN son muy importantes.
Algunas de estas secuencias de ADN no codificante se copian en moléculas de ARN no codificantes especiales. Estos ARN tienen funciones vitales, como el ARN de transferencia (ARNt), el ARN ribosómico (ARNr) y el ARN regulador.
Otras funciones del ADN no codificante incluyen:
- Ayudar a controlar cuándo y cómo se usan las instrucciones del ADN para crear proteínas.
- Servir como puntos de "enganche" para otras estructuras importantes.
- Marcar los puntos de inicio para copiar el ADN.
- Formar los centrómeros (partes centrales de los cromosomas) y los telómeros (extremos de los cromosomas).
La cantidad de ADN no codificante varía mucho entre diferentes especies. A menudo, solo una pequeña parte del genoma (todo el ADN de un organismo) se encarga de dar las instrucciones para las proteínas. Sin embargo, cada vez se descubre que una parte más grande de ese ADN no codificante tiene funciones importantes, especialmente en la regulación de los genes.
Durante mucho tiempo, a una gran parte del ADN no codificante se le llamó "ADN basura" porque se pensaba que no tenía ninguna función biológica. Pero esta idea ha cambiado mucho.
El proyecto internacional Encyclopedia of DNA Elements (ENCODE) descubrió que al menos el 80% del ADN del genoma humano tiene algún tipo de actividad bioquímica. Esto significa que está haciendo algo, aunque no siempre sea una función biológica clara. Algunos científicos han debatido si toda actividad bioquímica significa una función biológica. Las estimaciones de la parte del genoma humano que es biológicamente funcional, basadas en la genómica comparativa (comparar el ADN entre especies), varían entre el 8% y el 15%. Sin embargo, otros argumentan que estas estimaciones pueden ser bajas.
Se ha descubierto que el ADN no codificante participa en la epigenética (cambios que afectan cómo se usan los genes sin cambiar el ADN en sí) y en complejas redes de cómo los genes interactúan. Su estudio es clave en la biología evolutiva del desarrollo, que investiga cómo los seres vivos cambian y se desarrollan a lo largo del tiempo.
Contenido
Cantidad de ADN no codificante en el genoma

La cantidad total de ADN en el genoma es muy diferente entre los organismos, y la proporción de ADN que codifica proteínas y el que no, también varía enormemente. Por ejemplo, se cree que más del 98% del genoma humano no codifica proteínas, incluyendo la mayoría de las secuencias dentro de los intrones y gran parte del ADN entre genes. En cambio, en las bacterias típicas, solo el 20% de su genoma no codifica.
En los eucariotas (organismos con células complejas, como plantas y animales), el tamaño del genoma y, por lo tanto, la cantidad de ADN no codificante, no siempre está relacionado con la complejidad del organismo. Esto se conoce como el enigma de valor C. Por ejemplo, el genoma de la ameba unicelular Polychaos dubium tiene más de 200 veces la cantidad de ADN que el de los humanos. El genoma del pez globo Takifugu rubripes es solo una octava parte del tamaño del genoma humano, pero tiene un número similar de genes. Aproximadamente el 90% del genoma de Takifugu es ADN no codificante. Esto nos dice que la mayor parte de la diferencia en el tamaño del genoma se debe a la cantidad de ADN no codificante, no a la cantidad de ADN que codifica proteínas.
En 2013, se descubrió un nuevo "récord" para el genoma eucariota más eficiente en la planta Utricularia gibba, que tiene solo un 3% de ADN no codificante y un 97% de ADN que sí codifica. Esta planta parece haber eliminado partes de su ADN no codificante, lo que sugiere que este tipo de ADN podría no ser tan esencial para todas las plantas, aunque es muy útil para los humanos. Otros estudios en plantas han encontrado funciones cruciales en partes del ADN no codificante que antes se consideraban sin importancia, lo que ha ampliado nuestra comprensión de cómo se regulan los genes.
Tipos de secuencias de ADN no codificantes
Elementos cis y transreguladores
Los elementos reguladores cis son secuencias de ADN que controlan la copia de un gen cercano. Muchos de estos elementos son importantes en la evolución y el control del desarrollo de un organismo. Los elementos cis pueden encontrarse en regiones no traducidas o dentro de los intrones. Los elementos transreguladores controlan la copia de un gen que está lejos.
Los promotores ayudan a que un gen específico se copie y suelen estar antes de la parte que codifica. Las secuencias potenciadoras también pueden influir en la cantidad de copias de genes, incluso si están muy lejos.
Intrones
Los intrones son secciones no codificantes dentro de un gen. Se copian en el ARN mensajero precursor, pero luego se eliminan mediante un proceso llamado empalme de ARN para formar el ARN mensajero maduro. Muchos intrones parecen ser elementos genéticos móviles (partes del ADN que pueden moverse).
Algunos intrones, como los del grupo I en el protozoo Tetrahymena, parecen ser elementos genéticos "egoístas" que no afectan al organismo, ya que se eliminan de las partes que sí codifican (exones) durante el procesamiento del ARN. Sin embargo, otros intrones tienen funciones biológicas importantes, quizás actuando como ribozimas (moléculas de ARN con actividad enzimática) que regulan la actividad del ARNt y el ARNr, así como la expresión de genes que codifican proteínas. Por ejemplo, el intrón trnL se encuentra en todas las plantas verdes y se ha mantenido durante miles de millones de años. Archivo:Pre-mRNA to mRNA.svg
Pseudogenes
Los pseudogenes son secuencias de ADN parecidas a Genes conocidos, pero que han perdido su capacidad de dar instrucciones para crear proteínas o ya no se usan en la célula. Los pseudogenes pueden surgir de la copia inversa de ARN o de la duplicación de genes funcionales. Se convierten en "fósiles genómicos" que no funcionan debido a mutaciones que impiden su copia o que alteran fatalmente la forma en que se leen sus instrucciones.
Aunque se pensaba que los pseudogenes no podían recuperar su función, algunos pueden seguir funcionando durante millones de años e incluso "reactivarse" para codificar proteínas. Como se cree que los pseudogenes cambian sin la presión de la evolución, pueden ser útiles para estudiar los tipos y la frecuencia de las mutaciones genéticas espontáneas.
Secuencias repetidas, transposones y elementos virales
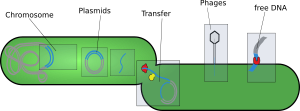
Los transposones y retrotransposones son elementos genéticos móviles que pueden cambiar de lugar en el genoma. Las secuencias repetidas de retrotransposones, como los elementos nucleares intercalados largos (LINE) y cortos (SINE), forman una gran parte de los genomas de muchas especies. Las secuencias Alu, un tipo de SINE, son los elementos móviles más abundantes en el genoma humano. Se ha descubierto que algunos SINEs controlan la copia de ciertos genes que codifican proteínas.
Las secuencias de retrovirus endógenos son el resultado de la copia inversa de genomas de retrovirus en el ADN de las células reproductivas. Las mutaciones en estas secuencias pueden inactivar el genoma viral.
Más del 8% del genoma humano está formado por secuencias de retrovirus endógenos (la mayoría ya no funcionan), y más del 42% proviene de retrotransposones. Otro 3% son restos de transposones de ADN. Se cree que gran parte de la mitad restante del genoma, cuyo origen aún no se explica, proviene de elementos transponibles que estuvieron activos hace mucho tiempo (más de 200 millones de años) y que las mutaciones los han hecho irreconocibles. La variación en el tamaño del genoma en al menos dos tipos de plantas se debe principalmente a las secuencias de retrotransposones.
Telómeros
Los telómeros son regiones de ADN repetitivo que se encuentran al final de un cromosoma. Su función es proteger el cromosoma del desgaste durante la copia del ADN. Estudios recientes han demostrado que los telómeros ayudan a mantener su propia estabilidad. El ARN que contiene repeticiones teloméricas (TERRA) son copias de los telómeros. Se ha demostrado que TERRA mantiene la actividad de la telomerasa (una enzima) y alarga los extremos de los cromosomas.
El término "ADN basura"
El término "ADN basura" se hizo popular en la década de 1960. Fue usado por primera vez en 1972 por el biólogo David Comings para referirse a todo el ADN no codificante. Ese mismo año, Susumu Ohno formalizó el término, sugiriendo que los genomas de mamíferos no podían tener demasiados genes funcionales debido al "costo" de las mutaciones dañinas. Ohno predijo que los genomas de mamíferos no podrían tener más de 30,000 genes bajo selección, lo cual es consistente con los aproximadamente 20,000 genes del genoma humano.
Otra razón para la teoría de Ohno fue la observación de que especies muy parecidas podían tener genomas de tamaños muy diferentes, lo que se llamó la paradoja del valor C en 1971. Aunque la utilidad del término "ADN basura" ha sido cuestionada porque "sugiere fuertemente que no tiene ninguna función", y se ha recomendado usar un término más neutral como "ADN no codificante", la expresión "ADN basura" todavía se usa para referirse a las partes del genoma para las que no se ha encontrado una función clara.
Desde finales de los años 70, se ha visto que la mayoría del ADN no codificante en genomas grandes proviene de la amplificación de elementos transponibles (partes del ADN que se copian a sí mismas). En 1980, W. Ford Doolittle y Carmen Sapienza escribieron en la revista Nature que si un ADN sin función conocida ha desarrollado una estrategia para asegurar su supervivencia (como la transposición), no se necesita otra explicación para su existencia.
La cantidad de ADN basura dependería de la velocidad a la que estos elementos se copian y la velocidad a la que se pierde el ADN no funcional. En el mismo número de Nature, Leslie Orgel y Francis Crick escribieron que el ADN basura tiene "poca especificidad y no da ninguna ventaja selectiva al organismo". El término se usa principalmente en la ciencia popular y de forma coloquial en publicaciones científicas. Se ha sugerido que sus connotaciones podrían haber retrasado el interés en las funciones biológicas del ADN no codificante. Varias pruebas indican que algunas secuencias de "ADN basura" probablemente tienen una actividad funcional no identificada y que el proceso de exaptación (cuando algo que no tenía una función específica adquiere una nueva) de fragmentos de ADN originalmente egoísta o no funcional ha sido común a lo largo de la evolución.
Proyecto ENCODE
En 2012, el proyecto ENCODE, un programa de investigación apoyado por el Instituto Nacional de Investigación del Genoma Humano, informó que el 76% de las secuencias de ADN no codificantes del genoma humano se copiaban y que casi la mitad del genoma era accesible a proteínas que regulan los genes, como los factores de transcripción. Sin embargo, la sugerencia de ENCODE de que más del 80% del genoma humano es bioquímicamente funcional ha sido criticada por otros científicos. Ellos argumentan que ni la accesibilidad de los segmentos del genoma a los factores de transcripción ni su copia garantizan que esos segmentos tengan una función bioquímica o que sean ventajosos para la supervivencia.
Además, las estimaciones de funcionalidad antes de ENCODE se basaban en la conservación del genoma en los mamíferos. En respuesta, otros científicos argumentan que la copia y el empalme generalizados que se observan directamente en el genoma humano mediante pruebas bioquímicas son un indicador más preciso de la función genética que la conservación del genoma. Las estimaciones de conservación pueden dar pistas para identificar posibles elementos funcionales, pero no limitan la cantidad total de elementos funcionales que podrían existir en el genoma. Además, gran parte del ADN que parece "basura" está involucrado en la regulación epigenética y parece ser necesario para el desarrollo de organismos complejos.
En un artículo de 2014, los investigadores de ENCODE intentaron responder a la pregunta de si las regiones no conservadas pero bioquímicamente activas son realmente funcionales. Señalaron que en la literatura, las partes funcionales del genoma se han identificado de diferentes maneras en estudios anteriores, dependiendo de los métodos utilizados. Se han usado tres enfoques principales para identificar partes funcionales del genoma humano:
- Enfoques genéticos: Se basan en cambios en las características físicas del organismo. Pueden pasar por alto elementos funcionales que no se manifiestan físicamente.
- Enfoques evolutivos: Se basan en la conservación de las secuencias a lo largo del tiempo. Tienen dificultades para alinear con precisión secuencias de múltiples especies, ya que los genomas de especies incluso muy parecidas varían considerablemente.
- Enfoques bioquímicos: Se basan en pruebas bioquímicas y fueron usados por ENCODE. Aunque tienen alta reproducibilidad, las señales bioquímicas no siempre significan automáticamente una función.
Los investigadores de ENCODE señalaron que el 70% de la copia del ADN era muy baja (menos de 1 copia por célula). Dijeron que esta "mayor proporción del genoma con una señal bioquímica reproducible pero baja y menor conservación evolutiva es difícil de analizar entre funciones específicas y ruido biológico". Además, la resolución de las pruebas a menudo es mucho más amplia que los sitios funcionales reales, por lo que es poco probable que algunas de las secuencias "bioquímicamente activas pero selectivamente neutrales" cumplan funciones críticas, especialmente aquellas con un nivel bajo de señal bioquímica.
A esto añadieron: "Sin embargo, también reconocemos limitaciones importantes en nuestra detección actual de restricciones, dado que algunas funciones específicas de humanos son esenciales pero no conservadas y que las regiones relevantes para enfermedades no necesitan estar restringidas selectivamente para ser funcionales". Por otro lado, argumentaron que la fracción del 12-15% del ADN humano bajo restricción funcional, según lo estimado por varios métodos evolutivos, aún podría ser una subestimación. Concluyeron que los datos bioquímicos ofrecen pistas sobre la función molecular de los elementos de ADN y los tipos de células en los que actúan. En última instancia, los enfoques genéticos, evolutivos y bioquímicos pueden usarse juntos para identificar regiones que pueden ser funcionales en la biología humana y en las enfermedades.
Algunos críticos han argumentado que la funcionalidad solo puede evaluarse en comparación con una hipótesis nula adecuada. En este caso, la hipótesis nula sería que estas partes del genoma no son funcionales y tienen propiedades que se esperarían de dichas regiones basándose en nuestra comprensión general de la evolución molecular y la bioquímica. Según estos críticos, hasta que se demuestre que una región en cuestión tiene características adicionales, más allá de lo que se espera de la hipótesis nula, debe etiquetarse provisionalmente como no funcional.
Evidencia de funcionalidad
Muchas secuencias de ADN no codificantes deben tener alguna función biológica importante. Esto se ve en estudios de genómica comparativa que muestran regiones de ADN no codificante altamente conservadas, a veces durante cientos de millones de años. Esto implica que estas regiones no codificantes están bajo una fuerte presión evolutiva y selección positiva. Por ejemplo, en los genomas de humanos y ratones, que se separaron de un ancestro común hace 65-75 millones de años, las secuencias de ADN que codifican proteínas representan solo alrededor del 20% del ADN conservado, mientras que el 80% restante del ADN conservado se encuentra en regiones no codificantes.
El mapeo de enlaces a menudo identifica regiones cromosómicas asociadas con una enfermedad sin evidencia de variantes de genes funcionales dentro de la región, lo que sugiere que las variantes genéticas que causan la enfermedad se encuentran en el ADN no codificante. La importancia de las mutaciones de ADN no codificantes en el cáncer se investigó en abril de 2013.
Los cambios genéticos no codificantes (polimorfismos) influyen en la susceptibilidad a enfermedades infecciosas, como la hepatitis C. Además, estos polimorfismos contribuyen a la susceptibilidad al sarcoma de Ewing, un tipo agresivo de cáncer de huesos en niños.
Algunas secuencias específicas de ADN no codificante pueden ser características esenciales para la estructura de los cromosomas, la función del centrómero y el reconocimiento de cromosomas homólogos durante la meiosis (división celular para formar células reproductivas).
Según un estudio comparativo de más de 300 genomas procariotas y más de 30 eucariotas, los eucariotas parecen necesitar una cantidad mínima de ADN no codificante. La cantidad se puede predecir usando un modelo de crecimiento para redes genéticas reguladoras, lo que implica que es necesario para fines de regulación. En humanos, el mínimo previsto es aproximadamente el 5% del genoma total.
Más del 10% de los 32 genomas de mamíferos pueden funcionar formando estructuras secundarias específicas del ARN. El estudio utilizó genómica comparativa para identificar mutaciones compensatorias del ADN que mantienen los pares de bases del ARN, una característica distintiva de las moléculas de ARN. Más del 80% de las regiones genómicas que muestran evidencia evolutiva de la conservación de la estructura del ARN no muestran una fuerte conservación de la secuencia de ADN.
El ADN no codificante separa los genes entre sí con espacios largos. Esto ayuda a que una mutación en un gen o parte de un cromosoma, como una eliminación o inserción, no afecte a todo el cromosoma. Cuando la complejidad del genoma es relativamente alta, como en el genoma humano, no solo entre diferentes genes, sino también dentro de muchos genes, hay espacios de intrones para proteger todo el segmento que codifica y minimizar los cambios causados por la mutación. El ADN no codificante quizás sirva para disminuir la probabilidad de que los genes se dañen durante el cruce cromosómico.
Regulación de la expresión génica
Algunas secuencias de ADN no codificantes determinan los niveles de uso de varios genes, tanto los que se copian para hacer proteínas como los que participan en la regulación de los genes.
Factores de transcripción
Algunas secuencias de ADN no codificantes determinan dónde se unen los factores de transcripción. Un factor de transcripción es una proteína que se une a secuencias específicas de ADN no codificantes, controlando así el flujo (o copia) de información genética del ADN al ARN mensajero.
Operadores
Un operador es un segmento de ADN al que se une una proteína llamada represor. Un represor es una proteína que se une al ADN y regula el uso de uno o más genes al unirse al operador y bloquear la unión de la ARN polimerasa al promotor, impidiendo así que los genes se copien. Este bloqueo se llama represión.
Potenciadores
Un potenciador es una región corta de ADN a la que pueden unirse proteínas (llamadas factores de acción trans), al igual que un conjunto de factores de transcripción, para aumentar los niveles de copia de genes en un grupo de genes.
Silenciadores
Un silenciador es una región de ADN que desactiva el uso de un gen cuando se une a una proteína reguladora. Funciona de manera muy similar a los potenciadores, pero su efecto es el de desactivar genes.
Promotores
Un promotor es una región de ADN que facilita la copia de un gen particular cuando un factor de transcripción se une a él. Los promotores generalmente se encuentran cerca de los genes que regulan y antes de ellos.
Aisladores
Un aislante genético es un elemento límite que tiene dos funciones distintas en el uso de los genes: puede bloquear la acción de un potenciador o, rara vez, actuar como una barrera contra el ADN muy compactado. Un aislante en una secuencia de ADN es como una coma en una oración, porque indica dónde termina una secuencia que ha sido potenciada o reprimida.
Usos
Evolución
Las secuencias compartidas de ADN que aparentemente no tienen función son una importante evidencia de que los seres vivos tienen un ancestro común.
Las secuencias de pseudogenes parecen acumular mutaciones más rápidamente que las secuencias que codifican, debido a la pérdida de presión de la selección natural. Esto permite la creación de variantes mutantes que pueden adquirir nuevas funciones y ser favorecidas por la selección natural. Así, los pseudogenes pueden servir como "materia prima" para la evolución y pueden considerarse "protogenes".
Correlaciones de largo alcance
Se ha encontrado una diferencia estadística entre las secuencias de ADN que codifican y las que no. Se ha observado que los nucleótidos en secuencias de ADN no codificantes muestran correlaciones de largo alcance, mientras que las secuencias codificantes no lo hacen.
Antropología Forense
La policía a veces recoge ADN como prueba para fines de identificación forense. Como se describe en Maryland v. King, una decisión de la Corte Suprema de EE. UU. de 2013:
El método actual para las pruebas forenses de ADN se basa en un análisis de los cromosomas que se encuentran en el núcleo de todas las células humanas. El material de ADN en los cromosomas está compuesto por regiones "codificantes" y "no codificantes". Las regiones codificantes se conocen como genes y contienen la información necesaria para que una célula produzca proteínas... las regiones no codificantes de proteínas... no están directamente relacionadas con la producción de proteínas, [y] se han llamado ADN "basura". El adjetivo "basura" puede confundir a la gente, ya que de hecho esta es la región del ADN que se usa con casi total seguridad para identificar a una persona.
Véase también
 En inglés: Non-coding DNA Facts for Kids
En inglés: Non-coding DNA Facts for Kids

