Clorato de amonio para niños
Datos para niños
Clorato de amonio |
||
|---|---|---|
 |
||
 |
||
| Nombre IUPAC | ||
| Clorato de amonio | ||
| General | ||
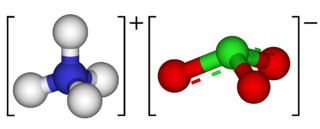
| Fórmula estructural | NH4ClO3 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 10192-29-7 | |
| ChemSpider | 55411 | |
| PubChem | 11679808 61491, 11679808 | |
|
InChI
InChI=InChI=1S/ClHO3.H3N/c2-1(3)4;/h(H,2,3,4);1H3
Key: KHPLPBHMTCTCHA-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Densidad | 2,42 kg/m³; 2420 g/cm³ | |
| Masa molar | 101,49 g/mol | |
| Punto de fusión | 653 K (380 °C) | |
| Estructura cristalina | sistema rómbico | |
| Termoquímica | ||
| ΔfH0sólido | 62,7 kcal/mol kJ/mol | |
| Compuestos relacionados | ||
| Otros aniones | perclorato de amonio cloruro de amonio bromato de amonio |
|
| Otros cationes | Clorato de bario Clorato de potasio Clorato de sodio |
|
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El clorato de amonio es un compuesto inorgánico con la fórmula química NH4ClO3. Es una sustancia muy inestable y se utiliza en la fabricación de ciertos materiales.
Contenido
¿Qué es el Clorato de Amonio?
El clorato de amonio es un compuesto químico que no se encuentra en la naturaleza. Se forma a partir de elementos como el nitrógeno, el hidrógeno, el cloro y el oxígeno. Su fórmula, NH4ClO3, nos dice cuántos átomos de cada elemento tiene. Es conocido por ser muy inestable, lo que significa que puede reaccionar de forma inesperada.
¿Cómo se obtiene el Clorato de Amonio?
Existen varias maneras de crear clorato de amonio en un laboratorio. Una forma es mezclando ácido clórico con amoníaco o con carbonato de amonio. Esta reacción se llama neutralización.
- Método 1: Reacción de neutralización
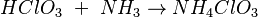
Otro método consiste en combinar ciertas sustancias que contienen clorato, como el clorato de bario, el clorato de estroncio o el clorato de calcio, con carbonato de amonio o sulfato de amonio. Al hacer esto, se forma un sólido que se separa (llamado precipitado) y queda una solución de clorato de amonio. Este clorato de amonio se puede obtener en forma de pequeños cristales que se disuelven fácilmente en agua.
- Método 2: Reacción de precipitación
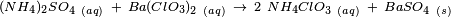
Propiedades y precauciones del Clorato de Amonio
El clorato de amonio tiene propiedades muy particulares que lo hacen peligroso si no se maneja con cuidado.
¿Cómo reacciona el Clorato de Amonio al calor?
Cuando se calienta, el clorato de amonio se descompone a una temperatura de aproximadamente 102 grados Celsius. Al descomponerse, libera gases como nitrógeno, cloro y oxígeno.
¿Es soluble en otros líquidos?
Este compuesto se disuelve bien en agua con un poco de alcohol. Sin embargo, no se disuelve en alcohol concentrado.
¿Por qué es tan inestable y peligroso?
El clorato de amonio es un oxidante muy fuerte. Esto significa que puede causar o acelerar la combustión de otros materiales. Es tan inestable que puede descomponerse de forma repentina, incluso a temperatura ambiente. Si se expone a la luz del sol por unos minutos o recibe un golpe, puede reaccionar de forma explosiva. Incluso sus soluciones líquidas son inestables.
Debido a su naturaleza peligrosa, esta sustancia solo debe mantenerse en solución cuando sea absolutamente necesario. Nunca debe permitirse que se formen cristales sólidos. Por su alto riesgo, el transporte de clorato de amonio está prohibido por las autoridades de transporte en algunos países, como en Estados Unidos.
Véase también
 En inglés: Ammonium chlorate Facts for Kids
En inglés: Ammonium chlorate Facts for Kids

