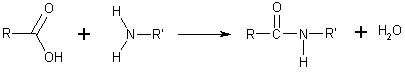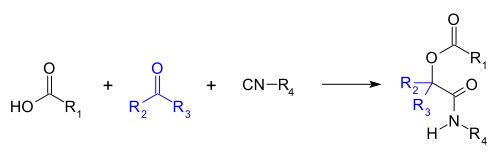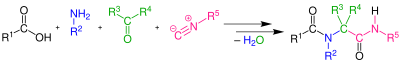Amida para niños
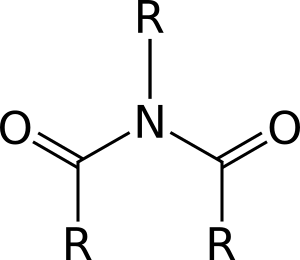
Una amida es un compuesto que se forma conceptual o químicamente por el reemplazo del hidroxilo de un oxácido por un sustituyente amino. En química orgánica, se le denomina por antonomasia como "amida" a las amidas de los ácidos carboxílicos (estrictamente, carboxamida). Se puede considerar como un derivado de un ácido carboxílico por sustitución del grupo —OH del ácido por un grupo —NH2, —NHR o —NRR' (llamado grupo amino). Por esto su grupo funcional es del tipo RCONR'R'', siendo CO un carbonilo, N un átomo de nitrógeno, y R, R' y R'' radicales orgánicos o átomos de hidrógeno:
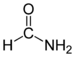
| Formamida (amida del ácido fórmico) |
Amida (carboxamida) (amida de ácido carboxílico) |
Urea o carbamida (amida del ácido carbónico) |
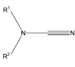
Cianimida (amida del ácido ciánico) |
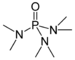
Hexametilfosforamida (amida hexametilada del ácido fosfórico) |
Sulfamida (amida de ácido sulfúrico) |
Nitramida (amida de ácido nítrico) |
|---|---|---|---|---|---|---|
 |
 |
 |
 |
Cuando el grupo amida no es el principal, se nombra usando el prefijo carbamoil:
CH3-CH2-CH(CONH2)-CH2-CH2-COOH → ácido 4-carbamoilhexanoico.
Todas las amidas, excepto la primera de la serie, son sólidas a temperatura ambiente y sus puntos de ebullición son elevados, más altos que los de los ácidos correspondientes. Presentan excelentes propiedades disolventes y son bases muy débiles. Uno de los principales métodos de obtención de estos compuestos consiste en hacer reaccionar el amoníaco (o aminas primarias o secundarias) con ésteres. Las amidas son comunes en la naturaleza, y una de las más conocidas es la urea, una diamida que no contiene hidrocarburos. Las proteínas y los péptidos están formados por amidas. Un ejemplo de poliamida de cadena larga es el nailon. Las amidas también se utilizan mucho en la industria farmacéutica.
Contenido
Poliamidas
La amida del ácido carbónico es denominada urea y sus derivados son el grupo funcional ureido.
Las diacilaminas son denominadas como grupo funcional imida y son análogas a los anhídridos carboxílicos, por ejemplo el carb0xili0
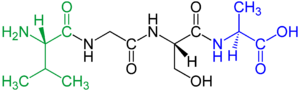
Las poliamidas son compuestos que contienen grupos amida. Algunos son sintéticas, como el nailon, pero también se encuentran en la naturaleza, en las proteínas, formadas a partir de los aminoácidos, por reacción de un grupo carboxilo de un aminoácido con un grupo amino de otro. En las proteínas al grupo amida se le llama enlace peptídico.
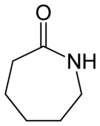
El nailon es una poliamida debido a los característicos grupos amida en la cadena principal de su formulación. Por ejemplo, el nailon 6 se obtiene por polimerización de la ε-caprolactama.
Ciertas poliamidas del tipo nailon son la poliamida-6, la poliamida-11, la poliamida-12, la poliamida-9,6, la poliamida-6,9, la poliamida-6,10 y la poliamida-6,12. Se pueden citar como ejemplo de poliamidas no lineales los productos de condensación de ácidos dimerizados de aceites vegetales con aminas.
Los péptidos, incluyendo las proteínas como la seda, a la que el nailon reemplazó, también son poliamidas. Estos grupos amida son muy polares y pueden unirse entre sí mediante enlaces por puente de hidrógeno. Debido a esto y a que la cadena del nailon es tan regular y simétrica, los nailones son a menudo cristalinos, y forman excelentes fibras.
Síntesis de amidas
La síntesis de amidas se puede llevar a cabo por diversos métodos. El método más simple es la condensación de un ácido carboxílico con una amina. Esta reacción es termodinámicamente favorable en general, pero tiene una elevada energía de activación, debido principalmente a la primera desprotonación del ácido carboxílico y la protonación de la amina, lo cual forma un producto estable, el carboxilato de aminio. Esto reduce la reactividad. Además, se requieren altas temperaturas.
- RCO2H + R′R″NH
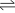 RCO−
RCO−
2 + R′R″NH+
2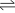 RC(O)NR′R″ + H2O
RC(O)NR′R″ + H2O
Se conocen muchos métodos para conducir el equilibrio hacia la derecha. En su mayor parte, estas reacciones implican "activar" el ácido carboxílico convirtiéndolo primero en un mejor electrófilo; tales como ésteres, cloruros de ácido (reacción de Schotten-Baumann) o anhídridos (método de Lumière-Barbier). Los métodos convencionales en la síntesis de péptidos usan agentes de acoplamiento tales como HATU, hidroxibenzotiazol (HOBt) o PyBOP. Recientemente, han surgido reactivos novedosos a base de boro para la formación del enlace CO-N, incluyendo el uso de catalizadores de ácido 2-yodofenilborónico, MIBA y borato de tris(2,2,2-trifluoroetilo).
| Nombre de la reacción | Sustrato | Detalles |
|---|---|---|
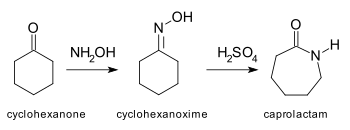
| Transposición de Beckmann | Cetona cíclica | Reactivo: hidroxilamina en medio ácido. Se forma una lactama.
|
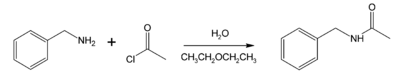
| Reacción de Schotten-Baumann | Halogenuro de acilo | Reactivo: amina con un halogenuro de acilo en medio básico |
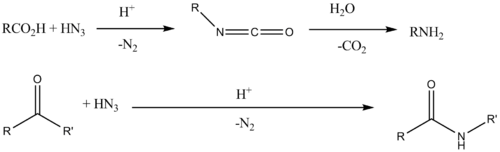
| Reacción de Schmidt | Cetonas | Reactivo: Ácido hidrazoico |
| Hidrólisis de nitrilos | Nitrilo | Reactivo: Agua en medio ácido
|
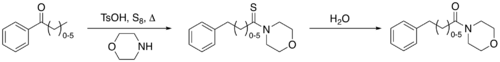
| Reacción de Willgerodt–Kindler | Aril alquil cetonas | Azufre y morfolina |
| Reacción de Passerini | Ácido carboxílico, cetona o aldehído | Reacción de tres componentes entre un ácido carboxílico, un compuesto carbonílico, como una cetona o un aldehído, y un isocianuro, para formar α-hidroxicarboxamidas.
|
| Reacción de Ugi | Isocianuro, ácido carboxílico, cetona, amina primaria | Condensación de cuatro componentes entre un aldehído, una amina, un ácido carboxílico y un isocianuro para preparar derivados de α-aminoacil amidas. |
| Reacción de Bodroux | Ácido carboxílico, reactivo de Grignard con un derivado de anilina ArNHR′ | 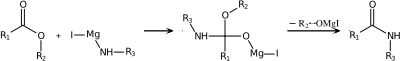 |
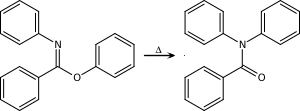
| Transposición de Chapman | Arilo, imino éter | Para N,N-diaril amidas. El mecanismo de reacción está basado en una sustitución nucleofílica aromática. |
| Síntesis de amidas de Leuckart | Isocianato | Reacción de un areno con un isocianato catalizado por cloruro de aluminio. Se forma una benzamida. |
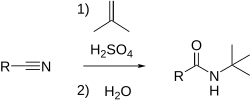
| Reacción de Ritter | Alquenos, alcoholes, o cualquier otra fuente de carbocatiónes | Amidas con el nitrógeno enlazado a un carbono terciario por medio de una reacción de adición entre un nitrilo y un carbocatión terciario en presencia de ácidos concentrados. |
| Adición fotolítica de una formamida a olefinas | Alquenos terminales | Reacción de homologación radicalaria entre un alqueno termina y formamida. |
| Aminólisis de ésteres | Ésteres | Reacción de aminólisis ácida de ésteres. |
Reacciones de amidas
Las principales reacciones de las amidas son:
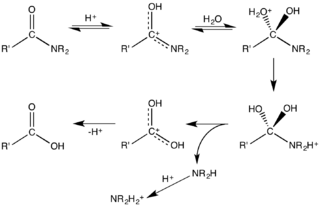
- Hidrólisis ácida o básica: La amida se hidroliza en medio básico formando un carboxilato de metal o en medio ácido formando un ácido carboxílico.
- Deshidratación: En presencia de un deshidratante como cloruro de tionilo o pentóxido de fósforo se produce un nitrilo.
- Reducción: Las amidas pueden reducirse con hidruro de litio y aluminio a aminas.
- Transposición de Hofmann: En presencia de un halógeno en medio básico se produce una compleja reacción que permite la obtención de una amina con un carbono menos en su cadena principal.
Ejemplo de amida
- La acrilamida se emplea en distintas aplicaciones, aunque es más conocida por ser probablemente carcinógena y estar presente en bastantes alimentos al formarse por procesos naturales al cocinarlos.
- Son fuente de energía para el cuerpo humano.
- Pueden ser vitaminas en el cuerpo o analgésicos.
Importancia y usos
Las amidas son comunes en la naturaleza y se encuentran en sustancias como los aminoácidos, las proteínas, el ADN y el ARN, hormonas y vitaminas.
La urea es utilizada para la excreción del amoníaco (NH3) en el ser humano y mamíferos. También es muy utilizada en la industria farmacéutica y en la industria del nailon.
Véase también
 En inglés: Amide Facts for Kids
En inglés: Amide Facts for Kids