Cloruro de aluminio para niños
Datos para niños
Cloruro de aluminio |
||
|---|---|---|
 |
||
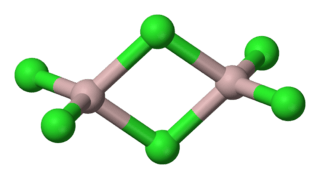 Dimero tricloruro de aluminio
|
||
| Nombre IUPAC | ||
| Cloruro de aluminio | ||
| General | ||
| Otros nombres | Cloruro de aluminio (III) | |
| Fórmula estructural | ||
| Fórmula molecular | AlCl3 | |
| Identificadores | ||
| Número CAS | 7446-70-0 | |
| Número RTECS | BD0530000 | |
| ChEBI | 30114 | |
| ChemSpider | 22445 | |
| DrugBank | DB11081 | |
| PubChem | 24012 | |
| UNII | LIF1N9568Y | |
|
Cl[Al](Cl)Cl
|
||
|
InChI
InChI=1S/Al.3ClH/h;3*1H/q+3;;;/p-3
Key: VSCWAEJMTAWNJL-UHFFFAOYSA-K |
||
| Propiedades físicas | ||
| Apariencia | sólido blanco o amarillo pálido, higroscópico | |
| Densidad | 2,48 kg/m³; 0,00248 g/cm³ | |
| Masa molar | 133,34 g/mol | |
| Punto de fusión | 192,4 °C (466 K) | |
| Punto de ebullición | 120 °C (393 K) | |
| Estructura cristalina | sistema cristalino monoclínico | |
| Riesgos | ||
| LD50 | anhidro: 380 mg/kg, rat (oral) hexahydrate: 3311 mg/kg, rat (oral) |
|
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El cloruro de aluminio (AlCl3) es un compuesto formado por aluminio y cloro. Es un sólido que se ve blanco o amarillo pálido.
Este compuesto tiene una característica especial: aunque está hecho de un metal (aluminio) y un no metal (cloro), sus átomos se unen compartiendo electrones. Esto se conoce como enlace covalente.
Contenido
¿Cuáles son las propiedades del Cloruro de Aluminio?
El cloruro de aluminio tiene un punto de fusión y un punto de ebullición bajos. Esto significa que se derrite y se convierte en gas a temperaturas relativamente bajas.
Se convierte directamente de sólido a gas (un proceso llamado sublimación) a 178° C. Cuando está derretido, no conduce bien la electricidad. Esto es diferente de otros compuestos similares, como la sal de mesa (cloruro de sodio), que sí conducen electricidad cuando están fundidos.
¿Cómo reacciona el Cloruro de Aluminio?
El cloruro de aluminio es un compuesto muy interesante porque puede actuar como un ácido o como una base. A las sustancias que tienen esta doble capacidad se les llama anfóteras.
Cloruro de Aluminio en el agua
Cuando el cloruro de aluminio se mezcla con agua destilada, se separa en pequeñas partículas llamadas iones. Estas partículas son iones de aluminio (Al3+) y iones de cloro (Cl-).
Luego, el ion de aluminio reacciona con el agua. Se une a partes del agua y libera otras partículas llamadas protones. Como resultado, se forma hidróxido de aluminio.
Si a esta mezcla se le añade hidróxido de sodio, el ion de aluminio reaccionará con los iones de hidróxido presentes.
Véase también
 En inglés: Aluminium chloride Facts for Kids
En inglés: Aluminium chloride Facts for Kids

