Estibano para niños
El estibano, también conocido como trihidruro de antimonio, es un compuesto químico formado por antimonio (Sb) e hidrógeno (H), con la fórmula SbH3. A temperatura y presión normales, es un gas que no tiene color. Es el principal hidruro de antimonio y se parece mucho al amoniaco (NH3), aunque es más pesado.
Las moléculas de estibano tienen una forma de pirámide triangular. Sus ángulos H–Sb–H son de 91.7 grados y la distancia entre el antimonio y el hidrógeno es de 1.707 Å. Al igual que el sulfuro de hidrógeno (H2S), este gas tiene un olor fuerte y desagradable, similar al de los huevos podridos.
Datos para niños
Estibano |
||
|---|---|---|
 |
||
 |
||
| Nombre IUPAC | ||
| Trihidruro de antimonio Estibano |
||
| General | ||
| Fórmula semidesarrollada | SbH3 | |
| Fórmula estructural | 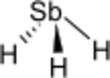 |
|
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 7803-52-3 | |
| ChEBI | 30288 | |
| ChemSpider | 8992 | |
| PubChem | 9359 | |
|
InChI
InChI=InChI=1S/Sb.3H
Key: OUULRIDHGPHMNQ-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Apariencia | Gas incoloro | |
| Densidad | 548 kg/m³; 0,548 g/cm³ | |
| Masa molar | 124,784 g/mol | |
| Punto de fusión | 184,65 K (−89 °C) | |
| Punto de ebullición | 256,15 K (−17 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | Insoluble | |
| Peligrosidad | ||
| NFPA 704 |
4
4
2
|
|
| Riesgos | ||
| Ingestión | Extremadamente mortal. | |
| Inhalación | Altamente tóxico. Olor muy desagradable, parecido al de un huevo podrido. | |
| Piel | El contacto debería ser evitado. | |
| Ojos | El contacto debería ser evitado. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
Contenido
¿Cómo se obtiene el estibano?
El estibano (SbH3) se suele crear combinando compuestos de antimonio con otros elementos. Por ejemplo, se puede obtener a partir de óxido de antimonio y un compuesto llamado hidruro de litio y aluminio. También se puede formar a partir de cloruro de antimonio y borohidruro de sodio.
Otra forma de producir estibano es haciendo reaccionar ciertos compuestos de antimonio con ácidos, incluso con agua. Sin embargo, el estibano que se forma de esta manera es inestable.
Propiedades del estibano
Las características químicas del estibano son parecidas a las de la arsina (AsH3). Al igual que otros hidruros pesados, el estibano no es muy estable y tiende a descomponerse en sus elementos originales.
Este gas se descompone lentamente a temperatura ambiente. Pero si se calienta a unos 200 °C, se descompone muy rápido. Esta descomposición puede acelerarse por sí misma y, en algunos casos, ser muy enérgica.
El estibano reacciona fácilmente con el oxígeno del aire. Cuando esto sucede, se transforma en óxido de antimonio y agua.
Al igual que el amoniaco, el estibano puede actuar como una base débil. Esto significa que puede donar un par de electrones a otros compuestos. También puede donar protones (partículas con carga positiva) en ciertas reacciones químicas.
Usos del estibano
El estibano se utiliza en la fabricación de semiconductores. Los semiconductores son materiales que conducen la electricidad de forma especial y son clave en los aparatos electrónicos. El estibano se usa para añadir pequeñas cantidades de antimonio a estos materiales, un proceso llamado "dopaje". Esto se hace mediante una técnica conocida como deposición química de vapor (CVD).
También se ha considerado su uso como un agente para controlar plagas, similar a la fosfina (PH3). Sin embargo, no se usa mucho para esto porque es inestable y difícil de producir.
Historia del descubrimiento
Debido a que el estibano (SbH3) y la arsina (AsH3) son muy parecidos, el estibano se puede detectar con una prueba especial llamada la Prueba de Marsh. Esta prueba, creada por James Marsh alrededor de 1836, sirve para encontrar arsina, que se forma en presencia de arsénico.
El proceso funciona así: se toma una muestra con zinc y ácido sulfúrico diluido. Si hay arsénico en la muestra, se libera arsina en forma de gas. Este gas se calienta en un tubo de vidrio, lo que hace que se descomponga. Si aparece un depósito oscuro en la parte fría del tubo, indica que hay antimonio.
El estibano fue descubierto de forma independiente en 1837 por Lewis Thomson y la compañía alemana Pfaff. Al principio, fue difícil estudiar sus propiedades porque no se sabía cómo producirlo de forma confiable. En 1876, Francis Jones intentó varios métodos para crearlo. Finalmente, en 1901, Alfred Stock logró determinar la mayoría de las propiedades de este compuesto.
Precauciones con el estibano
El estibano es un gas que puede encenderse fácilmente y es muy peligroso. Por suerte, como es inestable, casi no se encuentra de forma natural en el aire.
Si una persona entra en contacto con estibano, puede sentir dolor de cabeza, mareos y náuseas. También puede afectar los glóbulos rojos del cuerpo, lo que puede causar problemas de salud. Por estas razones, es muy importante manejar el estibano con extremo cuidado y solo bajo supervisión de expertos.
Galería de imágenes
Véase también
 En inglés: Stibine Facts for Kids
En inglés: Stibine Facts for Kids