Cero absoluto para niños
El cero absoluto es la temperatura más baja que se puede alcanzar. A esta temperatura, la energía de las partículas de un material es la más pequeña posible. Esto significa que las moléculas y átomos apenas se mueven.
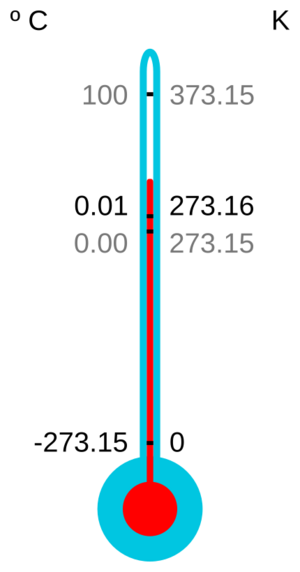
El cero absoluto es el punto de partida para la escala de Kelvin (0 K) y la escala de Rankine (0 R). Por acuerdo internacional, 0 K equivale a aproximadamente −273.15 °C (grados Celsius) o −459.67 °F (grados Fahrenheit).
Según las leyes de la termodinámica, es imposible alcanzar el cero absoluto de forma perfecta. Sin embargo, los científicos han logrado acercarse mucho. Por ejemplo, en 2014, en Italia, se enfrió un recipiente de cobre a 0.006 K (−273.144 °C) durante 15 días. En 2015, científicos del Instituto Tecnológico de Massachusetts enfriaron un gas a 500 nK (0.0000005 K) por encima del cero absoluto, ¡un récord!
A 0 K, todas las sustancias conocidas se volverían sólidas, y sus moléculas perderían casi toda su capacidad de moverse o vibrar.
Contenido
¿Qué sucede cerca del cero absoluto?
Cuando la temperatura se acerca mucho al cero absoluto, algunos materiales muestran comportamientos muy especiales y sorprendentes.
Condensado de Bose-Einstein
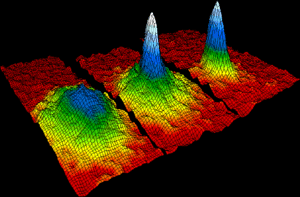
En 1924, los científicos Albert Einstein y Satyendranath Bose predijeron un estado de la materia llamado condensado de Bose-Einstein. En este estado, un grupo de partículas llamadas bosones se comportan como una sola "superpartícula". Este fenómeno se confirmó en 1995 y ha sido muy estudiado desde entonces.
Superfluidos
A temperaturas muy bajas, algunos líquidos, como el helio, pueden convertirse en "superfluidos". Esto significa que fluyen sin ninguna fricción, como si no tuvieran viscosidad. También pueden subir por las paredes de un recipiente.
Aplicaciones en la ciencia
Una aplicación práctica de las temperaturas cercanas al cero absoluto se encuentra en el acelerador de partículas LHC del CERN. Este gran colisionador de partículas alcanza una temperatura de 1.9 K. Para que funcione, algunos de sus circuitos deben estar extremadamente fríos para convertirse en "superconductores", lo que permite que la electricidad fluya sin resistencia. Esto se logra usando helio y nitrógeno líquido para enfriar los circuitos.
Temperaturas negativas en escalas comunes
Las temperaturas que vemos como números negativos en las escalas Celsius o Fahrenheit (como -10 °C) simplemente significan que son más frías que el punto de congelación del agua (0 °C).
Existen algunos sistemas especiales que pueden alcanzar lo que se llama "temperaturas verdaderamente negativas" en la escala Kelvin. Aunque suene extraño, un sistema con una temperatura "negativa" en Kelvin no es más frío que el cero absoluto. De hecho, es más "caliente" que cualquier sistema con temperatura positiva en Kelvin, en el sentido de que si se juntan, el calor fluirá del sistema "negativo" al "positivo". Este es un concepto muy avanzado de la física.
Historia del cero absoluto
La idea de una temperatura mínima posible ha existido por mucho tiempo.
Primeras ideas
Uno de los primeros científicos en hablar de una temperatura mínima fue Robert Boyle en 1665. Se preguntaba si existía un "frío extremo" natural.
El termómetro de aire
En 1702, el físico francés Guillaume Amontons mejoró el termómetro de aire. Notó que si el aire se enfriaba mucho, su volumen se reduciría a cero. Calculó que el cero de su escala estaría alrededor de −240 °C. Más tarde, en 1779, Johann Heinrich Lambert sugirió que −270 °C podría ser el frío absoluto.
El trabajo de Lord Kelvin
A mediados del siglo XIX, después de que se entendiera mejor la relación entre el calor y la energía, Lord Kelvin propuso una escala de temperatura que no dependía de ninguna sustancia. Basándose en los principios de la termodinámica, estableció su cero en −273.15 °C, muy cerca de los cálculos anteriores. Esta es la escala de Kelvin que usamos hoy.
La ley de Charles
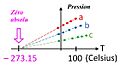
Entre 1787 y 1802, científicos como Jacques Charles y Joseph Louis Gay-Lussac descubrieron que los gases, a presión constante, cambiaban su volumen de forma lineal con la temperatura. Esto sugería que el volumen de un gas se reduciría a cero si se enfriaba a unos −273 °C.
La carrera por el frío extremo
Los científicos estaban muy interesados en alcanzar el cero absoluto en el laboratorio.
- En 1845, Michael Faraday logró licuar la mayoría de los gases conocidos, alcanzando −130 °C.
- En 1877, Louis Paul Cailletet y Raoul Pictet produjeron las primeras gotas de aire líquido a −195 °C.
- En 1883, los profesores polacos Zygmunt Wróblewski y Karol Olszewski produjeron oxígeno líquido a −218 °C.
El desafío final fue licuar el hidrógeno y el helio.
- En 1898, James Dewar licuó el hidrógeno, llegando a −252 °C.
- En 1908, Heike Kamerlingh Onnes fue el primero en licuar el helio, alcanzando −269 °C. Al reducir la presión del helio líquido, llegó a una temperatura aún más baja, cerca de 1.5 K. Por este logro, recibió el Premio Nobel en 1913. Kamerlingh Onnes continuó estudiando las propiedades de los materiales a estas temperaturas, descubriendo la superconductividad y los superfluidos.
Galería de imágenes
-
Robert Boyle fue pionero en la idea de un cero absoluto.
Véase también
 En inglés: Absolute zero Facts for Kids
En inglés: Absolute zero Facts for Kids