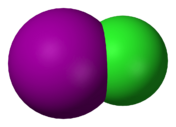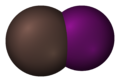Interhalógeno para niños
Un compuesto interhalógeno es una molécula especial que está formada por dos o más tipos diferentes de átomos halógenos. Los halógenos son elementos químicos como el flúor, el cloro, el bromo, el yodo y el astatino. Lo importante es que estos compuestos solo tienen halógenos y ningún otro tipo de elemento.
La mayoría de los compuestos interhalógenos que conocemos están hechos de solo dos halógenos distintos. Sus fórmulas suelen ser XYn, donde 'n' puede ser 1, 3, 5 o 7. La letra X representa el halógeno que atrae los electrones con menos fuerza (es decir, el menos electronegativo). El valor de 'n' siempre es un número impar porque los halógenos tienen una forma particular de unirse. Todos estos compuestos reaccionan fácilmente con el agua (a esto se le llama hidrólisis) y pueden formar iones (partículas con carga eléctrica). Los compuestos que contienen astatina duran muy poco tiempo porque la astatina es un elemento muy inestable.
Hasta ahora, no se han confirmado compuestos interhalógenos que contengan tres o más halógenos diferentes. Aunque algunos estudios sugieren que podrían existir, no son muy estables.
Contenido
- Compuestos Interhalógenos: Una Guía para Jóvenes Químicos
- Galería de imágenes
- Véase también
Compuestos Interhalógenos: Una Guía para Jóvenes Químicos
Los compuestos interhalógenos son fascinantes porque combinan elementos de la misma familia química, los halógenos, de maneras únicas. Entender cómo se forman y cómo se comportan nos ayuda a comprender mejor el mundo de la química.
¿Qué son los Compuestos Interhalógenos?
Los compuestos interhalógenos son como "familias" de átomos halógenos que se unen entre sí. Imagina que los halógenos son hermanos, y estos compuestos son grupos de hermanos que se juntan sin que nadie más se una a ellos. Siempre están formados por al menos dos halógenos diferentes.
Tipos de Compuestos Interhalógenos
Los compuestos interhalógenos se clasifican según cuántos átomos de halógeno tienen en su molécula.
Interhalógenos con Dos Átomos (XY)
Estos compuestos tienen un átomo de un halógeno y un átomo de otro halógeno. Sus características suelen estar entre las de los dos halógenos que los forman. Aunque se unen compartiendo electrones (un enlace covalente), el halógeno menos electronegativo (el que atrae menos los electrones) tiene una pequeña carga positiva. Se conocen muchas combinaciones de flúor, cloro, bromo y yodo, pero no todas son estables. Los que tienen astatina son muy inestables o ni siquiera se han podido formar.
- El monofluoruro de cloro (ClF) es el más ligero de estos compuestos. Es un gas sin color que hierve a -100 °C.
- El monofluoruro de bromo (BrF) no se ha obtenido puro, ya que se descompone rápidamente.
- El monofluoruro de yodo (IF) es inestable y se descompone a 0 °C.
- El monocloruro de bromo (BrCl) es un gas de color marrón amarillento que hierve a 5 °C.
- El monocloruro de yodo (ICl) se presenta como cristales rojos transparentes que se derriten a 27.2 °C, formando un líquido marrón.
- El monocloruro de astato (AtCl) se crea combinando astato gaseoso con cloro.
- El monobromuro de yodo (IBr) es un sólido cristalino de color rojo oscuro. Se derrite a 42 °C y hierve a 116 °C.
- El monobromuro de astato (AtBr) se forma al combinar astato con bromo.
- El monoioduro de astato (AtI) se fabrica uniendo astato y yodo.
No se han descubierto fluoruros de astato. Se cree que son tan reactivos que reaccionarían con los recipientes de vidrio.
Interhalógenos con Cuatro Átomos (XY₃)
Estos compuestos tienen un átomo de un halógeno central y tres átomos de otro halógeno.
- El trifluoruro de cloro (ClF₃) es un gas sin color que se vuelve un líquido verde y luego un sólido blanco. Se usa en la fabricación de hexafluoruro de uranio.
- El trifluoruro de bromo (BrF₃) es un líquido amarillo-verdoso que conduce la electricidad. Se usa en química orgánica para añadir flúor a otras moléculas.
- El trifluoruro de yodo (IF₃) es un sólido amarillo que se descompone por encima de los -28 °C. No se sabe mucho de él porque es muy inestable.
- El tricloruro de yodo (ICl₃) forma cristales de color amarillo limón. Reacciona con muchos cloruros de metales.
Interhalógenos con Seis Átomos (XY₅)
Todos los interhalógenos estables con seis u ocho átomos tienen un halógeno más pesado unido a cinco o siete átomos de flúor. El flúor es muy bueno para estabilizarlos debido a su tamaño pequeño y su fuerte atracción por los electrones.
- El pentafluoruro de cloro (ClF₅) es un gas sin color. Reacciona muy fuerte con el agua y la mayoría de los metales y no metales.
- El pentafluoruro de bromo (BrF₅) es un líquido sin color que produce vapores. Reacciona fuertemente con el agua y la mayoría de los metales y no metales.
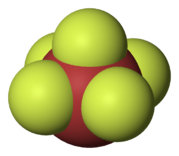
- El pentafluoruro de yodo (IF₅) es un líquido sin color. Es muy reactivo, incluso con el vidrio.
Interhalógenos con Ocho Átomos (XY₇)
Estos son los interhalógenos más grandes conocidos.
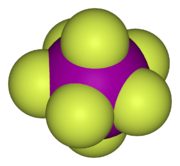
- El heptafluoruro de yodo (IF₇) es un gas sin color y un agente muy fuerte para añadir flúor. Es el único compuesto interhalógeno conocido donde el átomo más grande tiene siete átomos más pequeños unidos a él.
- Todos los intentos de crear heptafluoruro de bromo o de cloro no han tenido éxito.
¿Cómo se Producen los Interhalógenos?
Los interhalógenos se pueden producir de varias maneras. Una forma es exponer interhalógenos más pequeños a halógenos puros. Por ejemplo, el ClF₃ se puede hacer a partir de ClF y F₂. Este método es muy útil para crear fluoruros de halógenos.
También es posible producir interhalógenos combinando directamente dos halógenos puros bajo diferentes condiciones. Este método puede crear casi cualquier interhalógeno, excepto el IF₇.
¿Para Qué Sirven los Interhalógenos?
Algunos interhalógenos son muy útiles en la química.
- El BrF₃, el IF₅ y el ICl son buenos para añadir halógenos a otras sustancias.
- El monocloruro de yodo se usa para medir la cantidad de grasa en aceites y como catalizador (algo que acelera una reacción) en algunas reacciones.
- Varios interhalógenos, como el IF₇, se usan para formar otros compuestos llamados polihaluros.
Características Especiales de los Interhalógenos
Los enlaces en los interhalógenos suelen ser más reactivos que los enlaces en las moléculas de halógenos puros (como F₂ o Cl₂), porque los enlaces interhalógenos son más débiles.
- Cuando los interhalógenos entran en contacto con el agua, se transforman en iones. Con el BrF₅, esta reacción puede ser muy fuerte.
- La capacidad de un interhalógeno para oxidar (quitar electrones a otra sustancia) aumenta con el número de halógenos unidos al átomo central.
- Los interhalógenos que contienen flúor tienden a evaporarse más fácilmente que los que tienen halógenos más pesados.
- La mayoría de los interhalógenos son gases. Algunos, especialmente los que contienen bromo, son líquidos, y la mayoría de los que contienen yodo son sólidos.
- Cuanto mayor es la diferencia en la fuerza con la que los dos halógenos atraen electrones, mayor es el punto de ebullición del interhalógeno.
- Todos los interhalógenos son diamagnéticos, lo que significa que son ligeramente repelidos por un campo magnético.
Otros Compuestos Similares
Existen compuestos parecidos que contienen "pseudohalógenos", que son grupos de átomos que se comportan de forma similar a los halógenos. Algunos ejemplos son las azidas halógenas (como FN₃, ClN₃) y los cianógenos halógenos (como FCN, ClCN).
Galería de imágenes
Véase también
 En inglés: Interhalogen Facts for Kids
En inglés: Interhalogen Facts for Kids
- Intercalcogen
- Haluro de hidrógeno