Ciclopropano para niños
Datos para niños
Ciclopropano |
||
|---|---|---|
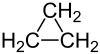    |
||
| Nombre IUPAC | ||
| Ciclopropano | ||
| General | ||
| Fórmula semidesarrollada | C3H8 | |
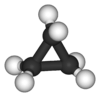
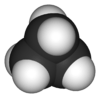
| Fórmula estructural | Ver imagen | |
| Fórmula molecular | C3H8 | |
| Identificadores | ||
| Número CAS | 75-19-4 | |
| ChEBI | 30365 | |
| ChEMBL | CHEMBL1796999 | |
| ChemSpider | 6111 | |
| DrugBank | DB13984 | |
| PubChem | 6351 | |
| UNII | 99TB643425 | |
| KEGG | D03627 | |
|
InChI
InChI=InChI=1S/C3H6/c1-2-3-1/h1-3H2
Key: LVZWSLJZHVFIQJ-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Densidad | 1879 kg/m³; 0001 g/cm³ | |
| Masa molar | 42,08 g/mol | |
| Punto de fusión | 145 K (−128 °C) | |
| Punto de ebullición | 240 K (−33 °C) | |
| Peligrosidad | ||
| Límites de explosividad | 2.4% - 10.4% | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El ciclopropano es un gas que se usó como anestésico. Esto significa que ayudaba a las personas a quedarse dormidas durante las operaciones. Hoy en día, se usan otras sustancias para este fin. El ciclopropano era muy reactivo en condiciones normales. Si se mezclaba con oxígeno, existía un riesgo importante de explosión.
Contenido
Ciclopropano: Un Gas Especial
¿Qué es el Ciclopropano?
El ciclopropano es un tipo de compuesto químico llamado cicloalcano. Su fórmula es C3H6. Esto significa que tiene tres átomos de carbono unidos entre sí. Forman una especie de anillo o triángulo. Cada átomo de carbono también está unido a dos átomos de hidrógeno.
Es el cicloalcano más sencillo que existe. Las uniones entre los átomos de carbono en el ciclopropano son un poco diferentes. Son menos fuertes que las uniones típicas entre átomos de carbono. Esto se debe a que los átomos de carbono forman un ángulo de 60 grados. Este ángulo es mucho más pequeño que el ángulo normal de 109.5 grados que suelen tener.
Debido a este ángulo tan cerrado, el ciclopropano es más reactivo. Es decir, reacciona más fácilmente que otros compuestos similares. Por ejemplo, es más reactivo que los alcanos que no tienen forma de anillo. También es más reactivo que otros cicloalcanos como el ciclohexano o el ciclopentano.
¿Cómo se usaba en Medicina?
El ciclopropano se empezó a usar en la medicina por el anestesista estadounidense Ralph Waters. Él lo usaba en un sistema especial para que no se desperdiciara. Este gas tenía un olor dulce y no irritaba.
Cuando se mezclaba ciclopropano con oxígeno y se inhalaba, las personas se dormían rápidamente. Además, no era desagradable para los pacientes.
¿Por qué ya no se usa?
A pesar de sus ventajas, el ciclopropano dejó de usarse. Una de las razones era su alto costo. Pero la razón principal era su naturaleza explosiva. Si el gas se mezclaba con oxígeno, podía explotar.
Además, después de una anestesia prolongada con ciclopropano, algunos pacientes podían tener una bajada repentina de la presión arterial. Esto podía causar problemas con el ritmo del corazón. Esta reacción se conocía como "choque ciclopropano". Por todas estas razones, el ciclopropano se usó cada vez menos. Finalmente, fue reemplazado por otros agentes anestésicos más seguros.
Véase también
 En inglés: Cyclopropane Facts for Kids
En inglés: Cyclopropane Facts for Kids

