Acetato de litio para niños
Datos para niños
Acetato de litio |
||
|---|---|---|
 Cristales de acetato de litio
|
||
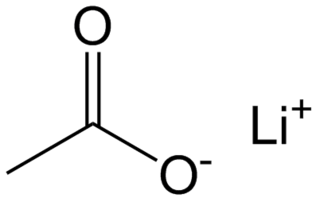 Estructura
|
||
| General | ||
| Fórmula estructural | <chem>CH3COOLi</chem> | |
| Fórmula molecular | <chem>C2H3LiO2</chem> | |
| Identificadores | ||
| Número CAS | 546-89-4 | |
| KEGG | D08134 | |
|
InChI
InChI=InChI=1S/C2H4O2.Li/c1-2(3)4;/h1H3,(H,3,4);/q;+1/p-1
Key: XIXADJRWDQXREU-UHFFFAOYSA-M |
||
| Propiedades físicas | ||
| Apariencia | cristal | |
| Densidad | 1230 kg/m³; 1,23 g/cm³ | |
| Masa molar | 65,99 g/mol | |
| Punto de fusión | 286 °C (559 K) | |
| Propiedades químicas | ||
| Solubilidad en agua | 45.0 g/100 mL | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El acetato de litio es una sustancia química. Es una sal, lo que significa que se forma cuando un ácido y una base se unen. En este caso, se forma a partir de litio y ácido acético. Se ve como un polvo blanco o cristales. A veces, también se encuentra con moléculas de agua unidas a él.
Contenido
¿Cómo se obtiene el acetato de litio?
El acetato de litio se puede crear de varias maneras en un laboratorio.
Reacción con hidróxido de litio
Una forma es mezclando hidróxido de litio con ácido acético. Esta reacción produce acetato de litio disuelto en agua.
-
- <chem>LiOH{_{(s)}} + CH3COOH{_{(l)}} -> CH3COOLi{_{(aq)}} + H2O{_{(l)}} </chem>
Reacción con carbonato de litio
También se puede obtener usando carbonato de litio y ácido acético. En esta reacción, además de acetato de litio, se libera dióxido de carbono en forma de gas.
-
- <chem>Li2CO3{_{(s)}} + 2CH3COOH{_{(l)}} -> 2CH3COOLi{_{(aq)}} + CO2\uparrow{_{(g)}} + H2O{_{(l)}} </chem>
¿Qué propiedades tiene el acetato de litio?
El acetato de litio es un material cristalino de color blanco.
Solubilidad
Se disuelve fácilmente en agua. También puede disolverse en éter y un poco en etanol.
Formas cristalinas
Cuando el acetato de litio tiene dos moléculas de agua unidas (dihidratado), forma cristales transparentes. Estos cristales pueden tener dos estructuras diferentes, llamadas forma-α y forma-β, con densidades ligeramente distintas.
¿Para qué se usa el acetato de litio?
El acetato de litio tiene varios usos importantes en la ciencia y la industria.
En el laboratorio: Electroforesis
En los laboratorios, el acetato de litio se usa como un "tampón" para la electroforesis en gel. Esta técnica ayuda a separar y estudiar el ADN y el ARN.
- ¿Por qué es útil? El acetato de litio permite que la electroforesis sea más rápida. Esto se debe a que conduce menos electricidad que otros tampones comunes.
- Menos calor: Al generar menos calor, la temperatura del gel se mantiene más baja. Esto permite usar voltajes más altos para acelerar el proceso.
- Resultados confiables: Las pruebas posteriores con el ADN o ARN separado funcionan bien.
Para fragmentos muy pequeños de ADN (menos de 500 pares de bases), a veces se prefieren otros tampones. Estos otros tampones pueden dar una mejor separación en ese rango de tamaño.
En la industria química
El acetato de litio también se usa en la fabricación de ciertos materiales:
- Es un catalizador en la producción de poliéster. Un catalizador es una sustancia que acelera una reacción química.
- Ayuda a prevenir la corrosión en algunas resinas.
- Se usa en la creación de resinas alquídicas y polímeros acrílicos.
En la medicina
Este compuesto se utiliza en algunos tratamientos que emplean sales de litio.
Otros usos
El acetato de litio también se usa para ayudar a que las células de levadura sean más permeables. Esto significa que permite que el ADN entre en ellas, lo cual es útil en experimentos de biología molecular.
Véase también
 En inglés: Lithium acetate Facts for Kids
En inglés: Lithium acetate Facts for Kids

