Triyoduro de nitrógeno para niños
Datos para niños
Triyoduro de nitrógeno |
||
|---|---|---|
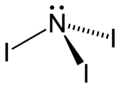
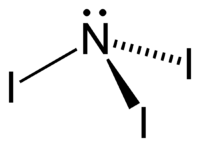 Fórmula estructural
|
||
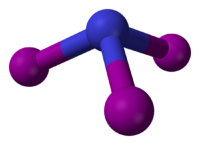 Estructura tridimensional.
|
||
| General | ||
| Otros nombres | Yoduro de nitrógeno, Triyoduro de amoníaco | |
| Fórmula estructural | 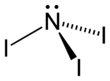 |
|
| Fórmula molecular | NI3 | |
| Identificadores | ||
| Número CAS | 13444-85-4 | |
| ChemSpider | 55511 | |
| PubChem | 61603 | |
|
InChI
InChI=InChI=1S/I3N/c1-4(2)3
Key: FZIONDGWZAKCEX-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Apariencia | rojo (parecido al ladrillo) | |
| Masa molar | 394,77 g/mol | |
| Propiedades químicas | ||
| Solubilidad en agua | no | |
| Peligrosidad | ||
| NFPA 704 |
0
1
4
|
|
| Riesgos | ||
| Riesgos principales | Explosivo extremadamente sensible | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El triyoduro de nitrógeno es un compuesto inorgánico con la fórmula NI3. Es conocido por ser un material muy inestable que reacciona con gran facilidad. Incluso un toque suave puede hacer que se descomponga rápidamente, liberando una nube de vapor de yodo de color púrpura.
Contenido
¿Qué es el Triyoduro de Nitrógeno?
El triyoduro de nitrógeno es una sustancia química que combina nitrógeno y yodo. Su fórmula, NI3, nos dice que cada molécula tiene un átomo de nitrógeno y tres átomos de yodo. Es famoso por su alta inestabilidad, lo que significa que sus enlaces químicos son muy débiles y se rompen con facilidad.
¿Cómo se ve y qué propiedades tiene?
Este compuesto tiene un color rojizo, similar al de un ladrillo. Su masa molar es de 394,77 g/mol. No se disuelve en agua.
Una característica interesante es que su punto de fusión comienza a los -20 °C. A esta temperatura, el triyoduro de nitrógeno puede empezar a sublimarse, es decir, pasar directamente de estado sólido a gaseoso sin convertirse en líquido.
¿Por qué reacciona tan fácilmente?
La razón principal de la alta reactividad del triyoduro de nitrógeno es su estructura química. Cuando está seco, es muy inestable. Esto se debe a que la forma en que sus átomos están unidos no es muy fuerte. Una pequeña cantidad de energía, como un ligero toque, puede romper estos enlaces.
Cuando el triyoduro de nitrógeno se descompone, se transforma rápidamente en nitrógeno gaseoso (N2) y yodo gaseoso (I2). Esta transformación de un sólido a tres gases libera mucha energía en muy poco tiempo. Por eso, incluso una pequeña perturbación puede iniciar esta reacción.
La reacción de descomposición es la siguiente:
- 2 NI3(s) → N2(g) + 3 I2(g)
¿Cómo se prepara este compuesto?
El triyoduro de nitrógeno fue estudiado por primera vez en 1990 usando una técnica llamada cristalografía de rayos X. Esto permitió a los científicos entender mejor su estructura.
Una forma de prepararlo es haciendo reaccionar nitruro de boro con monofluoruro de yodo a temperaturas muy bajas (-30 °C). Esta reacción produce NI3 puro, aunque en pequeñas cantidades:
- BN + 3IF → NI3 + BF3
También se puede preparar el triyoduro de nitrógeno haciendo reaccionar yodo con amoníaco. Si esta reacción se hace a bajas temperaturas con amoníaco sin agua, el primer producto es NI3 · (NH3)5. Este material puede perder algo de amoníaco al calentarse, formando NI3 · (NH3). Esta forma es más estable si se mantiene fría y húmeda con amoníaco.
Galería de imágenes
Véase también
 En inglés: Nitrogen triiodide Facts for Kids
En inglés: Nitrogen triiodide Facts for Kids