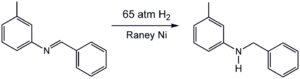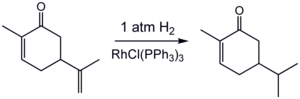Hidrogenación para niños
La hidrogenación es un tipo de reacción química donde se añade hidrógeno (H2) a otro compuesto. Generalmente, esta reacción se aplica a compuestos orgánicos que tienen enlaces dobles o triples, como los alquenos o alquinos. La mayoría de las veces, la hidrogenación se realiza añadiendo hidrógeno gaseoso bajo presión y con la ayuda de un catalizador.
Un ejemplo sencillo es cuando se añade hidrógeno a los enlaces dobles de los alquenos, transformándolos en alcanos, que son compuestos con solo enlaces simples.
La hidrogenación es muy importante en varias industrias, como la de alimentos, la farmacéutica y la petroquímica.
Contenido
Historia de la Hidrogenación
Se considera que el químico francés Paul Sabatier es el pionero de la hidrogenación. En 1897, él descubrió que pequeñas cantidades de níquel ayudaban a que el hidrógeno se uniera a moléculas de compuestos orgánicos en estado gaseoso.
Más tarde, en 1902 en Alemania y en 1903 en Gran Bretaña, Wilhelm Normann patentó un método para hidrogenar aceites líquidos usando hidrógeno gaseoso. Esto marcó el inicio de una gran industria a nivel mundial.
¿Cómo Funciona la Hidrogenación?
La hidrogenación es la adición de H2 a compuestos orgánicos que no están "saturados" (es decir, tienen enlaces dobles o triples). Por ejemplo, puede transformar alquenos en alcanos, o aldehídos en alcoholes.
Para que la hidrogenación ocurra, se necesitan tres elementos principales:
- El compuesto al que se le va a añadir hidrógeno (llamado sustrato).
- Una fuente de hidrógeno.
- Un catalizador metálico.
La reacción se lleva a cabo a diferentes temperaturas y presiones, dependiendo del sustrato y de la actividad del catalizador.
Sustratos: ¿A qué se añade el hidrógeno?
Cuando se añade H2 a un alqueno, se produce un alcano. Por ejemplo:
- RCH=CH2 + H2 → RCH2CH3
El hidrógeno se añade a los enlaces dobles o triples de una manera específica, generalmente por el lado de la molécula que tiene menos obstáculos.
Algunos ejemplos de compuestos que se pueden hidrogenar y sus productos son:
- Alquenos se convierten en alcanos.
- Alquinos se convierten en alquenos (con una forma específica llamada cis).
- Aldehídos se convierten en alcoholes primarios.
- Cetonas se convierten en alcoholes secundarios.
- Ésteres se convierten en dos alcoholes.
- Iminas se convierten en aminas.
- Amidas se convierten en aminas.
- Nitrilos se convierten en iminas (que pueden hidrogenarse de nuevo).
- Nitrocompuestos se convierten en aminas primarias.
Catalizadores: Los Ayudantes de la Reacción
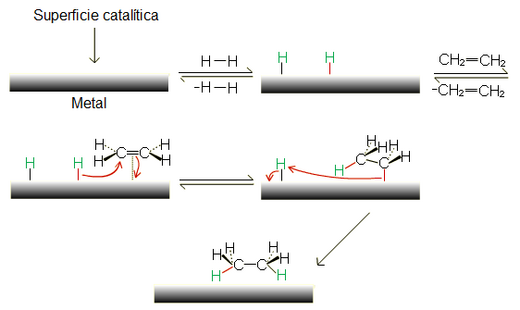
Sin catalizadores metálicos, el hidrógeno gaseoso (H2) y los compuestos orgánicos no reaccionan fácilmente a temperaturas normales. El catalizador se une tanto al H2 como al compuesto, facilitando que se unan.
Metales como el platino, paladio, rodio y rutenio son catalizadores muy activos. Funcionan bien a bajas temperaturas y presiones de hidrógeno. Algunos ejemplos son el catalizador de Adams y el catalizador de Wilkinson.
También existen catalizadores más económicos, como los basados en níquel (Níquel Raney y Níquel Urushibara). Sin embargo, estos a menudo hacen que el proceso sea más lento o requieren temperaturas más altas. La elección del catalizador depende de un equilibrio entre su costo y la velocidad de la reacción.
Existen dos tipos principales de catalizadores:
- Catalizadores homogéneos: Se disuelven en el mismo líquido donde está el compuesto a hidrogenar.
- Catalizadores heterogéneos: Son sólidos que se suspenden en el líquido o se usan con compuestos en estado gaseoso.
Catálisis Homogénea
Un ejemplo de catalizador homogéneo es el catalizador de Wilkinson, que contiene rodio. Estos catalizadores permiten controlar la reacción de manera muy precisa. Por ejemplo, pueden ayudar a que se forme un tipo específico de molécula cuando el compuesto original puede dar dos formas diferentes.
Catálisis Heterogénea
Los catalizadores heterogéneos son los más usados en la industria. Su actividad se puede ajustar cambiando el entorno alrededor del metal. A veces, se usan "sustancias especiales" que detienen la hidrogenación en un punto intermedio. Esto permite hidrogenar solo ciertas partes de una molécula sin afectar otras.
Por ejemplo, el Catalizador Lindlar se usa para transformar alquinos en alquenos sin que se conviertan en alcanos.
Fuentes de Hidrógeno
La fuente más común de hidrógeno para estas reacciones es el gas H2, que se compra en cilindros a presión. A menudo, la hidrogenación se realiza a presiones más altas que la presión atmosférica normal.
Hidrogenación por Transferencia
El hidrógeno también se puede obtener de otras moléculas, llamadas "donantes de hidrógeno", en lugar de usar hidrógeno gaseoso. Estos donantes pueden ser líquidos como la hidracina o el ácido fórmico. Este método es útil para reducir compuestos específicos.
Hidrogenación Electrolítica
Algunos compuestos, como las cetonas, pueden hidrogenarse usando electricidad. En este proceso, se usan líquidos especiales y la electricidad actúa como fuente de hidrógeno.
¿Qué Pasa con la Energía en la Hidrogenación?
La hidrogenación es una reacción que libera mucho calor, es decir, es exotérmica. Por ejemplo, al hidrogenar aceites vegetales, se libera suficiente calor para aumentar la temperatura del aceite.
El proceso de hidrogenación ha sido muy estudiado. Se sabe que el hidrógeno se añade a la molécula de una forma específica.
Cuando se hidrogenan compuestos con anillos aromáticos (como el benceno), el primer enlace es más difícil de hidrogenar porque se necesita mucha energía para romper la estabilidad del anillo. El producto intermedio es muy reactivo y se hidrogena rápidamente hasta convertirse en un compuesto completamente saturado.
Usos en la Industria Alimenticia
La hidrogenación se utiliza en la fabricación de algunos alimentos para obtener grasas semisólidas. Este proceso cambia la forma de los ácidos grasos, lo que afecta su punto de fusión y otras propiedades.
Durante este proceso, los enlaces dobles de los ácidos grasos pueden cambiar de una forma llamada "cis" a una forma llamada "trans". Los ácidos grasos "trans" (AGt) pueden hacer que las cadenas de carbono se mantengan más rígidas.
Los ácidos grasos trans que se forman en este proceso son un tema de interés en la industria alimenticia debido a que se ha investigado su impacto en la salud.
Los aceites parcialmente hidrogenados comenzaron a usarse en alimentos a principios del siglo XX como una alternativa a la mantequilla. Se hicieron más populares en las décadas de 1950, 1960 y 1970.
La Organización Mundial de la Salud (OMS) ha señalado que los ácidos grasos trans, que se forman al convertir aceites líquidos en grasas sólidas, suelen encontrarse en algunos aperitivos, alimentos horneados o fritos. La OMS sugiere que el consumo de grasas trans puede estar relacionado con problemas de salud. La OMS recomienda que la cantidad total de grasas trans que se consume sea muy limitada.
Véase también
 En inglés: Hydrogenation Facts for Kids
En inglés: Hydrogenation Facts for Kids
- Hidrogenación (aceites)
- Catalizador de Adkins
- Níquel Raney
- Catalizador de Wilkinson