Complejo mayor de histocompatibilidad para niños
El Complejo Mayor de Histocompatibilidad (conocido como CMH o MHC por sus siglas en inglés) es un grupo de genes muy importantes que se encuentran en todos los animales con columna vertebral, incluyendo a los humanos. En nuestro caso, estos genes están en el cromosoma 6. Su trabajo principal es crear unas moléculas especiales, como "tarjetas de identificación" para nuestras células.
Estas moléculas, llamadas antígenos leucocitarios humanos (o HLA en humanos), ayudan a nuestro sistema inmunitario a reconocer qué células son nuestras y cuáles son extrañas, como las de virus o bacterias. Así, el sistema inmunitario sabe a quién atacar para protegernos.
El CMH es una de las partes más variadas de nuestro genoma (nuestro mapa genético). Esto significa que hay muchas versiones diferentes de estos genes, lo que ayuda a que cada persona tenga un sistema inmunitario único y fuerte.
Contenido
Descubrimiento del CMH
El CMH fue descubierto en la década de 1950. Antes de eso, en 1900, se habían encontrado los grupos sanguíneos, y en 1940, el factor Rh. Estos descubrimientos fueron importantes para entender cómo nuestro cuerpo reconoce diferentes tipos de células.
Primeros pasos en la investigación
En 1936, un científico llamado Peter Gorer fue el primero en describir un sistema similar al CMH en ratones. Luego, George Snell sugirió que el rechazo de tejidos en ratones se debía a diferencias en ciertas moléculas. A este sistema en ratones lo llamaron "H-2".
En 1952, Jean Dausset pensó que algo parecido a los grupos sanguíneos debía existir en los leucocitos (glóbulos blancos). Demostró esto al ver cómo los glóbulos blancos de un paciente se agrupaban con el suero de otra persona. Por su trabajo, recibió un Premio Nobel.
Avances en la identificación
La primera vez que se identificó una molécula específica del CMH fue en 1958. Se le llamó antígeno MAC, que hoy conocemos como HLA-A2. En los años 60, otros científicos como Jon van Rod, Rose Payne y Walter Bodmer confirmaron que estas moléculas eran muy variadas.
En 1964, se inició un gran esfuerzo internacional para estudiar el CMH, llamado el Taller Internacional de Histocompatibilidad. Allí se descubrió que los genes HLA-A, B y C estaban en el cromosoma 6. Al principio, se pensó que solo estaban en los glóbulos blancos, por eso se les llamó "antígenos leucocitarios humanos" (HLA).
En los años 70, se identificaron las moléculas HLA de clase II. Con el tiempo, la investigación se centró más en los genes que en las moléculas que producían.
Reconocimiento de la función inmune
En 1969, Baruj Benacerraf demostró algo muy importante: el CMH no solo causaba el rechazo en los trasplantes, sino que también era clave para activar la respuesta del sistema inmunitario contra cosas extrañas. Por este descubrimiento, también ganó un Premio Nobel en 1980.
En 1987, Bjorkman logró ver la estructura detallada de las moléculas HLA-A2 y las de clase II. Finalmente, en 1999, se logró descifrar la secuencia completa de los genes del CMH.
Entre 1980 y 2000, el conocimiento sobre el CMH creció muchísimo. Se descubrieron miles de versiones diferentes de estos genes. La región HLA-B se convirtió en la parte más variada del genoma humano. Las variaciones en el CMH son muy importantes porque influyen en cómo nuestro cuerpo se defiende de enfermedades.
Cómo se organizan los genes del CMH
La región del CMH es la parte del genoma de los mamíferos con más genes y más variedad. Es fundamental para nuestra inmunidad.
El CMH en humanos
En los humanos, el CMH es una sección muy grande del cromosoma 6 que contiene más de 200 genes.
Esta región se divide en dos zonas principales:
- Una zona tiene los genes de clase II. Estos genes producen moléculas que ayudan a presentar partes de invasores (como bacterias) a un tipo de linfocitos T llamados "cooperadores".
- La otra zona tiene los genes de clase I. Estos genes producen moléculas que presentan partes de invasores (como virus) a otro tipo de linfocitos T, llamados "citotóxicos".
Entre estas dos zonas, hay otros genes que también son importantes para la respuesta inmune, como los que producen proteínas del sistema del complemento.
Ambos tipos de moléculas del CMH son como "detectives" que muestran "pistas" (pequeños fragmentos de proteínas) a los linfocitos T. Así, el sistema inmunitario puede identificar y eliminar lo que no pertenece a nuestro cuerpo.
Moléculas CMH de clase I
Las moléculas CMH de clase I se encuentran en casi todas las células de nuestro cuerpo, excepto en los glóbulos rojos. Son como la "identificación" de cada célula.
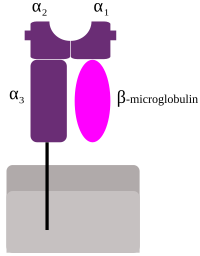
Los genes principales de clase I son HLA-A, HLA-B y HLA-C. Son muy variados, con miles de versiones diferentes. Estas moléculas están formadas por una cadena pesada (llamada alfa) y una cadena más pequeña (beta2 microglobulina).
Su función principal es mostrar péptidos (pequeños trozos de proteínas) que vienen de dentro de la célula a los linfocitos T citotóxicos (CD8+). Si la célula está infectada por un virus, por ejemplo, el CMH de clase I mostrará un trozo de proteína viral. El linfocito T CD8+ lo reconocerá y destruirá la célula infectada.
Moléculas CMH de clase II
Las moléculas CMH de clase II se encuentran principalmente en células especiales llamadas células presentadoras de antígenos, como las células dendríticas y los macrófagos. Estas células son como "centinelas" que recogen información del exterior.
Estas moléculas están formadas por dos cadenas, una alfa y una beta. Su trabajo es presentar péptidos que vienen de fuera de la célula (por ejemplo, de bacterias que la célula ha "comido") a los linfocitos T cooperadores (CD4+). Los linfocitos T CD4+ no destruyen la célula directamente, sino que ayudan a coordinar la respuesta inmune.
La gran variedad del CMH
La región del CMH es muy especial por dos razones:
- Es poligénica: tiene varios genes diferentes de clase I y de clase II.
- Es polimórfica: de cada uno de esos genes, existen muchísimas versiones o alelos diferentes en la población.
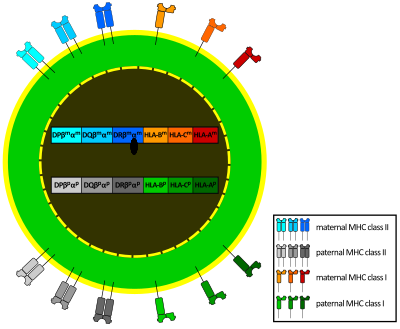
Los genes del CMH se expresan de forma codominante. Esto significa que heredamos una versión de cada gen de nuestra madre y otra de nuestro padre, y ambas versiones se expresan al mismo tiempo. Por ejemplo, una célula puede tener hasta seis tipos diferentes de moléculas CMH de clase I.
El conjunto de alelos que una persona hereda en un cromosoma se llama haplotipo CMH. Cada persona tiene dos haplotipos CMH, uno de cada progenitor.
La gran variedad del CMH es tan grande que, excepto los gemelos idénticos, no hay dos personas que tengan exactamente el mismo conjunto de genes y moléculas CMH.
Esta variedad es crucial para nuestra supervivencia. Las partes más variadas de cada molécula CMH son las que entran en contacto con los péptidos. Esto significa que cada versión de la molécula CMH puede unirse a un tipo específico de péptido. Así, aunque cada molécula CMH puede presentar muchos péptidos diferentes, no puede presentar todos.
En una población, la existencia de tantos alelos diferentes asegura que siempre habrá personas con moléculas CMH capaces de reconocer y combatir un nuevo microbio o uno que haya mutado. Esto ayuda a que la población en general pueda defenderse de una gran diversidad de amenazas.
Funciones de las moléculas del CMH
Las moléculas CMH de clase I y clase II presentan péptidos a los linfocitos T, lo que es esencial para que nuestro sistema inmunitario elimine los invasores. Sin embargo, lo hacen de maneras diferentes:
| Característica | Vía CMH de clase II | Vía CMH de clase I |
|---|---|---|
| Células que las presentan | Células dendríticas, macrófagos, linfocitos B | Casi todas las células del cuerpo |
| Linfocitos T que responden | Linfocitos T cooperadores (CD4+) | Linfocitos T citotóxicos (CD8+) |
| Origen de las proteínas | Proteínas de fuera de la célula (ej. bacterias) | Proteínas de dentro de la célula (ej. virus) |
| Dónde se unen los péptidos | En compartimentos especiales dentro de la célula | En el Retículo endoplásmico |
Los linfocitos T de una persona solo pueden reconocer un péptido si este es presentado por una molécula CMH de la misma persona. Esto se llama restricción del CMH. Es como si los linfocitos T solo confiaran en las "tarjetas de identificación" de su propio cuerpo.
Las moléculas del CMH solo pueden presentar péptidos (trozos de proteínas). Esto significa que los linfocitos T solo reaccionan a antígenos que son proteínas, no a grasas o azúcares. Cada molécula CMH puede presentar un solo péptido a la vez, pero puede presentar muchos tipos diferentes de péptidos.
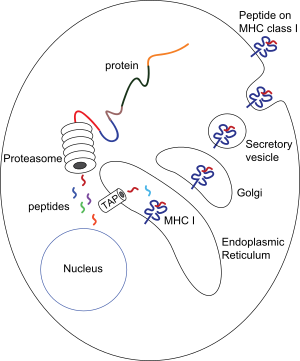
Las moléculas del CMH adquieren los péptidos que van a presentar mientras se están formando dentro de la célula. Por eso, los péptidos que presentan vienen de microbios que están dentro de la célula. Las moléculas CMH de clase I presentan péptidos de proteínas que están en el citoplasma (como las de los virus), mientras que las de clase II presentan péptidos de proteínas que están en vesículas dentro de la célula (como las de bacterias que la célula ha "comido").
Las moléculas del CMH solo se muestran en la superficie de la célula si tienen un péptido unido. Si no tienen un péptido, se degradan. Las moléculas con péptidos pueden permanecer en la superficie por días, dando tiempo a que un linfocito T las encuentre y active la respuesta inmune.
En cada persona, las moléculas del CMH pueden presentar tanto péptidos propios (de las proteínas de nuestro propio cuerpo) como péptidos extraños (de invasores). La mayoría de los péptidos que se presentan son propios, porque son más abundantes. Sin embargo, los linfocitos T son muy sensibles y pueden detectar un péptido extraño incluso si solo una pequeña parte de las moléculas CMH lo presentan.
Los péptidos propios normalmente no activan una respuesta inmune, porque los linfocitos T que reaccionarían contra ellos son eliminados o desactivados en el timo (un órgano del sistema inmunitario). La presencia de péptidos propios en las moléculas CMH es importante para que los linfocitos T puedan "patrullar" el cuerpo, buscando constantemente cualquier péptido extraño.
El CMH y los trasplantes
Las moléculas del CMH fueron identificadas por primera vez por su papel en el rechazo de trasplantes de tejidos entre ratones. En humanos, estas moléculas se llaman antígenos HLA.
Como ya sabes, cada célula humana expresa muchas versiones diferentes de moléculas CMH de clase I y clase II. La gran variedad de estos genes hace que sea muy raro que dos personas, que no sean gemelos idénticos, tengan exactamente las mismas moléculas CMH.
Cuando se realiza un trasplante de órganos o de células madre, las moléculas HLA del donante pueden actuar como antígenos. Esto significa que pueden ser reconocidas como "extrañas" por el sistema inmunitario del receptor, lo que puede provocar el rechazo del trasplante. La reacción contra las moléculas CMH de otra persona es una de las respuestas inmunes más fuertes que existen.
Los linfocitos T del receptor pueden confundirse y reconocer las moléculas CMH del donante como si fueran propias, pero con un péptido extraño. Esto hace que el sistema inmunitario del receptor ataque el órgano trasplantado, como si fuera un tejido infectado o con problemas. Este reconocimiento de moléculas CMH extrañas como propias se llama alorreconocimiento.
Existen dos tipos principales de rechazo de trasplantes relacionados con el CMH:
- Rechazo hiperagudo: Ocurre muy rápido si el receptor ya tiene anticuerpos contra las moléculas HLA del donante. Esto puede pasar si la persona ha recibido transfusiones de sangre o trasplantes anteriores.
- Rechazo agudo y disfunción crónica: Se produce cuando el receptor forma nuevos anticuerpos contra las moléculas HLA del trasplante. Esto puede dañar el órgano con el tiempo.
Por estas razones, antes de un trasplante, es muy importante hacer pruebas para ver si las moléculas HLA del donante y del receptor son compatibles. Cuantas más similitudes haya, mayores serán las posibilidades de que el trasplante sea exitoso. La compatibilidad total solo existe entre gemelos idénticos. Hoy en día, existen bases de datos mundiales que ayudan a encontrar donantes con la mejor compatibilidad posible.
Galería de imágenes
Véase también



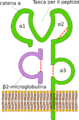
 En inglés:
En inglés: