Óxido de cromo(II) para niños
Datos para niños
Óxido de cromo(II) |
||
|---|---|---|
 |
||
 |
||
| Nombre IUPAC | ||
| Monoxido de cromo | ||
| General | ||
| Fórmula molecular | CrO | |
| Identificadores | ||
| Número CAS | 12018-00-7 | |
| ChemSpider | 2300900 | |
|
O=[Cr]
|
||
|
InChI
InChI=InChI=1S/Cr.O
Key: XVOFZWCCFLVFRR-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Apariencia | negro | |
| Masa molar | 67,996 g/mol | |
| Punto de ebullición | 573,15 K (300 °C) | |
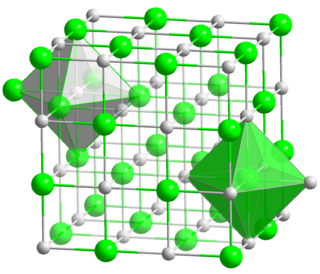
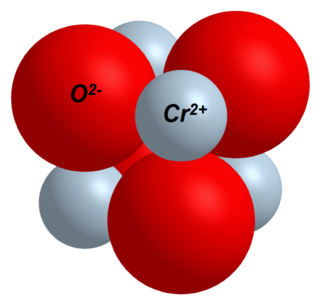
| Estructura cristalina | isométrico, cF8 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El Óxido de cromo(II) (CrO), también conocido como monóxido de cromo, es un compuesto inorgánico que se forma a partir de los elementos cromo y oxígeno. Este compuesto es de color negro y reacciona rápidamente con el aire.
Contenido
¿Cómo se obtiene el Óxido de Cromo(II)?
El óxido de cromo(II) se puede obtener de varias maneras en un laboratorio.
Métodos de preparación del Óxido de Cromo(II)
- Una forma es mediante la oxidación de una mezcla de cromo y mercurio (llamada amalgama de cromo) usando ácido nítrico o oxígeno.
- 2CrHg3 + O2 = 2CrO + 6Hg
- 2CrHg + O2 = 2CrO + 2Hg
- También se puede obtener al reducir otro compuesto de cromo, el óxido de cromo(III), usando una sustancia llamada hipofosfito.
- H3PO2 + 2Cr2O3 → 4CrO + H3PO4
- Otra manera es calentando un compuesto llamado carbonilo de cromo (Cr(CO)6) hasta que se descompone.
Propiedades y reacciones del Óxido de Cromo(II)
El óxido de cromo(II) tiene propiedades químicas interesantes y reacciona con otras sustancias.
¿Cómo reacciona el Óxido de Cromo(II) con el oxígeno?
Cuando el óxido de cromo(II) se calienta a 100 °C, reacciona con el oxígeno del aire para transformarse en óxido de cromo(III).
-
- 4CrO + O2 = 2Cr2O3
¿Puede el Óxido de Cromo(II) convertirse en cromo puro?
Sí, si se calienta el óxido de cromo(II) a 1000 °C junto con hidrógeno, se puede obtener cromo metálico puro.
-
- CrO + H2 = Cr + H2O
También se puede reducir a cromo metálico usando carbono.
-
- CrO + C = Cr + CO
¿Es soluble el Óxido de Cromo(II) en ácidos?
El óxido de cromo(II) se disuelve en ácido clorhídrico. Durante esta reacción, libera hidrógeno y forma cloruro de cromo(III). Sin embargo, no se disuelve en ácido nítrico ni en ácido sulfúrico diluido.
Véase también
 En inglés: Chromium(II) oxide Facts for Kids
En inglés: Chromium(II) oxide Facts for Kids

