Fluoruro de bismuto(V) para niños
Datos para niños
Fluoruro de bismuto(V) |
||
|---|---|---|
 |
||
 |
||
| General | ||
| Otros nombres | Pentafluoruro de bismuto | |
| Fórmula molecular | BiF5 | |
| Identificadores | ||
| Número CAS | 7787-62-4 | |
| ChEBI | 30426 | |
| ChemSpider | 21172752 | |
| PubChem | 123260 | |
| UNII | BX273GFK98 | |
|
InChI
InChI=InChI=1S/Bi.5FH/h;5*1H/q+5;;;;;/p-5
Key: BAHXPLXDFQOVHO-UHFFFAOYSA-I |
||
| Propiedades físicas | ||
| Masa molar | 303,9724148 g/mol | |
El Fluoruro de bismuto(V), también conocido como Pentafluoruro de bismuto, es un compuesto químico con la fórmula BiF5. Es un sólido de color blanco que reacciona con mucha facilidad. Aunque es interesante para los científicos, no tiene muchos usos prácticos.
Contenido
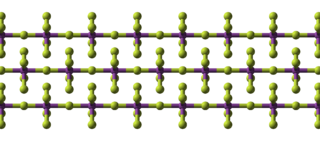
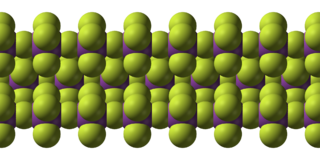
¿Cómo es la estructura del Fluoruro de bismuto(V)?
El BiF5 tiene una estructura especial que se repite, formando cadenas largas. Imagina que son como bloques de construcción que se unen uno tras otro. Cada bloque es un octaedro de BiF6, que es una forma geométrica con ocho caras. Estos bloques se conectan por las esquinas, creando una cadena continua. Esta forma es similar a la de otro compuesto llamado alfa-UF5.
¿Cómo se prepara el Fluoruro de bismuto(V)?
Para obtener BiF5, los científicos pueden usar diferentes métodos.
Preparación con flúor
Una forma es calentar BiF3 junto con F2 a una temperatura muy alta, alrededor de 500 grados Celsius.
- BiF3 + F2 → BiF5
Preparación con trifluoruro de cloro
Otra manera es usar ClF3 como un "agente fluorante". Esto significa que el ClF3 ayuda a añadir átomos de flúor al BiF3. Esta reacción se realiza a unos 350 grados Celsius.
- BiF3 + ClF3 → BiF5 + ClF
¿Qué reacciones tiene el Fluoruro de bismuto(V)?
El pentafluoruro de bismuto es uno de los compuestos más reactivos de su tipo. Es un agente fluorante muy potente, lo que significa que es excelente para añadir flúor a otras sustancias.
Reacciones con agua y otros elementos
Reacciona con mucha fuerza con el agua, formando ozono y difluoruro de oxígeno. También reacciona con el yodo o el azufre a temperatura ambiente.
Reacciones con hidrocarburos y uranio
El BiF5 puede transformar queroseno (que es un tipo de hidrocarburo) en fluorocarbonos si la temperatura supera los 50 grados Celsius. Además, puede cambiar el UF4 a UF6 a 150 grados Celsius.
Reacciones con bromo y cloro
A 180 grados Celsius, el pentafluoruro de bismuto puede añadir flúor al Br2 para formar BrF3. También puede hacer lo mismo con el Cl2 para crear ClF.
Reacciones con fluoruros de metales alcalinos
El BiF5 también reacciona con los fluoruros de metales alcalinos (como el sodio o el potasio) para formar compuestos llamados hexafluorobismutatos. Estos compuestos contienen un grupo especial de átomos llamado anión hexafluorobismutato, que se escribe como [BiF6]-.
Galería de imágenes
Véase también
 En inglés: Bismuth(V) fluoride Facts for Kids
En inglés: Bismuth(V) fluoride Facts for Kids



