Dualidad onda corpúsculo para niños
La dualidad onda-partícula es una idea fascinante de la mecánica cuántica. Nos dice que las cosas muy pequeñas, como los electrones o la luz, pueden comportarse de dos maneras diferentes. A veces actúan como ondas, que se extienden por el espacio, y otras veces como partículas, que son como pequeños puntos localizados.
En la física clásica, que describe el mundo que vemos a diario, una onda y una partícula son muy distintas. Una partícula tiene una posición y una masa definidas, mientras que una onda se propaga y no tiene masa. Pero en el mundo cuántico, esta diferencia se difumina.
El famoso científico Stephen Hawking dijo en 2001 que la dualidad onda-partícula significa que "no hay diferencias fundamentales entre partículas y ondas: las partículas pueden comportarse como ondas y viceversa". Esto ha sido demostrado muchas veces con experimentos.
Esta idea revolucionaria fue propuesta por el físico francés Louis-Victor de Broglie en 1924. Él sugirió que toda la materia tiene una onda asociada. Al principio, su idea no fue muy popular porque no había pruebas. Sin embargo, Albert Einstein vio su importancia, y cinco años después, De Broglie ganó el Premio Nobel de Física por su trabajo.
De Broglie propuso una fórmula para calcular la longitud de onda (que es como el tamaño de la onda) de la onda asociada a la materia:
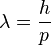
Aquí, 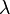 es la longitud de onda,
es la longitud de onda, 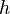 es la constante de Planck (un número muy, muy pequeño), y
es la constante de Planck (un número muy, muy pequeño), y 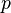 es el momento lineal de la partícula (que depende de su masa y velocidad).
es el momento lineal de la partícula (que depende de su masa y velocidad).
Contenido
Historia de la Dualidad Onda-Partícula
¿Cómo se entendía la luz antes?
Las primeras ideas sobre la luz fueron muy debatidas. Christiaan Huygens propuso que la luz era una onda, como las ondas en el agua. Pero Isaac Newton, un científico muy influyente, pensó que la luz estaba hecha de pequeñas partículas. La teoría de Newton fue la más aceptada durante mucho tiempo.
En el siglo XIX, nuevos experimentos, como el de la difracción (cuando la luz se dobla al pasar por un borde) y la interferencia (cuando dos ondas se encuentran y se combinan), demostraron que la luz se comportaba como una onda. El Experimento de Young fue clave para esto.
Sin embargo, a principios del siglo XX, surgieron nuevos problemas. El efecto fotoeléctrico, explicado por Albert Einstein en 1905, mostró que la luz también tenía propiedades de partícula.
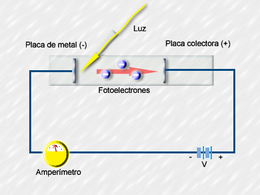
El Efecto Fotoeléctrico y los Fotones
El efecto fotoeléctrico es un fenómeno curioso: si haces incidir luz sobre una placa de metal, puede producir electricidad. Esto ocurre porque la luz "arranca" electrones del metal.
Lo extraño es que una luz azul débil podía arrancar electrones, pero una luz roja muy fuerte no lo hacía. Según la teoría de las ondas, una luz más brillante (más fuerte) debería tener más energía y arrancar más electrones. Pero no era así.
Einstein resolvió este misterio diciendo que la luz está hecha de pequeños "paquetes" de energía llamados fotones. Cada fotón tiene una cantidad de energía que depende de la frecuencia de la luz (su color).

Donde E es la energía, h es la constante de Planck, y ν es la frecuencia.
Solo los fotones con suficiente energía (es decir, con una frecuencia alta, como la luz azul) podían arrancar electrones. La luz roja, aunque fuera muy brillante, tenía fotones con poca energía y no podía hacerlo. Por esta explicación, Einstein también recibió el Premio Nobel de Física en 1921.
Las Ondas de Materia de De Broglie
Inspirado por la idea de Einstein de que la luz (una onda) podía actuar como partícula, Louis-Victor de Broglie se preguntó si lo contrario también era cierto: ¿podrían las partículas (como los electrones) actuar como ondas?
En 1924, De Broglie propuso que toda la materia tiene características tanto de onda como de partícula, y que se comporta de una u otra forma según el experimento. Él relacionó la longitud de onda de una partícula con su momento lineal (masa por velocidad) con la siguiente fórmula:
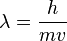
Aquí, λ es la longitud de onda, h es la constante de Planck, m es la masa de la partícula y v es su velocidad. Esta fórmula nos dice que cuanto mayor sea la masa o la velocidad de un objeto, más pequeña será su longitud de onda asociada.
Esta hipótesis fue confirmada tres años después por experimentos que mostraron la difracción de electrones. Esto significa que los electrones, que son partículas, se doblaban y creaban patrones como si fueran ondas. Los científicos George Paget Thomson, Clinton Joseph Davisson y Lester Halbert Germer realizaron estos experimentos y compartieron el Premio Nobel en 1937.
¿Por qué no vemos las propiedades ondulatorias en objetos grandes, como una pelota de fútbol o una persona? Porque su masa es tan grande que la longitud de onda asociada es increíblemente pequeña, ¡demasiado pequeña para ser detectada!
Objetos Más Grandes con Comportamiento Ondulatorio
Se han realizado experimentos similares con neutrones y protones, y más recientemente con átomos y moléculas, demostrando que también actúan como ondas.
En 1999, científicos de la Universidad de Viena observaron la difracción de moléculas de fulereno (C60), que son bastante grandes. Esto demostró que incluso objetos con una masa considerable pueden mostrar propiedades ondulatorias.
Entendiendo la Dualidad Onda-Partícula
La mecánica cuántica nos ayuda a entender la dualidad onda-partícula. En lugar de ver las partículas como puntos que siguen una trayectoria fija, la mecánica cuántica las describe como una especie de "campo de materia" que se propaga como una onda. Las propiedades de onda que vemos son una consecuencia de cómo se propaga este campo.
Cuando medimos la posición de una partícula cuántica, este "campo de materia" parece "colapsar" en una región muy pequeña, haciendo que la partícula aparezca localizada. Es como si la partícula se extendiera como una onda, pero cuando la buscamos, la encontramos en un lugar específico, como una partícula.
Esta idea es un poco extraña porque nuestra experiencia diaria se basa en objetos grandes que siguen las leyes de la mecánica newtoniana. En el mundo cuántico, las cosas son diferentes:
- Los sistemas pueden evolucionar de forma impredecible cuando se miden.
- No podemos conocer con precisión infinita y al mismo tiempo ciertas propiedades de una partícula (esto se conoce como el principio de incertidumbre de Heisenberg).
- Las propiedades de las partículas no existen de forma definida hasta que las observamos.
Las soluciones a las ecuaciones de la mecánica cuántica se llaman funciones de onda. Estas funciones nos dan la probabilidad de encontrar una partícula en un lugar determinado. La partícula se propaga como una onda, pero cuando la detectamos, aparece como una partícula completa y localizada.
Aplicaciones de la Dualidad Onda-Partícula
La dualidad onda-partícula tiene aplicaciones prácticas muy importantes. Un ejemplo es el microscopio de electrones. Como los electrones tienen una longitud de onda muy pequeña, se pueden usar para "ver" objetos mucho más pequeños de lo que se podría ver con la luz visible. Esto permite a los científicos observar detalles diminutos de materiales y células.
Véase también
 En inglés: Wave–particle duality Facts for Kids
En inglés: Wave–particle duality Facts for Kids