Extracción líquido-líquido para niños
La extracción líquido-líquido es una técnica de laboratorio que se usa en química para separar sustancias. Imagina que tienes una sustancia mezclada en un líquido, y quieres sacarla de ahí. Esta técnica usa otro líquido diferente que no se mezcla con el primero (como el aceite y el agua). La idea es que la sustancia que quieres separar se disuelva mejor en el segundo líquido.
Este proceso se basa en principios físicos. La sustancia se mueve de un líquido al otro según qué tan bien se disuelva en cada uno. Es como si la sustancia "eligiera" dónde prefiere estar.
A veces, a este proceso también se le llama extracción líquida o extracción con disolvente. Sin embargo, estos nombres pueden confundirse con la lixiviación, que es cuando se extrae algo de un sólido.
Contenido
¿Cómo funciona la extracción líquido-líquido?
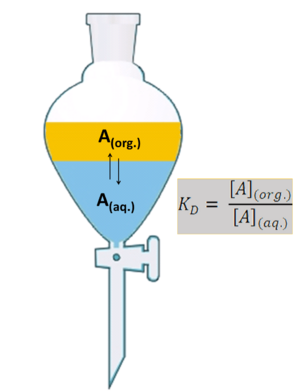
La clave de la extracción líquido-líquido es que una sustancia se distribuye entre dos líquidos que no se mezclan. Piensa en ello como una competencia: la sustancia se disuelve más en uno de los líquidos que en el otro.
La Ley de Distribución
Un científico llamado Walther Nernst explicó este proceso. Él descubrió que, a una temperatura específica, la relación entre la cantidad de una sustancia en un líquido y la cantidad en el otro líquido es siempre la misma. A esta relación se le llama constante de distribución o coeficiente de reparto, y se representa con la letra KD.
Esta constante nos ayuda a saber si una sustancia se puede extraer fácilmente. Si la KD es alta, significa que la sustancia prefiere mucho el segundo líquido, y será más fácil extraerla.
Relación de Distribución: Cuando las cosas cambian
A veces, la sustancia que queremos extraer puede cambiar de forma química en uno de los líquidos. Por ejemplo, una sustancia puede estar como una molécula normal en un líquido, pero en el agua puede dividirse en partes más pequeñas (iones).
Cuando esto sucede, usamos algo llamado relación de distribución, que se representa con la letra D. Esta relación tiene en cuenta todas las formas en que la sustancia puede estar en cada líquido. El valor de D puede cambiar según las condiciones, como la acidez o basicidad (pH) del agua.
Por ejemplo, si una sustancia es más soluble en el líquido orgánico cuando no tiene carga eléctrica, y el pH del agua hace que tenga carga, entonces no se extraerá tan bien. Pero si el pH se ajusta para que no tenga carga, se extraerá mucho mejor.
¿Qué líquidos se usan para extraer?
Para la extracción líquido-líquido, siempre se usan dos líquidos que no se mezclan. Uno de ellos suele ser agua o una solución acuosa (con agua), y el otro es un líquido orgánico que no se mezcla bien con el agua.
Para elegir los líquidos, se consideran varias cosas:
- El líquido orgánico no debe mezclarse con el agua.
- La sustancia que queremos extraer debe disolverse mucho mejor en el líquido orgánico que en el agua.
- Los demás componentes de la mezcla no deben disolverse en el líquido orgánico.
- Es bueno que el líquido orgánico tenga un punto de ebullición bajo. Así, una vez que se extrae la sustancia, se puede calentar el líquido para que se evapore y dejar la sustancia pura.
- El líquido no debe reaccionar con la sustancia que se quiere extraer.
Es importante saber que muchos líquidos orgánicos son inflamables. Algunos también pueden ser tóxicos, por lo que siempre se deben usar con cuidado y siguiendo las normas de seguridad.
| Nombre | Densidad (g/ml) | Solubilidad en agua (g/100 ml) | P. ebullición (ºC) | Observaciones |
|---|---|---|---|---|
| Acetato de etilo | 0,90 | 8,0 | 78 | Inflamable, irritante |
| Benceno | 0,88 | 0,5 | 80 | Inflamable, tóxico |
| Ciclohexano | 0,78 | 0,001 | 81 | Inflamable |
| Cloroformo | 1,49 | 0,5 | 61 | Tóxico |
| Diclorometano | 1,33 | 2,0 | 61 | Tóxico |
| Éter etílico | 0,71 | 6,0 | 35 | Extremadamente inflamable |
| Hexano | 0,66 | 0,0001 | 60 | Inflamable |
| Pentano | 0,626 | 0,04 | 36 | Inflamable |
| Tolueno | 0,9 | 0,05 | 111 | Inflamable |
| Tetracloruro de carbono | 1,59 | 0,025 | 77 | Tóxico |
¿Cómo se realiza la extracción?
La extracción líquido-líquido se puede hacer en un laboratorio a pequeña escala o en grandes fábricas. El principio es el mismo en ambos casos.
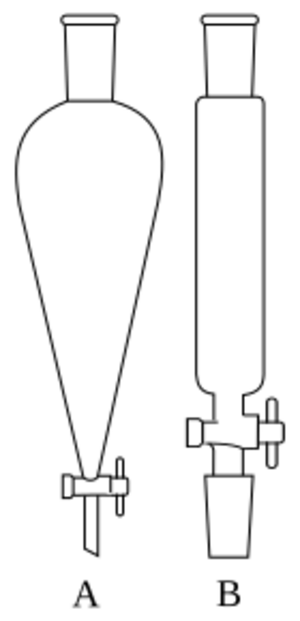
En el laboratorio, se usa un recipiente especial llamado embudo de decantación. Se vierte el líquido que contiene la sustancia y luego el líquido extractor. Después, se cierra el embudo y se agita con fuerza para que los dos líquidos se mezclen bien y la sustancia pueda pasar de uno a otro.
Después de agitar, se deja reposar el embudo. Los dos líquidos se separarán en capas, y la sustancia que queremos estará ahora en el líquido extractor.
Extracción simple
Si la sustancia se disuelve mucho, mucho mejor en el líquido extractor (es decir, si la KD o D es muy alta), a veces basta con una sola extracción para separar casi toda la sustancia.
Extracción repetitiva
En la práctica, casi nunca se extrae el 100% de la sustancia en un solo intento. Por eso, es mejor hacer varias extracciones seguidas. Esto significa usar varias porciones pequeñas del líquido extractor, una tras otra. Cada vez, se agita, se separan los líquidos y se junta la parte que contiene la sustancia. Al final, se habrán recogido la mayor parte de la sustancia.
¿Para qué se usa la extracción líquido-líquido?
Esta técnica es muy importante en la industria y en los laboratorios.
Usos en la industria
La extracción líquido-líquido se usa en muchas industrias, por ejemplo:
- En la industria del petróleo, para separar diferentes tipos de hidrocarburos.
- En la industria bioquímica, para separar antibióticos o recuperar proteínas.
- Para recuperar metales poco comunes o isótopos radiactivos.
- Para limpiar el agua de fábricas, eliminando sustancias como fenol o ácido fórmico que podrían dañar ríos y lagos.
Usos en el laboratorio
En los laboratorios, la extracción líquido-líquido se usa para:
- Purificar sustancias cuando se están creando nuevas en un proceso de síntesis química.
- Eliminar sustancias que podrían interferir en un análisis químico, para que los resultados sean más precisos.
Galería de imágenes
Véase también
 En inglés: Liquid–liquid extraction Facts for Kids
En inglés: Liquid–liquid extraction Facts for Kids