Ácido bromoso para niños
Datos para niños
Ácido bromoso |
||
|---|---|---|
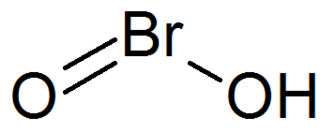 |
||
| Nombre IUPAC | ||
| Dioxobromato (III) de hidrógeno hidróxidoóxidobromo hidroxi-Λ3-bromanona |
||
| General | ||
| Otros nombres | Ácido dioxobrómico (III) | |
| Fórmula semidesarrollada | HBrO2 | |
| Fórmula estructural | HOBrO | |
| Fórmula molecular | ? | |
| Identificadores | ||
| ChEBI | 29247 | |
| ChemSpider | 145144 | |
| PubChem | 165616 | |
|
InChI
InChI=InChI=1S/BrHO2/c2-1-3/h(H,2,3)
Key: DKSMCEUSSQTGBK-UHFFFAOYSA-N |
||
| Propiedades físicas | ||
| Masa molar | 112,911 g/mol | |
| Compuestos relacionados | ||
| Ácidos de bromo | ácido bromhídrico ácido hipobromoso ácido brómico ácido perbrómico |
|
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. |
||
El ácido bromoso, con la fórmula química HBrO2, es un compuesto que contiene el elemento bromo. En este compuesto, el bromo tiene un "estado de oxidación" de +3, lo que indica cómo se comparten sus electrones en la molécula.
Este ácido no es muy estable, lo que significa que no dura mucho tiempo por sí solo. Generalmente, aparece como un "compuesto intermedio" en algunas reacciones químicas. Por ejemplo, se forma durante la oxidación de otras sustancias llamadas hipobromitos. También es importante en una reacción química especial conocida como la reacción de Belousov-Zhabotinskii.
Contenido
Ácido Bromoso: Un Compuesto Químico Especial
¿Qué es el Ácido Bromoso?
El ácido bromoso es un tipo de ácido que contiene bromo, hidrógeno y oxígeno. Su fórmula, HBrO2, nos dice que cada molécula tiene un átomo de hidrógeno, uno de bromo y dos de oxígeno. A diferencia de otros ácidos, el ácido bromoso es bastante inestable y se descompone rápidamente.
Las sales que se forman a partir del ácido bromoso se llaman bromitos. Algunos bromitos son más estables que el propio ácido y pueden ser aislados y estudiados.
¿Cómo se Forma el Ácido Bromoso?
El ácido bromoso se puede obtener de varias maneras en el laboratorio, aunque siempre como un compuesto que existe por poco tiempo.
Reacciones para Obtenerlo
Una forma de producir ácido bromoso es combinando ácido hipobromoso con ácido hipocloroso. Esta es una reacción química clásica:
- HBrO + HClO → HBrO2 + HCl
También se puede formar a partir de una reacción llamada "dismutación" del ácido hipobromoso. En este tipo de reacción, una misma sustancia se transforma para formar dos productos diferentes:
- 2 HBrO → HBrO2 + HBr
Finalmente, el ácido bromoso puede obtenerse mediante una reacción de "comproporción". Esto ocurre cuando dos compuestos que contienen el mismo elemento (en este caso, bromo) pero en diferentes estados de oxidación, reaccionan para formar un nuevo compuesto con un estado de oxidación intermedio. En este caso, el ácido brómico y el ácido bromhídrico reaccionan para formar ácido bromoso:
- 2 HBrO3 + HBr → 3 HBrO2
Sales del Ácido Bromoso: Los Bromitos
Aunque el ácido bromoso es inestable, algunas de sus sales, los bromitos, sí son estables y se pueden obtener. Por ejemplo, se han logrado aislar el bromito de sodio trihidratado (NaBrO2·3H2O) y el bromito de bario monohidratado (Ba(BrO2)2·H2O). Estas sales son importantes porque nos permiten estudiar las propiedades del bromo en este estado de oxidación.
¿Para Qué Sirve el Ácido Bromoso?
El ácido bromoso y sus sales, los bromitos, pueden participar en reacciones químicas importantes.
Reacciones Importantes
Una de las propiedades químicas del ácido bromoso y los bromitos es su capacidad para reducir otras sustancias. Por ejemplo, pueden reducir los permanganatos a manganatos. Esto significa que les "quitan" oxígeno o electrones a otras moléculas en una reacción de reducción-oxidación.
- 2MnO−
4 + BrO−
2 + OH− → 2MnO2−
4 + BrO−
3 + H2O
Además, el ácido bromoso reacciona con los bromuros en un ambiente ácido para formar bromo elemental. Esta reacción es un ejemplo de cómo el ácido bromoso puede transformarse en otras formas de bromo.
- HBrO2 + 3 Br− + 3 H+ → 2 Br2 + 2 H2O
Véase también
 En inglés: Bromous acid Facts for Kids
En inglés: Bromous acid Facts for Kids
- Bromito

