Permanganato para niños
Los permanganatos son un tipo de compuestos químicos que se forman a partir de un ácido llamado ácido permangánico. Su fórmula es HMnO4. Son sustancias de un color violeta muy intenso y tienen una gran capacidad para reaccionar con otras sustancias, quitándoles electrones. Esto se conoce como ser un agente oxidante.
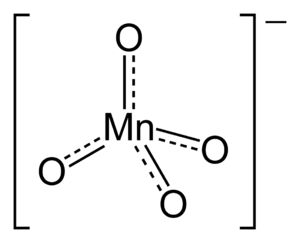
Los permanganatos contienen una parte especial llamada anión permanganato, que se escribe MnO4–. En este anión, el elemento manganeso (Mn) se encuentra en su estado de oxidación más alto, que es +7.
Contenido
¿Cómo reaccionan los permanganatos?
El anión permanganato es un oxidante muy potente. Esto significa que puede quitar electrones a otras sustancias con mucha facilidad. Incluso puede reaccionar con el agua, liberando oxígeno.
Reacciones con el agua
Aunque el permanganato es un oxidante fuerte, su reacción con el agua es bastante lenta. Esto es especialmente cierto si no hay luz y si el ambiente no es ni muy ácido ni muy básico. Sin embargo, si la disolución es ácida, la reacción es más notoria, aunque sigue siendo lenta. Si se calienta la mezcla, la reacción se acelera. Por ejemplo, al calentar permanganato en una disolución básica, se libera oxígeno y se forma otro compuesto llamado manganato, que es de color verde.
Reacciones con sustancias orgánicas
Cuando el permanganato entra en contacto con algunas sustancias orgánicas, puede provocar reacciones que liberan mucho calor. Esto puede incluso causar incendios. Por ejemplo, si se pone una gota de glicerina sobre un poco de permanganato de potasio en polvo, rápidamente se verá humo y luego una llama de color violeta.
¿Qué ocurre cuando el permanganato se reduce?
Cuando el permanganato reacciona y se reduce (es decir, gana electrones), el manganeso cambia de estado.
- En una disolución ácida, el manganeso suele terminar en el estado de oxidación +2. En este caso, la disolución se vuelve casi transparente o de un rosa muy pálido. Esta reacción se acelera si ya hay manganeso(II) presente.
- En una disolución neutra o ligeramente básica, el manganeso se reduce a óxido de manganeso(IV), que es un sólido de color marrón que se precipita (se asienta en el fondo).
- Si la disolución es muy básica, el permanganato se reduce a manganato, que es de color verde.
¿Cómo se obtienen los permanganatos?
El permanganato más conocido es el permanganato de potasio, cuya fórmula es KMnO4. Se puede obtener de varias maneras, como mediante un proceso llamado electrólisis o a partir de una disolución de manganato de potasio en un ambiente ácido.
¿Para qué se usan los permanganatos?
El permanganato de potasio se usa en la industria como un agente oxidante en diferentes procesos. Por ejemplo, se utiliza para transformar ciertas partes de moléculas en la fabricación de la sacarina, un edulcorante.
También se usa en el tratamiento de aguas. A veces se añade permanganato al agua para ayudar a limpiarla, eliminando sustancias orgánicas y ayudando a que las partículas pequeñas se unan y se asienten. En medicina, una disolución muy diluida de permanganato se usa a veces como desinfectante para la boca.
Consejos útiles
Las manchas que deja el permanganato suelen ser de óxidos de manganeso. Se pueden quitar fácilmente con disoluciones ligeramente ácidas de sulfito o tiosulfato. Sin embargo, estas sustancias pueden dejar manchas amarillas en los tejidos si se exponen al sol. Por eso, a menudo se prefiere usar ácido oxálico para limpiar estas manchas.
¿Por qué el permanganato es violeta?
El color violeta tan intenso del permanganato se debe a un fenómeno llamado "transferencia de carga". Esto significa que los electrones se mueven entre los átomos de oxígeno y el átomo central de manganeso, lo que hace que absorba y refleje la luz de una manera que vemos como color violeta.
El ácido oxálico, mencionado antes para quitar manchas, es una sustancia que puede reducir el permanganato y neutralizar los óxidos de manganeso que causan las manchas.
Véase también
 En inglés: Permanganate Facts for Kids
En inglés: Permanganate Facts for Kids