Sulfóxido para niños
Un sulfóxido es un tipo de compuesto químico. Imagina que es como un "primo" de los tioéteres, pero con un átomo de oxígeno extra unido a su átomo de azufre. Se puede decir que tienen un grupo especial llamado "sulfinilo" que conecta el azufre con otros dos átomos de carbono.
Un ejemplo natural de sulfóxido es la aliina, que se encuentra en el ajo. ¡Sí, el mismo ajo que usas para cocinar!
Contenido
Sulfóxidos: Compuestos Químicos Interesantes
¿Qué son los Sulfóxidos?
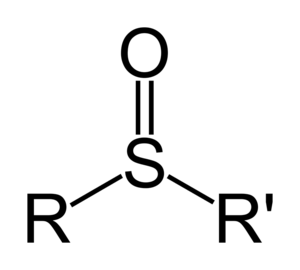
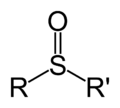
Los sulfóxidos se representan con una fórmula como R-S(=O)-R'. Aquí, la "R" y la "R'" son grupos de átomos que contienen carbono. El enlace entre el azufre (S) y el oxígeno (O) es un poco diferente a otros enlaces dobles que quizás conozcas, como los que se ven en las cetonas.
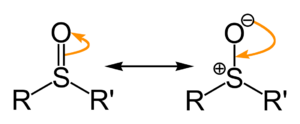
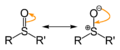
Este enlace entre el azufre y el oxígeno tiene una característica especial: es como si el oxígeno atrajera más los electrones, creando una pequeña carga negativa en el oxígeno y una positiva en el azufre. Esto hace que la molécula tenga un "lado" positivo y un "lado" negativo, como un pequeño imán.
La Estructura Especial de los Sulfóxidos
El átomo de azufre en un sulfóxido tiene un par de electrones que no están compartidos con otros átomos. Este par de electrones, junto con los dos grupos orgánicos (R y R') y el oxígeno, le dan al azufre una forma especial en el espacio, parecida a una pirámide con cuatro caras (llamada tetraédrica).
¿Por qué son Especiales Algunos Sulfóxidos?
Si los dos grupos orgánicos (R y R') unidos al azufre son diferentes, el átomo de azufre se convierte en lo que llamamos un "centro quiral". Esto significa que la molécula puede existir en dos formas que son como imágenes espejo una de la otra, ¡igual que tu mano izquierda y tu mano derecha! Un ejemplo es el metilfenilsulfóxido.
Si los dos grupos (R y R') son iguales, como en el dimetilsulfóxido (conocido como DMSO), la molécula es simétrica y no es quiral.
La energía necesaria para que estas formas "espejo" se conviertan una en la otra es bastante alta. Por eso, los sulfóxidos quirales pueden ser "ópticamente activos", lo que significa que pueden interactuar de una manera especial con la luz. Esto los hace útiles en la creación de ciertos medicamentos y como herramientas en la química.
¿Cómo se Forman los Sulfóxidos?
Los sulfóxidos se pueden obtener a partir de otros compuestos llamados sulfuros, mediante un proceso llamado oxidación. Es como añadirles oxígeno. Si se añade aún más oxígeno, los sulfóxidos pueden convertirse en otro tipo de compuestos llamados sulfonas.
Por ejemplo, el sulfuro de dimetilo puede oxidarse para formar dimetilsulfóxido, y luego, si se oxida de nuevo, se convierte en dimetilsulfona.
Los peróxidos son un tipo de sustancia que se usa comúnmente para oxidar los sulfuros y convertirlos en sulfóxidos.
Galería de imágenes
Véase también
 En inglés: Sulfoxide Facts for Kids
En inglés: Sulfoxide Facts for Kids