Estereoquímica para niños
La estereoquímica es una parte de la química que estudia cómo se organizan los átomos en el espacio dentro de las moléculas. También investiga cómo esta organización afecta las características y la forma en que reaccionan esas moléculas.
Imagina que las moléculas son como piezas de un rompecabezas. A veces, puedes tener las mismas piezas (los mismos átomos), pero si las conectas de una manera diferente o las giras en el espacio, obtendrás formas distintas. Estas formas diferentes se llaman isómeros. La estereoquímica se encarga de entender estas diferencias espaciales.
Aunque las moléculas tengan la misma fórmula, si sus átomos están acomodados de forma diferente en el espacio, pueden tener propiedades muy distintas. Esto es importante en muchas áreas de la química, como la química orgánica, la biología y la química de polímeros. El estudio de la estereoquímica fue un gran avance porque ayudó a explicar por qué existen diferentes tipos de isómeros y llevó a los científicos a entender que el átomo de carbono tiene una forma especial, como un tetraedro (una pirámide de cuatro caras).
Contenido
Historia de la Estereoquímica
Primeros Descubrimientos y la Luz Polarizada
La historia de la estereoquímica comenzó en 1815, cuando Jean-Baptiste Biot notó que algunas moléculas podían girar el plano de la luz polarizada. Imagina la luz como ondas que vibran en todas direcciones. La luz polarizada es luz que solo vibra en una dirección. Biot descubrió que ciertas sustancias podían hacer que esa dirección de vibración girara.
Sin embargo, a Louis Pasteur se le considera el primer estereoquímico. En 1849, mientras trabajaba con sales de ácido tartárico (que se encuentran en el vino), Pasteur observó algo sorprendente. Encontró dos tipos de cristales de esta sal. Unos giraban la luz polarizada en una dirección (como las manecillas del reloj) y otros la giraban en la dirección opuesta. Lo más curioso es que ambos tipos de cristales tenían las mismas propiedades físicas y químicas, ¡excepto por cómo interactuaban con la luz polarizada! Esto demostró que, aunque parecieran iguales, había una diferencia sutil en su estructura espacial.
El Átomo de Carbono Tetraédrico
En 1874, dos científicos, Jacobus Henricus van 't Hoff y Joseph Le Bel, explicaron el descubrimiento de Pasteur. Propusieron que la capacidad de estas moléculas para girar la luz se debía a la forma en que los átomos estaban unidos al carbono. Dijeron que el átomo de carbono se une a otros cuatro átomos de una manera que forma una figura de cuatro lados, como una pirámide (un tetraedro). Esta forma tetraédrica permite que existan moléculas que son como "imágenes especulares" una de la otra, como tu mano izquierda y tu mano derecha.
Más tarde, en 1904, Lord Kelvin introdujo el término "quiral" para describir estas moléculas que son imágenes especulares no superponibles. Es como si una molécula fuera la mano izquierda y la otra, la mano derecha: son iguales, pero no puedes superponerlas perfectamente.
Tipos de Isómeros
Para entender mejor la estereoquímica, es útil conocer los diferentes tipos de Isómeros:
- Isómeros estructurales: Son moléculas que tienen la misma fórmula química (los mismos átomos), pero sus átomos están conectados de un orden diferente. Por ejemplo, el alcohol y el éter pueden tener la misma cantidad de átomos de carbono, hidrógeno y oxígeno, pero están unidos de forma distinta.
- Estereoisómeros: Son moléculas que tienen los mismos átomos conectados en el mismo orden, pero se diferencian en cómo están orientados en el espacio. Es como si tuvieras el mismo collar de perlas, pero las perlas estuvieran giradas de una forma u otra.
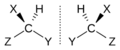
- Enantiómeros: Son un tipo especial de estereoisómeros que son imágenes especulares no superponibles entre sí. Piensa en tus manos: son imágenes especulares, pero no puedes poner una encima de la otra y que coincidan perfectamente.
- Diasteroisómeros: Son estereoisómeros que no son imágenes especulares entre sí. Son diferentes en su orientación espacial, pero no son "reflejos" uno del otro.
Cómo Representar Moléculas en 3D
Para estudiar las moléculas en 3D, los químicos usan diferentes formas de dibujarlas en papel:
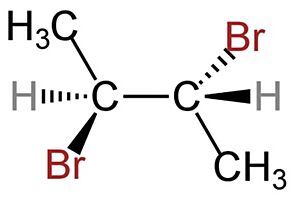
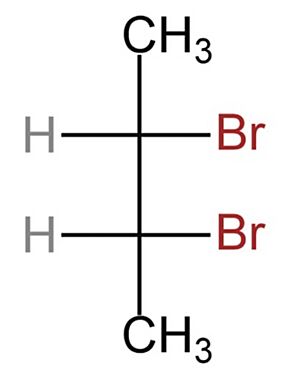
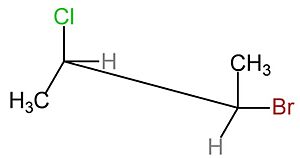
- Diagramas de cuñas y rayas: Estos dibujos nos ayudan a ver las moléculas en tres dimensiones. Las líneas normales muestran enlaces que están en el mismo plano que el papel. Las cuñas punteadas indican enlaces que se alejan de ti (hacia atrás del papel), y las cuñas oscuras y sombreadas muestran enlaces que se acercan a ti (hacia adelante del papel).
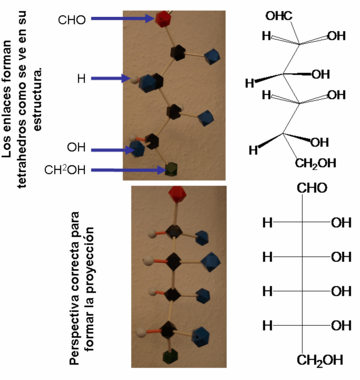
- Proyecciones de Fischer: Son una forma más sencilla de dibujar moléculas 3D en un plano. Todos los enlaces se dibujan como líneas que se cruzan en ángulos de 90 grados. Las líneas verticales representan enlaces que van hacia atrás y hacia adelante, y las líneas horizontales representan enlaces que salen hacia los lados.
- Proyecciones de caballete: Estas proyecciones muestran la molécula desde un ángulo, como si la estuvieras viendo de lado. Ayudan a entender cómo giran las partes de una molécula alrededor de un enlace.
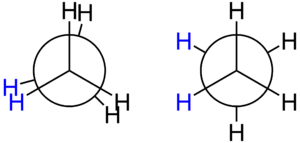
- Proyecciones de Newman: Se usan para ver una molécula mirando directamente a lo largo de un enlace entre dos átomos de carbono. El carbono más cercano se representa como un punto en el centro de un círculo, y el carbono de atrás se representa como el círculo mismo. Los átomos unidos a cada carbono se dibujan saliendo de estos puntos.
Importancia de la Estereoquímica en la Vida Real
La estereoquímica es muy importante en muchos campos, especialmente en la fabricación de materiales y en la medicina.
En Materiales
Por ejemplo, el caucho natural (el que viene de los árboles) está hecho de unidades repetitivas de una molécula llamada cis-poliisopreno. El caucho sintético, en cambio, puede tener unidades de trans-poliisopreno o una mezcla. Aunque son muy parecidos, la forma en que sus unidades están organizadas en el espacio hace que el caucho natural sea mucho más elástico y resistente que el sintético.
Otros materiales como el poliestireno y el polipropileno también mejoran sus propiedades físicas (como su resistencia) cuando sus moléculas están organizadas de una forma espacial específica.
En Medicina
Uno de los ejemplos más conocidos de la importancia de la estereoquímica en la medicina es el caso de la talidomida. Este medicamento fue creado en 1957 en Alemania y se recetaba a mujeres embarazadas para aliviar las náuseas matutinas. Sin embargo, se descubrió que causaba problemas graves en los bebés.
Después de mucha investigación, se encontró que la talidomida existía en dos formas, como dos enantiómeros (imágenes especulares). Una de estas formas era segura y ayudaba con las náuseas (la forma R), pero la otra forma (la forma S) causaba problemas en el desarrollo de los bebés. El cuerpo humano, al tomar el medicamento, podía transformar la forma segura en la forma dañina.
Este trágico evento enseñó a los científicos la importancia vital de la estereoquímica en la creación de medicamentos. Ahora, antes de aprobar un fármaco, se estudia muy cuidadosamente cómo sus diferentes formas espaciales pueden afectar al cuerpo. Un pequeño cambio en la orientación de los átomos puede hacer que un compuesto sea beneficioso o, por el contrario, muy peligroso.
Galería de imágenes
Véase también
 En inglés: Stereochemistry Facts for Kids
En inglés: Stereochemistry Facts for Kids
- Aquiralidad
- Isomería cis-trans
- Nomenclatura D-L
- Pasteur
- Reglas de Cahn-Ingold-Prelog