Éter (química) para niños
Contenido
¿Qué son los Éteres?
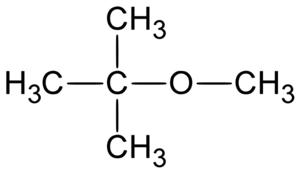
En el mundo de la química orgánica, un éter es un tipo de compuesto químico donde un átomo de oxígeno está unido a dos grupos de átomos, que pueden ser iguales o diferentes. Estos grupos suelen ser cadenas de carbono e hidrógeno. Imagina el oxígeno como un puente que conecta dos partes de una molécula.
Los éteres son muy comunes en la química y también en la bioquímica, que es la química de los seres vivos. Por ejemplo, son enlaces importantes en los carbohidratos (como los azúcares) y en la lignina, una sustancia que da rigidez a las plantas.
¿Cómo se forman los Éteres?
Los éteres se pueden obtener de varias maneras en el laboratorio. Una forma es a partir de dos alcoholes, aunque esto no se hace directamente. En su lugar, se usan pasos intermedios.
Una forma común de crear éteres es la síntesis de Williamson. En este método, se hace reaccionar un tipo de alcohol con otra sustancia para formar el éter deseado.
También se pueden formar éteres por la deshidratación de alcoholes. Esto significa quitar una molécula de agua de dos moléculas de alcohol, generalmente a altas temperaturas y con la ayuda de un ácido.
Tipos de Éteres
Los éteres se pueden clasificar según los grupos de átomos que están unidos al oxígeno:
- Si los dos grupos son iguales, se les llama éteres simples o simétricos.
- Si los dos grupos son diferentes, se les llama éteres mixtos o asimétricos.
Éter Dietílico: Un Ejemplo Importante
El éter dietílico (también conocido como etoxietano) es un éter muy conocido. Durante mucho tiempo, se le llamó simplemente "éter". Fue descubierto por el alquimista Raymundus Lullis en 1275 y sintetizado por primera vez por Valerius Cordus en 1540. En 1842, Crawford Williamson Long lo usó por primera vez como anestesia en medicina.
Éteres Corona: Moléculas Especiales
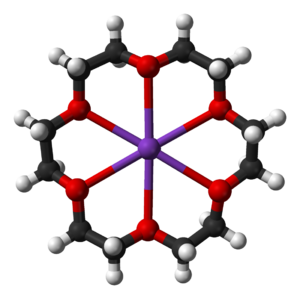
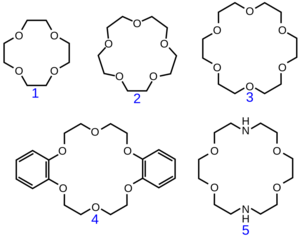
Los éteres corona son un tipo especial de éteres que tienen varios átomos de oxígeno en su estructura y forman un ciclo, como una corona. El nombre de un éter corona nos dice cuántos átomos tiene el ciclo y cuántos de ellos son oxígeno. Por ejemplo, "18-corona-6" significa que tiene un ciclo de 18 átomos, y 6 de ellos son oxígeno.
Estos compuestos son interesantes porque pueden atrapar iones (átomos con carga eléctrica) en su centro. Esto les permite ayudar a disolver sustancias que normalmente no se mezclarían. En los seres vivos, los éteres corona pueden ayudar a transportar iones a través de las membranas de las células.
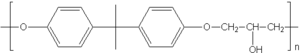
Poliéteres: Cadenas Largas
Los poliéteres son polímeros, es decir, moléculas muy grandes formadas por la repetición de unidades más pequeñas, que contienen enlaces éter en su cadena principal. Un ejemplo muy conocido son las resinas epoxi, que se usan como adhesivos muy fuertes.
Los epóxidos (o oxiranos) son un tipo de éter donde el oxígeno forma parte de un ciclo de tres átomos. Debido a la tensión en este pequeño ciclo, los epóxidos son más reactivos que otros éteres.
Nomenclatura: ¿Cómo se nombran?
Para nombrar los éteres, los químicos siguen reglas específicas. La forma más moderna, según la IUPAC (la organización que establece las reglas de nomenclatura química), es nombrarlos como alcoxialcanos. Esto significa que se considera que el grupo éter es un "sustituyente" en una cadena más larga. Por ejemplo, CH3-O-C6H5 se llama metoxibenceno.
También existe una forma tradicional de nombrarlos, que es nombrar los dos grupos unidos al oxígeno en orden alfabético, seguidos de la palabra "éter". Por ejemplo, el compuesto anterior se llamaría fenil metil éter.
Reacciones de los Éteres
Los éteres simples son bastante estables y no reaccionan fácilmente. Sus enlaces carbono-oxígeno son fuertes. Sin embargo, pueden reaccionar con ácidos muy fuertes, como el ácido yodhídrico, especialmente si se calientan.
Formación de Peróxidos
Una característica importante de algunos éteres es que, si se guardan en presencia de aire u oxígeno, pueden formar sustancias llamadas peróxidos. Estos peróxidos pueden ser peligrosos porque son explosivos. Por eso, es muy importante manipular y almacenar los éteres con cuidado en los laboratorios. Se recomienda no destilarlos completamente, ya que los peróxidos se concentran en el líquido restante.
Usos de los Éteres
Los éteres tienen varios usos importantes:
- Se usan como disolventes para muchas sustancias orgánicas, como aceites, grasas, resinas y perfumes.
- Pueden servir como combustible inicial en algunos motores diésel.
- Se emplean en la fabricación de pegamentos fuertes.
- Históricamente, algunos se usaron como anestesia.
Galería de imágenes
Véase también
 En inglés: Diethyl ether Facts for Kids
En inglés: Diethyl ether Facts for Kids
- Éster
- Dibutil éter