Disolución acuosa para niños
Una disolución acuosa es una mezcla especial donde una o más sustancias se disuelven en agua. Imagina que el agua es como un "disolvente" que ayuda a que otras cosas se mezclen con ella.
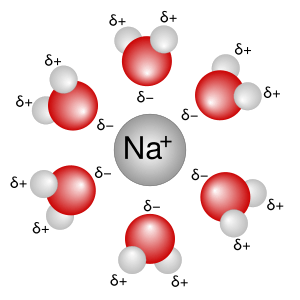
En química, cuando vemos una fórmula como NaCl(aq), la parte "(aq)" nos dice que la sal común (cloruro de sodio) está disuelta en agua. La palabra acuoso viene del latín aqua, que significa agua.
El agua es un disolvente muy importante porque puede disolver muchas cosas y es muy abundante en la naturaleza. Por eso, cuando hablamos de una "disolución" en química, casi siempre nos referimos a una disolución acuosa, a menos que se diga lo contrario.
También existen las disoluciones "no acuosas", que son aquellas donde el disolvente es otro líquido diferente al agua.
Contenido
¿Qué hace que una sustancia se disuelva en agua?
Algunas sustancias se disuelven muy bien en agua, mientras que otras no.
- Las sustancias que se disuelven fácilmente en agua se llaman hidrofílicas. Un buen ejemplo es la sal de mesa.
- Las sustancias que no se disuelven bien en agua se llaman hidrofóbicas. Piensa en el aceite, que no se mezcla con el agua.
En una disolución acuosa, las moléculas de agua pueden separarse en pequeñas partes llamadas iones de hidrógeno (H+) y iones hidróxido (OH-). Estos iones están en un equilibrio constante.
¿Cómo se comportan los ácidos y las bases en el agua?
Los ácidos y las bases son tipos de disoluciones acuosas.
- Un ácido, como el cloruro de hidrógeno (HCl), libera iones de hidrógeno (H+) cuando se disuelve en agua.
- Una base, como el hidróxido de sodio (NaOH), libera iones hidróxido (OH-) cuando se disuelve en agua.
¿Qué son los electrolitos en las disoluciones acuosas?
Las disoluciones acuosas pueden conducir la corriente eléctrica. La forma en que lo hacen depende de si contienen electrolitos fuertes o débiles.
- Electrolitos fuertes: Son sustancias que se separan completamente en iones cuando se disuelven en agua. Estos iones pueden moverse libremente y permiten que la electricidad pase muy bien.
- Electrolitos débiles: Son sustancias que solo se separan un poco en iones cuando se disuelven en agua. Por eso, no conducen la electricidad tan bien.
Algunas sustancias se disuelven en agua pero no se separan en iones; estas se llaman no electrolitos. Ejemplos de no electrolitos son el azúcar y la urea.
¿Cómo ocurren las reacciones en disoluciones acuosas?
Muchas reacciones químicas que ocurren en disoluciones acuosas son de un tipo llamado reacciones de metátesis. Esto significa que las partes de dos compuestos se intercambian. Es como si dos parejas de baile cambiaran de compañero.
¿Qué es una reacción de precipitación?
Una reacción de metátesis muy común en disoluciones acuosas es la reacción de precipitación. Esto sucede cuando mezclas dos disoluciones acuosas y se forma un sólido que no se disuelve. Este sólido se llama precipitado.
Para que una sustancia se disuelva en agua, debe ser capaz de superar las fuerzas que mantienen unidas a las moléculas de agua. Si no puede, entonces las moléculas de la sustancia se agrupan y forman un precipitado.
Cuando los científicos escriben las ecuaciones de estas reacciones, necesitan saber qué sustancia formará el precipitado. Para esto, usan una tabla de solubilidad, que les dice qué compuestos se disuelven en agua (son acuosos) y cuáles no (son el precipitado). A veces, no se forma ningún precipitado.
Para entender bien estas reacciones, es importante conocer la cantidad de sustancia disuelta en el agua, lo que se llama concentración o molaridad.
Galería de imágenes
Véase también
 En inglés: Aqueous solution Facts for Kids
En inglés: Aqueous solution Facts for Kids