Pila de combustible para niños
Una pila de combustible, también conocida como celda de combustible, es un aparato especial que transforma la energía química de un combustible y un oxidante en electricidad. Imagina que es como una batería, pero con una diferencia clave: una pila de combustible recibe combustible y aire de forma continua, lo que le permite producir electricidad sin parar, a diferencia de una batería que se agota.
En una pila de combustible, los materiales que reaccionan (llamados electrodos) no se gastan como en una batería. En cambio, actúan como catalizadores, que son sustancias que aceleran las reacciones químicas sin consumirse. Este proceso es muy eficiente y ayuda a cuidar el medio ambiente, ya que no produce mucha contaminación. Las pilas de combustible pueden tener una eficiencia energética de entre el 40% y el 60%, y si se aprovecha el calor que generan (en un proceso llamado cogeneración), ¡pueden llegar hasta el 85-90%!
Las pilas de combustible pueden usar diferentes tipos de combustibles, como hidrógeno, y un oxidante, que suele ser oxígeno del aire. Una de sus primeras aplicaciones importantes fue en las naves espaciales. Allí, usaban hidrógeno y oxígeno para producir electricidad y, como resultado, ¡agua que los astronautas podían beber o usar para enfriar los sistemas de la nave!
El mercado de las pilas de combustible está creciendo. Se espera que en el futuro se usen mucho en casas y vehículos. Por ejemplo, la empresa japonesa Honda ha desarrollado un coche que funciona con este sistema, el FCX Clarity, y también un sistema para el hogar que produce hidrógeno a partir de gas natural para recargar el coche y, al mismo tiempo, genera electricidad y agua caliente para la casa.
Contenido
- Historia de las Pilas de Combustible
- ¿Cómo Funcionan las Pilas de Combustible?
- Partes de un Sistema de Pilas de Combustible
- Tipos de Pilas de Combustible
- Pila de Combustible de Membrana de Intercambio Protónico (PEM)
- Pila de Combustible de Metanol Directo (DMFC)
- Celdas de Combustible Alcalinas (AFC)
- Pila de Combustible de Ácido Fosfórico (PAFC)
- Pila de Combustible de Carbonato Fundido (MCFC)
- Pila de Combustible de Óxido Sólido (SOFC)
- Comparación de Tipos de Pilas de Combustible
- Otros Tipos de Pilas de Combustible
- Comportamiento de las Pilas de Combustible
- Usos de las Celdas de Combustible
- Economía y Medio Ambiente
- Glosario de Términos
- Véase también
Historia de las Pilas de Combustible
Aunque parezca una tecnología nueva, la historia de las pilas de combustible empezó hace casi 200 años. En 1838, el científico Christian Friedrich Schönbein en Suiza y el físico William Robert Grove en Gales comenzaron a investigar sobre ellas. Grove publicó sus hallazgos en 1843.
Hoy en día, estas celdas se usan en muchos lugares: desde aparatos pequeños como teléfonos móviles, hasta sistemas grandes para generar energía en edificios o para mover vehículos como submarinos y coches. Sin embargo, su desarrollo ha tenido altibajos. El interés por ellas ha aumentado en momentos de escasez de energía, como durante la crisis del petróleo de 1973, porque son más eficientes y necesitan menos combustible para producir la misma cantidad de energía.
Primeros Pasos (1843)
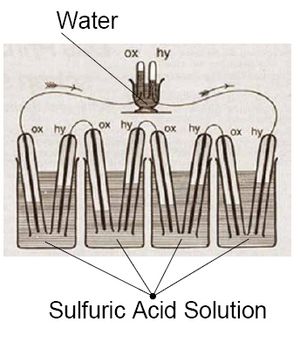
En 1843, William Robert Grove presentó su dispositivo. Usó dos electrodos de platino sumergidos en ácido sulfúrico, a los que les suministraba oxígeno e hidrógeno. Conectó cincuenta de estas celdas para generar suficiente electricidad.
Avances a Finales del Siglo XIX (1882-1889)
En 1882, el físico británico Lord Rayleigh mejoró el diseño de Grove, haciendo las celdas más eficientes.
En 1889, Ludwig Mond y Charles Langer usaron por primera vez el término "pila de combustible". Ellos lograron un gran avance al crear un prototipo que mantenía el electrolito (la sustancia que conduce la electricidad) en una matriz sólida, lo que facilitaba que los gases llegaran a los puntos donde ocurrían las reacciones.
Desarrollo Moderno (1950 y 1960)
A mediados del siglo XX, la tecnología de las pilas de combustible avanzó mucho. En 1954, el científico inglés Francis Thomas Bacon construyó una planta de energía de 5 kW con una pila de combustible alcalina. Esta pila usaba hidrógeno y oxígeno y podía hacer funcionar una máquina de soldar.
En los años 60, las ideas de Bacon se usaron en el programa espacial de Estados Unidos para dar electricidad y agua potable a los astronautas, aprovechando el hidrógeno y el oxígeno de los tanques de la nave.
En 1959, un equipo liderado por Harry Ihrig construyó un tractor de 15 kW que funcionaba con una pila de combustible. General Electric también desarrolló las primeras pilas de membrana de intercambio de protones (PEMFCs) para las misiones espaciales Gemini de la NASA.
Búsqueda de Alternativas (1970 y 1980)
Entre 1970 y 1980, debido a la crisis del petróleo, se investigó mucho para mejorar los materiales de las pilas de combustible, encontrar mejores fuentes de combustible y reducir sus costos.
En la década de 1980, se empezaron a probar las pilas de combustible en servicios públicos y en la fabricación de coches. En los años 90, se desarrollaron pilas de combustible grandes y fijas para edificios comerciales e industriales.
Hacia la Comercialización (1993-2013)
En 1993, la empresa canadiense Ballard desarrolló el primer vehículo comercial con pila de combustible usando tecnología PEM.
En 2007, las pilas de combustible comenzaron a venderse para usos fijos y auxiliares. En 2008, Honda empezó a vender su coche eléctrico FCX Clarity. Ese mismo año, el Premio Nobel de Química fue para Gerhard Ertl, cuyos estudios ayudaron a entender cómo funcionan estas pilas.
Panasonic fue la primera empresa en vender pilas de combustible para uso doméstico en Japón, vendiendo 31.000 unidades entre 2009 y 2013.
En 2013, la empresa británica "ACAL Energy" presentó una pila de combustible que podría ser más económica. Esta pila no usa platino como catalizador, sino un líquido especial, lo que reduce el costo y mejora su durabilidad.
¿Cómo Funcionan las Pilas de Combustible?
El funcionamiento de una pila de combustible es similar al de una batería, ya que ambas producen electricidad a partir de reacciones químicas. Sin embargo, la pila de combustible está diseñada para recibir combustible de forma continua, lo que le permite generar energía sin interrupción. Además, los electrodos en una pila de combustible no solo conducen la electricidad, sino que también actúan como catalizadores para las reacciones.
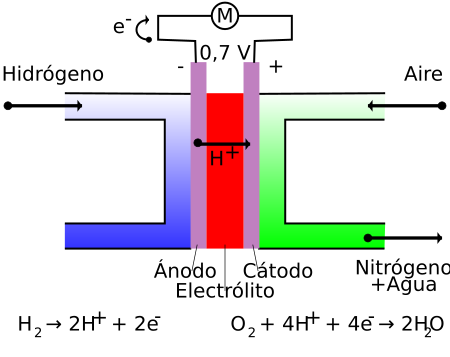
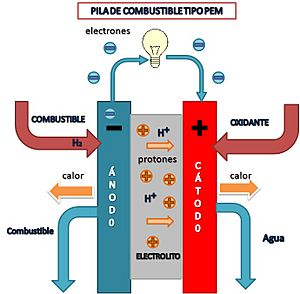
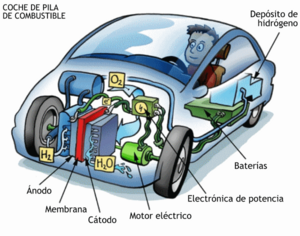
Para entender cómo funcionan, tomemos como ejemplo una de las más comunes: la pila de combustible de membrana de intercambio protónico (PEM). Esta pila tiene dos electrodos:
- El ánodo: donde el combustible (generalmente hidrógeno) se oxida.
- El cátodo: donde el oxidante (generalmente oxígeno) se reduce.
Entre el ánodo y el cátodo hay un electrolito, que es una membrana especial. Esta membrana es un aislante eléctrico (no deja pasar los electrones), pero sí permite el paso de los protones (partículas cargadas positivamente). Así, los electrones viajan desde el ánodo hasta el cátodo a través de un circuito externo, ¡generando la corriente eléctrica que usamos! Mientras tanto, los protones viajan a través del electrolito. En el cátodo, los electrones, protones y el oxígeno se unen para formar agua.
Para que los protones puedan pasar por la membrana, esta debe estar húmeda. Por eso, los gases que entran a la pila suelen humidificarse antes.
Además del hidrógeno puro, las pilas de combustible pueden usar hidrógeno que se encuentra en otras moléculas, como las del gas natural o el metanol. En estos casos, además de agua, también se produce dióxido de carbono.
Las pilas de combustible se pueden clasificar de varias maneras, por ejemplo, según el tipo de electrolito o el combustible que usan. La mayoría de las pilas en desarrollo hoy en día usan hidrógeno o gases ricos en hidrógeno, y oxígeno como oxidante. Una gran ventaja de usar hidrógeno y oxígeno es que el único producto de la reacción es agua, lo que las hace muy limpias.
Una sola pila de combustible produce menos de un voltio de electricidad. Por eso, para obtener la energía necesaria para la mayoría de las aplicaciones, se conectan varias pilas en serie, formando lo que se llama un "apilamiento" o "stack".
Voltaje
El voltaje de una celda individual es de aproximadamente 1.2 voltios cuando no hay corriente. Para obtener más voltaje, se agrupan muchas celdas en serie, formando un "apilamiento de células de combustible".
Materiales
Los materiales de las pilas de combustible varían según el tipo. Los electrodos suelen ser de nanotubos de metal, níquel o carbono, y a menudo están cubiertos por un catalizador como el platino o el paladio para mejorar su eficiencia. El electrolito puede ser de cerámica o una membrana especial hecha de polímeros.
Aspectos Clave en el Diseño
- Costos: El costo de los materiales, especialmente el catalizador de platino, ha sido un desafío. Sin embargo, se están investigando materiales más económicos para reducir el precio.
- Manejo del Agua: En las pilas PEM, la membrana debe mantenerse con la humedad justa. Si se seca demasiado, la pila puede dañarse. Si tiene demasiada agua, los gases no pueden llegar al catalizador.
- Control de Temperatura: Es importante mantener una temperatura constante en toda la pila para que funcione bien y no se dañe.
- Control de Flujo: La cantidad de combustible y oxígeno debe ser constante para que la pila funcione de manera eficiente.
- Durabilidad: Las pilas de combustible deben ser muy duraderas. Para coches, se espera que duren al menos 5.000 horas (unos 200.000 kilómetros) en diferentes temperaturas.
Partes de un Sistema de Pilas de Combustible
Un sistema de pilas de combustible tiene una "celda unitaria" como su parte más básica.
Celda Unitaria
Los elementos de una celda unitaria son:
- Electrolito: Es el material que conduce los iones (partículas cargadas) entre los electrodos. Puede ser líquido o sólido.
- Electrodos: Son las superficies donde ocurren las reacciones químicas. El combustible se oxida en el ánodo y el oxígeno se reduce en el cátodo. Suelen ser porosos para que los gases puedan llegar a la superficie.
Apilamientos
Como una sola pila produce poco voltaje (alrededor de 0.7 voltios), se conectan varias en serie para obtener el voltaje deseado. Estas conexiones se hacen con materiales que conducen bien la electricidad. Los apilamientos pueden ser planos o tubulares.
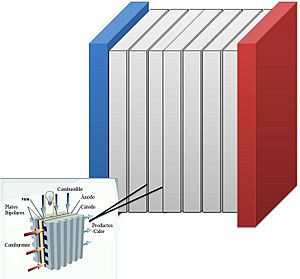
En los apilamientos planos, se usan "platos bipolares" que separan el combustible y el oxidante de las celdas vecinas y ayudan a distribuir los gases. Este diseño es eficiente porque la corriente eléctrica tiene un camino corto.
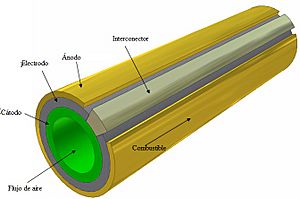
Otro tipo de apilamiento es el tubular, usado en pilas que funcionan a altas temperaturas, como las de óxido sólido (SOFC). Estas pilas suelen usar un material cerámico sólido como electrolito.
Sistemas Completos
Una pila de combustible no funciona sola. Necesita otros componentes y subsistemas, conocidos como "balance de planta" (BOP). Un sistema completo incluye el apilamiento de pilas de combustible y el BOP.
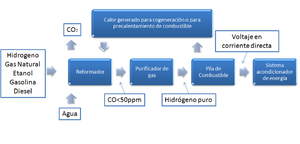
La configuración del BOP varía según el tipo de pila, la temperatura de operación, el combustible y la aplicación. Sin embargo, un sistema genérico podría incluir:
- Un reformador: Si el combustible no es hidrógeno puro (como gas natural), el reformador lo convierte en un gas rico en hidrógeno.
- Un purificador de gas: Elimina las impurezas del gas antes de que entre en la pila.
- La pila de combustible: Aquí se genera la electricidad.
- Sistemas para aprovechar el calor: El calor generado en la reacción puede usarse para precalentar el combustible o para cogeneración (producir más electricidad o calor para otros usos).
Tipos de Pilas de Combustible
Existen muchos tipos de pilas de combustible, que se pueden clasificar de varias maneras:
- Por el tipo de combustible y oxidante: Generalmente hidrógeno y oxígeno.
- Por el tipo de electrolito: Como ácido fosfórico o membrana de polímero.
- Por la temperatura de operación: Bajas (menos de 200°C) o altas (más de 600°C).
- Por su eficiencia: Varía según el tipo y la aplicación.
- Por su uso: Portátiles, fijas, para transporte, militares, espaciales.
- Por su potencia: Baja (pocos vatios) o alta (megavatios).
- Por el catalizador usado: Platino, metales no preciosos, etc.
La forma más común de clasificarlas es por el tipo de electrolito. Aquí te presentamos los cinco tipos principales:
Pila de Combustible de Membrana de Intercambio Protónico (PEM)
- Electrolito: Membrana de polímero sólido.
- Catalizador: Platino.
- Temperatura de operación: Alrededor de 80-95°C.
- Eficiencia eléctrica: 40-60%.
Las pilas PEM funcionan a temperaturas bajas, son potentes y pueden cambiar su potencia rápidamente. Se usan en telecomunicaciones, vehículos (como montacargas y autobuses) y se espera que pronto en coches de pasajeros. Pueden usar hidrógeno, metanol o combustibles reformados.
El principal desafío es reducir su costo y mejorar la membrana para que conduzca mejor los protones y retenga más agua.
PEM de Alta Temperatura (HT-PEM): Son PEM que pueden operar entre 120°C y 200°C. Se usan en vehículos y para dar energía a edificios, y pueden usar una mayor variedad de combustibles.
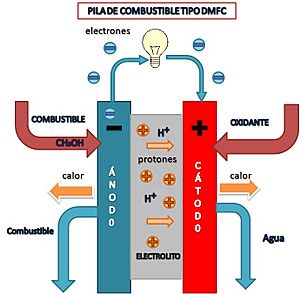
Pila de Combustible de Metanol Directo (DMFC)
- Electrolito: Membrana de polímero sólido.
- Catalizador: Platino.
- Temperatura de operación: Alrededor de 50-120°C.
- Eficiencia eléctrica: Por encima del 40%.
Las DMFC también usan una membrana de polímero. No necesitan un reformador, ya que el catalizador del ánodo extrae el hidrógeno directamente del metanol líquido. Como funcionan a baja temperatura, son ideales para aparatos pequeños como teléfonos móviles, ordenadores portátiles y cargadores de baterías.
El reto es encontrar una membrana que funcione a temperaturas más altas y un catalizador más activo para el metanol.
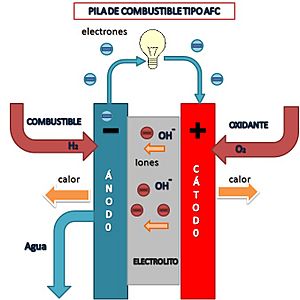
Celdas de Combustible Alcalinas (AFC)
- Electrolito: Solución de hidróxido de potasio en agua.
- Catalizador: Metales no preciosos.
- Temperatura de operación: Entre 105-245°C.
- Eficiencia eléctrica: 60-70%.
Las AFC necesitan hidrógeno y oxígeno puros, porque el dióxido de carbono las "envenena" y reduce su eficiencia. Por eso, se usan principalmente en el espacio y en submarinos. Son muy eficientes, una de las razones por las que la NASA las ha usado desde 1960 en misiones espaciales para electricidad y agua potable.
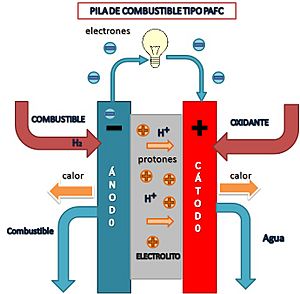
Pila de Combustible de Ácido Fosfórico (PAFC)
- Electrolito: Ácido fosfórico líquido.
- Catalizador: Platino sobre base de carbono.
- Temperatura de operación: Entre 180-205°C.
- Eficiencia eléctrica: 36-42%.
Las PAFC pueden usar hidrocarburos o biogás como combustible. Funcionan a temperaturas más altas que las PEM y toleran mejor las impurezas. Se usan mucho en cogeneración, para dar electricidad a edificios con alta demanda de energía.
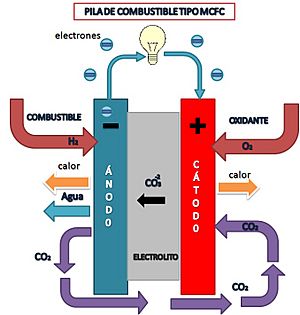
Pila de Combustible de Carbonato Fundido (MCFC)
- Electrolito: Carbonatos alcalinos sobre una matriz cerámica.
- Catalizador: Material de los electrodos (no platino).
- Temperatura de operación: Alrededor de 650°C.
- Eficiencia eléctrica: 50-60%.
Las MCFC operan a alta temperatura, lo que les permite convertir el combustible en hidrógeno dentro de la propia pila. Son resistentes a la contaminación por monóxido o dióxido de carbono, por lo que pueden usar gases derivados del carbón. Se usan en aplicaciones fijas y en cogeneración para edificios.
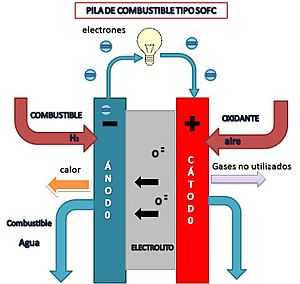
Pila de Combustible de Óxido Sólido (SOFC)
- Electrolito: Sólido cerámico u óxido metálico no poroso.
- Catalizador: Material de los electrodos (no platino).
- Temperatura de operación: 800-1000°C.
- Eficiencia eléctrica: 50-60%.
Estas pilas de alta temperatura pueden convertir hidrocarburos ligeros (como gas natural) internamente. Se usan en muchas aplicaciones fijas en todo el mundo. El reto actual es lograr que funcionen a temperaturas más bajas (600-800°C) y encontrar nuevos materiales para el electrolito.
Comparación de Tipos de Pilas de Combustible
| Tipo de Pila | Electrolito | Catalizador | Temperatura de Operación(°C) | Potencia | Eficiencia Eléctrica(%) | Usos Principales | Ventajas | Inconvenientes |
|---|---|---|---|---|---|---|---|---|
| PEMFC | polímero sólido | Platino | 80-95 | (0,1-100)kW |
|
|
|
|
| DMFC | polímero sólido | Platino | 50-120 | 1mW-100kW |
|
|
|
|
| AFC | solución de hidróxido de potasio en agua | metales no preciosos | 105-245 | (10-100)kW |
|
|
|
|
| PAFC | Ácido fosfórico líquido | platino sobre base de carbono | 180-205 | >10MW |
|
|
|
|
| MCFC | carbonatos alcalinos sobre una matriz cerámica | material de los electrodos (no platino) | 650 | 100W |
|
|
|
|
| SOFC | sólido cerámico | material de los electrodos (no platino) | 800-1000 | >100kW |
|
|
|
|
Otros Tipos de Pilas de Combustible
Existen otros tipos de pilas de combustible que se están investigando o ya se comercializan:
| Tipo de pila de combustible | Electrolito | Potencia eléctrica (W) | Temperatura de trabajo (°C) | Eficiencia de la pila (%) | Eficiencia del sistema (%) | Estado |
|---|---|---|---|---|---|---|
| Pila de combustible de hidruros metálicos | solución acuosa alcalina | -20 | Comercial / investigación | |||
| Pila de combustible electro-galvánica | solución acuosa alcalina | >40 | Comercial / investigación | |||
| Pila de combustible de ácido fórmico | membrana polimérica (ionómero) | < 50 W | < 40 | Comercial / investigación | ||
| Batería de zinc-aire | solución acuosa alcalina | <40 | Producción en masa | |||
| Pila de combustible microbiana | Membrana de polímero o ácido húmico | <40 | investigación | |||
| Pila de combustible regenerativa | membrana polimérica (ionómero) | <50 | Comercial / investigación | |||
| Pila de combustible borohidruro | solución acuosa alcalina | 70 | Comercial / investigación | |||
| Pila de combustible de metanol reformado | membrana polimérica (ionómero) | 5 W – 100 kW | 125-300 | 50–60 | 25–40 | Comercial / investigación |
| Pila de combustible de etanol | membrana polimérica (ionómero) | < 140 mW/cm² | > 25 | investigación | ||
| Pila de combustible REDOX | electrolitos líquidos y membrana polimérica (ionómero) | 1 kW – 10 MW | investigación | |||
| Pila de combustible cerámica protónica | conductor de H+ de óxido cerámico | investigación | ||||
| Pila de combustible de carbono | varios diferentes | 700–850 | 80 | 70 | Comercial / investigación | |
| Bio-pilas de combustible enzimáticas | cualquiera que no desnaturalice la enzima | <40 | investigación | |||
| Pila de combustible de magnesio-aire | agua salada | (-20)-555 | 90 | Comercial / investigación |
Comportamiento de las Pilas de Combustible
Una pila de combustible produce una reacción electroquímica que genera electricidad. La cantidad máxima de trabajo eléctrico que se puede obtener de una pila se relaciona con un concepto llamado energía libre de Gibbs.
Rendimiento
El rendimiento ideal de una pila de combustible es la relación entre la energía eléctrica que se obtiene y la energía química que se usa. Por ejemplo, para una pila que usa hidrógeno y oxígeno para producir agua, el rendimiento ideal es del 83%.
A diferencia de los motores de combustión, las pilas de combustible no están limitadas por el ciclo de Carnot, lo que significa que pueden tener un rendimiento muy alto al convertir directamente la energía química en eléctrica.
Sin embargo, en la práctica, el rendimiento real es menor que el ideal debido a pérdidas de energía. Una pila de combustible convierte la energía química en electricidad con un rendimiento de alrededor del 50%. Este rendimiento disminuye si la corriente que circula por la celda es mayor.
También hay que considerar las pérdidas al producir, transportar y almacenar el combustible. Por ejemplo, los vehículos con pilas de combustible que usan hidrógeno comprimido tienen una eficiencia del 22%.
Las pilas de combustible no almacenan energía como las baterías. A veces se combinan con otros sistemas para almacenar energía, como en centrales eléctricas que usan fuentes de energía intermitentes (como la solar o eólica).
En sistemas de "cogeneración" (donde se produce electricidad y calor al mismo tiempo), el rendimiento de la conversión de combustible a electricidad puede ser más bajo (15-20%), pero el calor que se genera se aprovecha, lo que aumenta la eficiencia total del sistema a alrededor del 80%.
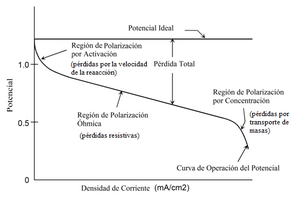
Comportamiento Real
Cuando una pila de combustible está funcionando y hay corriente eléctrica, el voltaje que produce es menor que el ideal. Esto se debe a varias pérdidas:
- Pérdidas por activación: Ocurren porque las reacciones químicas en los electrodos son lentas.
- Pérdidas óhmicas (resistivas): Se deben a la resistencia al paso de electrones en los electrodos y al paso de iones en el electrolito.
- Pérdidas por concentración: Suceden cuando el combustible o el oxígeno no llegan lo suficientemente rápido a los electrodos, o los productos de la reacción no se eliminan a tiempo.
Para reducir estas pérdidas, se pueden usar catalizadores más eficientes, materiales con alta conductividad, membranas delgadas y controlar bien la temperatura y el flujo de gases.
Factores que Afectan el Funcionamiento
El rendimiento de las pilas de combustible se ve afectado por:
- Las condiciones de operación (temperatura, presión, composición del gas).
- El diseño de la pila.
- Impurezas en el combustible.
- La durabilidad del dispositivo.
Usos de las Celdas de Combustible
Energía
Las pilas de combustible son muy útiles como fuentes de energía en lugares remotos, como naves espaciales, estaciones meteorológicas lejanas, parques grandes, zonas rurales y en algunas aplicaciones militares. Son compactas, ligeras y no tienen muchas partes móviles, lo que las hace muy fiables.
También se usan en sistemas de cogeneración para casas, oficinas y fábricas. Estos sistemas producen electricidad de forma constante (vendiendo el exceso a la red si no se usa) y, al mismo tiempo, generan aire y agua caliente con el calor que desprenden. Las pilas de combustible de ácido fosfórico (PAFC) son muy comunes en cogeneración y pueden alcanzar eficiencias combinadas de casi el 80%.
Las pilas de combustible son mucho más limpias que las plantas de energía tradicionales. Una planta de energía con pila de combustible que use gas natural podría generar muy pocos contaminantes (aparte del dióxido de carbono), mientras que los sistemas de combustión convencionales producen muchos más.
Existen proyectos experimentales donde paneles solares producen electricidad para electrolizadores que generan hidrógeno. Este hidrógeno se almacena y luego se usa en pilas de combustible para dar energía a hogares en islas o zonas rurales.
Las pilas de combustible también pueden usar gas de baja calidad de vertederos o plantas de tratamiento de aguas para generar energía y reducir las emisiones de metano. La planta de energía con pilas de combustible más grande está en California y produce 2.8 MW.
Un grupo musical llamado Protium fue el primero en el mundo en usar celdas de combustible de hidrógeno para alimentar sus equipos.
Cogeneración
Los sistemas de cogeneración con pilas de combustible (CHP) proporcionan calor y energía a hogares y edificios. Generan electricidad y, con el calor residual, producen aire y agua caliente. Esto ahorra energía porque se aprovecha el calor que normalmente se desperdiciaría. La eficiencia de estos sistemas puede llegar al 85%.
Vehículos con Pila de Combustible
Automóviles
Aunque no se venden masivamente, se han desarrollado más de 20 prototipos de coches con pilas de combustible (FECV) desde 2009, como el Honda FCX Clarity y el Toyota FCHV. Estos coches han recorrido millones de kilómetros, pueden recargarse en menos de 5 minutos y tienen una autonomía de 400 km.
Algunos expertos creen que los coches con pilas de combustible tardarán décadas en ser competitivos económicamente. Sin embargo, grandes fabricantes como Toyota, Mercedes-Benz, Hyundai, General Motors, Honda y Nissan planean lanzar modelos de producción en los próximos años.
Autobuses
Desde 2011, hay unos 100 autobuses con pilas de combustible en el mundo. Estos autobuses son más eficientes que los diésel o de gas natural y se han usado en ciudades como Whistler (Canadá), San Francisco (EE. UU.), Hamburgo (Alemania) y Londres (Inglaterra).
Montacargas
Los montacargas con pilas de combustible son vehículos industriales que se usan para mover materiales. La mayoría usan pilas PEM. En 2013, más de 4.000 montacargas de este tipo se usaban en Estados Unidos.
Tienen ventajas sobre los que usan gasolina o baterías: no producen emisiones locales, pueden trabajar 8 horas con un solo tanque de hidrógeno, se recargan en 3 minutos y duran de 8 a 10 años. Son ideales para almacenes refrigerados porque su rendimiento no se ve afectado por las bajas temperaturas.
Motocicletas y Bicicletas
En 2005, la empresa inglesa Intelligent Energy (IE) creó la primera motocicleta de hidrógeno, la ENV, que podía recorrer 160 km a 80 km/h. Honda y Suzuki también han desarrollado motocicletas y scooters con pilas de combustible.
Aviones
En 2003, el primer avión no tripulado propulsado por pilas de combustible realizó su primer vuelo. Investigadores de Boeing y Airbus también han hecho vuelos de prueba con aviones tripulados usando pilas de combustible y baterías. Los militares están interesados en esta tecnología por su bajo ruido y calor, y su capacidad para volar a gran altitud.
Barcos
El primer barco con pila de combustible, el HYDRA, usó un sistema AFC. Islandia planea convertir su flota pesquera a pilas de combustible. Ámsterdam ya tiene un ferry de pasajeros que funciona con pilas de combustible en sus canales.
Submarinos
Los submarinos alemanes Tipo 212A usan pilas de combustible (desarrolladas por Siemens) para sus propulsores, lo que les permite permanecer sumergidos durante semanas sin salir a la superficie. Son muy silenciosos, lo que les da una ventaja. Los submarinos españoles S-80 también usarán un sistema similar.
Estaciones de Servicio
La primera estación de abastecimiento de hidrógeno se abrió en Reikiavik, Islandia, en 2003. Esta estación produce su propio hidrógeno mediante electrólisis, usando solo electricidad y agua. En 2010, había 85 estaciones de hidrógeno en Estados Unidos, y se planea que Alemania tenga 50 para 2015. Japón también tiene una "autopista de hidrógeno".
Sistemas de Energía Portátiles
Las pilas de combustible portátiles se usan en el ocio (caravanas, cabañas), en la industria (para pozos de gas o petróleo remotos, torres de comunicación) y en el sector militar.
Otros Posibles Usos
- Plantas de energía base.
- Sistemas auxiliares de energía.
- Sistemas de energía de emergencia para hogares, hospitales y centros de datos.
- Equipos de telecomunicaciones y navales.
- Sistemas de alimentación ininterrumpida (UPS) para proteger equipos electrónicos.
- Calentamiento de agua con hidrógeno solar.
- Vehículos híbridos (pila de combustible y batería).
- Puertos portátiles para cargar pequeños dispositivos electrónicos.
- Teléfonos inteligentes, portátiles y tabletas.
- Aparatos de calefacción pequeños.
- Conservación de alimentos (eliminando el oxígeno).
- Detectores de monóxido de carbono.
Los principales desafíos actuales son encontrar materiales de soporte y catalizadores más eficientes, duraderos y económicos.
Economía y Medio Ambiente
En 2012, la industria de las pilas de combustible generó más de mil millones de dólares en ingresos a nivel mundial. Aunque aún no todas las empresas son rentables, el número de pilas de combustible enviadas globalmente ha crecido rápidamente.
Se predice que hay suficientes reservas de platino para la demanda futura, y se están investigando alternativas más económicas y duraderas, como recubrimientos de oro y paladio, o el uso de hierro y azufre en lugar de platino.
Las pilas de combustible son muy atractivas por su alta eficiencia y, en un escenario ideal con energías renovables, por no producir emisiones contaminantes. Sin embargo, si el hidrógeno se produce usando electricidad de centrales eléctricas que queman carbón, la contaminación se traslada a esas centrales.
Es importante considerar todo el ciclo del hidrógeno: su producción, uso, la infraestructura necesaria y los convertidores de energía. Las reservas mundiales de platino podrían no ser suficientes si todos los vehículos se convirtieran a pilas de combustible con la tecnología actual, lo que aumentaría el precio del platino. Por eso, se investigan catalizadores alternativos, como los de hierro y nitrógeno.
Glosario de Términos
- Electrodo: Parte de un conductor por donde entra o sale la corriente eléctrica.
- Ánodo: Electrodo donde ocurre la oxidación (pérdida de electrones). En pilas de combustible, es el terminal negativo.
- Cátodo: Electrodo donde ocurre la reducción (ganancia de electrones). En pilas de combustible, es el terminal positivo.
- Electrolito: Sustancia que conduce iones cargados de un electrodo a otro.
- Apilamiento: Varias pilas de combustible individuales conectadas en serie para aumentar el voltaje.
- Solución: Mezcla homogénea de una sustancia disuelta en otra.
- Catalizador: Sustancia química que acelera una reacción sin consumirse.
- Matriz: Lugar o estructura donde algo se origina o desarrolla.
- Membrana: Capa que separa los gases en una pila de combustible y actúa como electrolito.
|
Véase también
 En inglés: Fuel cell Facts for Kids
En inglés: Fuel cell Facts for Kids