Constante de los gases ideales para niños
La constante universal de los gases ideales, también conocida como constante de los gases o constante molar de los gases, es un número muy importante en la física y la termodinámica. Se usa para entender cómo se comportan los gases, especialmente los llamados "gases ideales". Esta constante relaciona el volumen, la presión, la temperatura y la cantidad de sustancia de un gas.
Contenido
¿Qué es la Constante Universal de los Gases?
Esta constante, que se representa con la letra R, se usa principalmente en una fórmula especial para los gases ideales. Un gas ideal es un modelo teórico que nos ayuda a entender cómo se comportan los gases en la vida real. En este modelo, se asume que las partículas del gas son muy pequeñas y no interactúan entre sí.
La fórmula principal donde aparece la constante R es la siguiente:

Aquí, cada letra significa algo:
- P es la presión del gas.
- V es el volumen que ocupa el gas.
- n es la cantidad de sustancia del gas (medida en moles).
- R es nuestra constante universal de los gases.
- T es la temperatura del gas.
Aunque los gases reales no son exactamente "ideales", muchos se comportan de forma muy parecida a este modelo, sobre todo si no están a presiones muy altas o temperaturas muy bajas.
¿Cuál es el Valor de R?
El valor de la constante R es siempre el mismo, pero puede expresarse con diferentes números dependiendo de las unidades que usemos para la presión, el volumen y la temperatura.
Aquí te mostramos algunos de sus valores más comunes:
- R = 0,08205746 en unidades de [atmósfera (presión) · litro (volumen)] / [mol (cantidad) · Kelvin (temperatura)]
- R = 8,31446261815324 en unidades de [julio (energía)] / [mol (cantidad) · Kelvin (temperatura)]
- R = 1,987207 en unidades de [caloría (energía)] / [mol (cantidad) · Kelvin (temperatura)]
El valor de 8,31446261815324 J/(mol·K) es el valor exacto que se usa en la ciencia moderna.
¿Por qué es Importante la Constante R?
Aunque su nombre nos hace pensar en gases, la constante R es mucho más importante de lo que parece. Aparece en muchas otras áreas de la física y la química, no solo en las relacionadas con los gases.
Esto se debe a que R está muy conectada con otra constante fundamental llamada la constante de Boltzmann. La constante de Boltzmann nos ayuda a entender cómo la energía de las partículas se relaciona con la temperatura de un sistema.
La relación entre R y la constante de Boltzmann (kB) es la siguiente:
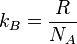
Donde NA es la constante de Avogadro, que nos dice cuántas partículas hay en un mol de sustancia.
Desde el año 2019, tanto la constante de Boltzmann como la constante de Avogadro tienen valores exactos definidos. Esto significa que el valor de R también es exacto.
Además de la ecuación de los gases ideales, la constante R (o la constante de Boltzmann) aparece en muchas otras fórmulas importantes en la ciencia, como las que describen reacciones químicas, propiedades de los materiales y el comportamiento de la energía a nivel microscópico.
Véase también
 En inglés: Boltzmann constant Facts for Kids
En inglés: Boltzmann constant Facts for Kids
- Ley de los gases ideales
- Constante de Avogadro
- Teoría cinética

