Adhesión para niños
La adhesión es una propiedad de la materia que permite que dos superficies, ya sean del mismo tipo o diferentes, se unan y se mantengan juntas cuando entran en contacto. Esto ocurre gracias a fuerzas muy pequeñas que actúan entre las moléculas de las sustancias.
La adhesión ha sido muy importante en la construcción desde hace mucho tiempo. Por ejemplo, el mortero (que es como un pegamento fuerte) une los ladrillos para construir paredes y edificios.
Es importante saber que la adhesión es diferente de la cohesión. La cohesión es la fuerza que mantiene unidas las partículas dentro de un mismo material (por ejemplo, cómo las moléculas de agua se atraen entre sí para formar una gota). En cambio, la adhesión es la fuerza que une las superficies de materiales distintos.


Contenido
¿Qué es la energía superficial?
La energía superficial es como la "energía" que tiene la superficie de un material. Imagina que quieres separar un material en dos partes; la energía superficial es la cantidad de trabajo que necesitas para crear esas dos nuevas superficies. Cuanto mayor sea la energía superficial de un material, más fácil será que otras cosas se peguen a él.
¿Cómo se pegan las cosas? Mecanismos de adhesión
Existen varias formas en que los materiales pueden unirse entre sí. Aquí te explicamos las cinco principales:
Adhesión mecánica: ¿Cómo funciona?
La adhesión mecánica ocurre cuando un material adhesivo se mete en los pequeños huecos o poros de otra superficie. Es como si se "enganchara" o "enclavara" en ella. Un buen ejemplo es el velcro, donde pequeños ganchos se unen a pequeños bucles. Algunos pegamentos textiles también funcionan así, pero a una escala mucho más pequeña.
Adhesión química: ¿Qué enlaces se forman?
La adhesión química sucede cuando los átomos de dos superficies diferentes forman enlaces entre sí. Estos enlaces pueden ser muy fuertes, como los enlaces iónicos o covalentes, donde los átomos comparten o intercambian electrones. También pueden ser enlaces más débiles, como los puentes de hidrógeno, que ocurren cuando un átomo de hidrógeno es atraído por otros átomos como el nitrógeno o el oxígeno.
Para que la adhesión química funcione, las superficies deben estar muy, muy cerca, a menos de un nanómetro (que es una milmillonésima parte de un metro). Esto hace que estos enlaces sean muy efectivos, pero también un poco frágiles si las superficies se separan.
Adhesión dispersiva: ¿Qué son las fuerzas de Van der Waals?
En la adhesión dispersiva, los materiales se mantienen unidos por unas fuerzas llamadas fuerzas de van der Waals. Estas fuerzas son atracciones débiles que ocurren entre las moléculas. Aunque cada molécula no tenga una carga eléctrica permanente, el movimiento de sus electrones puede crear pequeñas cargas temporales (polos positivos y negativos) que se atraen entre sí.
Estas fuerzas son muy importantes porque no necesitan que las superficies tengan una carga permanente. Por ejemplo, las calcomanías y pegatinas que se pegan al vidrio sin usar pegamento químico funcionan gracias a estas fuerzas. Son útiles porque no pierden su capacidad de pegarse tan rápido como otros adhesivos.
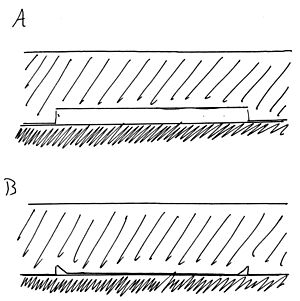
Cuando una gota de líquido se posa sobre una superficie, el ángulo de contacto nos dice qué tan bien se adhiere. Si el ángulo es bajo, significa que el líquido se extiende mucho y se adhiere bien a la superficie.

Adhesión electrostática: ¿Cómo se atraen las cargas?
Algunos materiales que conducen la electricidad pueden generar una diferencia de carga eléctrica cuando se unen. Esto crea una fuerza de atracción eléctrica entre ellos, similar a cómo un globo frotado se pega a la pared.
Adhesión difusiva: ¿Cómo se mezclan los materiales?
La adhesión difusiva ocurre cuando las moléculas de un material se mueven y se mezclan con las moléculas de otro material en la zona de contacto. Esto es muy efectivo con materiales como los polímeros (cadenas largas de moléculas), donde un extremo de la cadena puede "difundirse" o meterse en el otro material.
También es el mecanismo que se usa en la sinterización, un proceso donde polvos de metal o cerámica se calientan y se presionan. Los átomos de las partículas se mueven y se mezclan, haciendo que el material se vuelva más uniforme y fuerte.
Para que la difusión ocurra, las moléculas deben tener libertad para moverse. Por ejemplo, los polímeros que están "entrelazados" (reticulados) no pueden difundirse tan fácilmente como los que no lo están. Cuando las moléculas se mezclan a través de la superficie, forman muchos enlaces que, aunque individualmente sean débiles, juntos crean una unión muy fuerte.
Véase también
 En inglés: Adhesion Facts for Kids
En inglés: Adhesion Facts for Kids