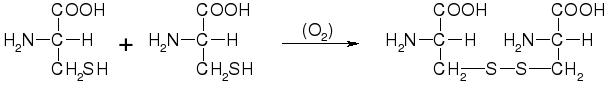Péptido para niños
Los péptidos son un tipo de molécula que se forma cuando varios aminoácidos se unen entre sí. Piensa en los aminoácidos como pequeños ladrillos; cuando se juntan, forman una cadena que es un péptido. Se unen mediante algo llamado enlace peptídico.
Los péptidos, al igual que las proteínas, se encuentran en la naturaleza y cumplen muchísimas funciones importantes en los seres vivos. Algunas de estas funciones aún se están investigando.
La diferencia principal entre un péptido y una proteína es su tamaño. Si se unen pocos aminoácidos, se forma un péptido. Si se unen muchos, se forma una proteína. No hay un número exacto que los separe, pero generalmente los péptidos son más pequeños.
Péptidos: Pequeños Constructores de la Vida
¿Qué son los Péptidos?
Los péptidos son cadenas cortas de aminoácidos. Los aminoácidos son las unidades básicas que forman tanto los péptidos como las proteínas. Se unen entre sí a través de un tipo especial de unión química llamada enlace peptídico.
Tipos de Péptidos: ¿Cuántos Ladrillos Tienen?
Los péptidos se clasifican según la cantidad de aminoácidos que los forman:
- Oligopéptidos: Tienen entre 2 y 10 aminoácidos.
- Dipéptidos: Si tienen 2 aminoácidos.
- Tripéptidos: Si tienen 3 aminoácidos.
- Tetrapéptidos: Si tienen 4 aminoácidos.
- Péptidos: Generalmente tienen entre 10 y 50 aminoácidos.
- Polipéptidos: Tienen entre 51 y 100 aminoácidos.
Las proteínas que se fabrican dentro de las células suelen estar formadas por uno o más polipéptidos. Algunos científicos consideran que el límite entre un péptido y una proteína está en los 100 aminoácidos.
Los péptidos son más pequeños que las proteínas. Además, las proteínas pueden estar formadas por varias cadenas de polipéptidos y a veces tienen otras partes adicionales. Un buen ejemplo de polipéptido es la insulina, que tiene 51 aminoácidos. La insulina es una hormona muy importante que ayuda a regular el azúcar en el cuerpo humano.
¿Cómo se Unen los Aminoácidos en un Péptido?
El enlace peptídico es una unión fuerte que se forma entre el grupo amino (–NH2) de un aminoácido y el grupo carboxilo (–COOH) de otro. Es como si se dieran la mano para unirse.
Para darle un nombre a un péptido, se empieza por el aminoácido que tiene el grupo –NH2 al principio de la cadena (llamado extremo N-terminal) y se termina con el aminoácido que tiene el grupo –COOH al final (llamado extremo C-terminal). Por ejemplo, si el primer aminoácido es alanina y el segundo es serina, el péptido se llamaría alanil-serina, o de forma abreviada, Ala-Ser o AS.
Comportamiento de los Péptidos en el Cuerpo
Los péptidos tienen un comportamiento especial en relación con los ácidos y las bases, similar al de los aminoácidos. Esto se debe a que tienen un grupo amino al principio y un grupo carboxilo al final, y algunos de sus aminoácidos pueden tener grupos que reaccionan con ácidos o bases.
Los péptidos, al igual que los aminoácidos y las proteínas, son moléculas que pueden actuar como ácidos o como bases. Esto les permite ayudar a mantener el equilibrio químico en los organismos, lo que es muy importante para que todo funcione bien.
Este comportamiento es clave en las enzimas, que son un tipo de péptidos o proteínas que actúan como aceleradores de las reacciones químicas en el cuerpo. Las enzimas funcionan mejor dentro de ciertos niveles de acidez o basicidad (pH). Si el pH cambia demasiado, la enzima puede perder su forma y dejar de funcionar correctamente.
Reacciones Químicas de los Péptidos
Los péptidos pueden participar en las mismas reacciones químicas que los aminoácidos, ya que tienen los mismos grupos químicos (amino, carboxilo y los grupos R de cada aminoácido). Estas reacciones se han usado para descubrir el orden de los aminoácidos en un péptido.
Reacciones del Grupo Amino
Una reacción importante del grupo amino es la que se usa para identificar el primer aminoácido de una cadena. Por ejemplo, con el reactivo de Sanger, se puede marcar el primer aminoácido y luego, al romper el péptido, identificarlo. Así fue como se descubrió la secuencia de la insulina.
Otro método es la degradación de Edman. Este proceso permite quitar un aminoácido a la vez del principio de la cadena sin romper el resto del péptido. Así, se puede ir identificando cada aminoácido en orden. Este es el método que usan las máquinas automáticas para leer la secuencia de las proteínas. Sin embargo, estas máquinas solo pueden leer los primeros 20 o 30 aminoácidos de una cadena larga.
Reacciones del Grupo Carboxilo
También es posible identificar los aminoácidos empezando por el final de la cadena (el extremo carboxilo-terminal). Para esto se usan unas enzimas especiales llamadas carboxipeptidasas. Estas enzimas rompen los enlaces peptídicos uno por uno desde el final. Hay diferentes tipos de carboxipeptidasas, y cada una es específica para ciertos tipos de aminoácidos.
Reacciones de los Grupos R
Los grupos R son las partes variables de los aminoácidos. Hay muchos reactivos que reaccionan específicamente con ciertos grupos R. Esto es útil para saber qué aminoácidos son esenciales para que una proteína funcione.
Una reacción interesante de los grupos R es la del grupo tiólico (-SH) de la cisteína, un tipo de aminoácido. Este grupo es muy sensible al oxígeno. Si dos moléculas de cisteína están cerca y hay oxígeno, pueden unirse formando un "puente disulfuro".
Estos puentes disulfuro son muy importantes porque ayudan a que las proteínas mantengan su forma tridimensional, que es crucial para su función. A veces, estos puentes se forman de manera natural para estabilizar la proteína.
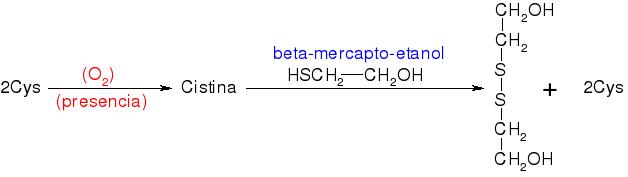
Sin embargo, si una proteína se aísla de su entorno natural, el oxígeno puede hacer que se formen puentes disulfuro donde no deberían, lo que podría hacer que la proteína pierda su función. Para evitar esto, se añaden sustancias como el β-mercapto-etanol, que se oxida en lugar de la cisteína, protegiéndola.
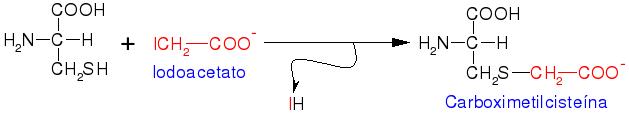
Cuando se quiere estudiar la composición de aminoácidos de una proteína, se rompe completamente en sus aminoácidos individuales. Para evitar que las cisteínas se oxiden durante este proceso, se añade un reactivo llamado iodoacetato, que las transforma en otra molécula y las protege.
Véase también
 En inglés: Peptide Facts for Kids
En inglés: Peptide Facts for Kids
- Secuencia de aminoácidos
- Neuropéptido
- Biuret