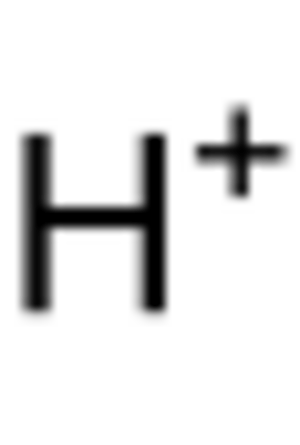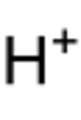Protonación para niños
En el mundo de la química, la protonación es un proceso muy importante. Imagina que tienes una molécula o un átomo, y de repente, se le une una pequeña partícula llamada protón. Eso es la protonación: la adición de un protón (que se representa como H+) a otra sustancia.
Esta reacción es una de las más básicas y fundamentales en la química. Es un paso clave en muchos procesos que ocurren en los laboratorios y en la naturaleza. Algunas sustancias pueden aceptar más de un protón; a estas se les llama "polibásicas". Esto es común en moléculas grandes, como las que encontramos en los seres vivos. Por otro lado, las sustancias que pueden perder protones se llaman "ácidas". Si pueden perder varios protones, se les llama "poliácidas".
Cuando una sustancia se protona, su peso y su carga eléctrica aumentan un poco. La protonación (y su opuesto, la deprotonación, que es cuando se pierde un protón) cambia muchas de las propiedades de una molécula. Por ejemplo, puede afectar cómo se mezcla con el agua, cómo reacciona con la luz o cómo interactúa con otras sustancias. La protonación también es esencial en algunas técnicas de laboratorio, como la espectrometría de masas, que ayuda a identificar moléculas.
La protonación y la deprotonación son el corazón de las reacciones ácido-base. Según una teoría importante, un ácido es una sustancia que dona un protón a otra sustancia.
Contenido
Velocidad de la Protonación en Química
Las reacciones de protonación suelen ser muy rápidas. Esto se debe, en parte, a que los protones se mueven con mucha facilidad, especialmente en el agua. La velocidad de estas reacciones está relacionada con la fuerza del ácido involucrado. Los ácidos que son más débiles protonan (o donan protones) de forma menos intensa que los ácidos fuertes. A veces, la protonación puede ser más lenta si causa un gran cambio en la forma o estructura de la molécula.
¿Es Reversible la Protonación?
Generalmente, las reacciones de protonación son reversibles. Esto significa que la sustancia que ganó el protón puede volver a perderlo sin que su estructura principal cambie. Sin embargo, en algunos casos, la adición de un protón puede hacer que la molécula cambie su forma. Por ejemplo, algunos tipos de moléculas llamadas alquenos pueden cambiar de una forma (llamada cis) a otra (llamada trans) si se les añade un protón. Muchas enzimas, que son proteínas que aceleran las reacciones químicas en nuestro cuerpo, funcionan usando mecanismos que implican la adición y eliminación reversible de protones en las sustancias con las que trabajan.
¿Qué Dice la IUPAC?
La IUPAC (Unión Internacional de Química Pura y Aplicada) es una organización que establece las reglas y nombres en química. Ellos sugieren usar el término "hidronación" en lugar de "protonación". Esto se debe a que, aunque la mayoría de los núcleos de hidrógeno son solo protones, una pequeña parte son otros tipos de hidrógeno, como el deuterio o el tritio. Sin embargo, en la práctica, la mayoría de los químicos siguen usando los términos "protón" y "protonación" porque son más comunes y fáciles de entender.
Galería de imágenes
Véase también
 En inglés: Protonation Facts for Kids
En inglés: Protonation Facts for Kids