Efecto estérico para niños
El efecto estérico es un concepto importante en la química orgánica. Se refiere a cómo el tamaño y la forma de los grupos de átomos en una molécula pueden influir en su comportamiento. Esto incluye cómo reacciona una molécula, qué forma adopta o cómo interactúa con otras moléculas.
Este término fue usado por primera vez en 1894 por un científico llamado Viktor Meyer. Él notó que algunas reacciones químicas eran muy lentas cuando había átomos o grupos grandes cerca del lugar donde ocurría la reacción. Para que dos moléculas reaccionen, deben chocar de una manera específica y con la orientación correcta. Si hay partes grandes que estorban, esto se vuelve más difícil.
El efecto estérico también ocurre cuando un grupo de átomos en una molécula interactúa con otros átomos o grupos dentro de la misma molécula. Esto puede cambiar algunas de sus características, como qué tan fácil se evapora (volatilidad) o a qué temperatura hierve (punto de ebullición).
Contenido
Tipos de efectos estéricos
¿Qué es el impedimento estérico?
El impedimento estérico ocurre cuando el tamaño de un grupo de átomos en una molécula impide que otra parte de la misma molécula reaccione. Piensa en ello como si un objeto grande bloqueara el camino de otro.
Un ejemplo de esto se ve en las reacciones de cetonas. Si usas una cetona con grupos muy grandes, la reacción se vuelve muy lenta. Esto sucede porque los grupos grandes ocupan mucho espacio y se repelen entre sí. Para que la reacción ocurra, se necesita más energía, lo que la hace más difícil y lenta.
Aunque a veces el impedimento estérico puede ser un problema, los químicos también lo usan como una herramienta útil. Pueden modificar el comportamiento de una molécula o incluso detener una reacción (esto se llama protección estérica). El impedimento estérico también influye en la velocidad de muchas reacciones químicas.
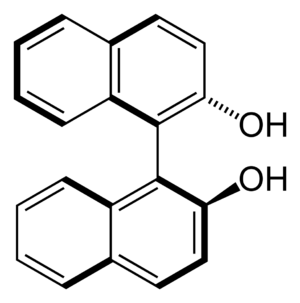
Otro efecto interesante es que el impedimento estérico puede evitar que una molécula gire libremente alrededor de un enlace sencillo. Por ejemplo, la molécula BINOL siempre tiene una forma retorcida debido a que algunos átomos de hidrógeno se estorban entre sí. Esto hace que la molécula sea "quiral", lo que significa que tiene una forma que no se puede superponer con su imagen en un espejo, como tus manos.
¿Cómo funciona la repulsión estérica?
La repulsión estérica ocurre cuando un grupo de átomos en una molécula es "protegido" o "debilitado" por otros grupos cercanos. Esto puede hacer que los átomos que quieren interactuar busquen otros lugares menos protegidos en la molécula. De esta manera, los científicos pueden controlar dónde y cómo ocurrirá una interacción molecular.
¿Qué es la atracción estérica?
La atracción estérica se da cuando las moléculas tienen formas que encajan perfectamente entre sí, como piezas de un rompecabezas. Cuando esto sucede, las moléculas reaccionan de una manera muy específica y selectiva. Es como si estuvieran diseñadas para interactuar de esa forma.
Cómo se mide el efecto estérico
Valores A
Los valores A nos ayudan a medir qué tan "voluminosos" son los grupos de átomos. Son números que se usan para saber cuál es la forma más estable de una molécula. Estos valores se obtienen midiendo la energía de diferentes formas de una molécula llamada ciclohexano. Cuanto más grande es un grupo, más prefiere estar en una posición específica para evitar estorbarse.
| Sustituyente | Valor-A |
|---|---|
| H | 0 |
| CH3 | 1,74 |
| CH2CH3 | 1,75 |
| CH(CH3)2 | 2,15 |
| C(CH3)3 | >4 |
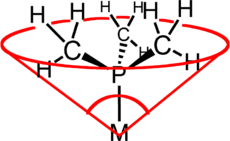
Ángulos cónicos
Los ángulos cónicos son otra forma de medir el tamaño de los grupos de átomos, especialmente en un tipo de química llamada química de coordinación. Se imaginan como el ángulo de un cono que se forma alrededor de un átomo central, mostrando cuánto espacio ocupa un grupo.
| Ligando | Ángulo (°) |
|---|---|
| PH3 | 87 |
| P(OCH3)3 | 107 |
| P(CH3)3 | 118 |
| P(CH2CH3)3 | 132 |
| P(C6H5)3 | 145 |
| P(cyclo-C6H11)3 | 179 |
| P(t-Bu)3 | 182 |
| P(2,4,6-Me3C6H2)3 | 212 |
Efecto estérico y fuerzas eléctricas
La forma y las propiedades de una molécula dependen de los enlaces químicos que la unen, como los enlaces covalentes o los puentes de hidrógeno. Pero estas uniones pueden ser modificadas por fuerzas de repulsión, como el efecto estérico.
Sin embargo, el efecto estérico por sí solo no siempre explica todo. También existen las fuerzas eléctricas (electrostáticas), como la inducción o la simetría molecular, que son muy importantes para entender cómo se comportan las moléculas. El efecto estérico y las fuerzas eléctricas trabajan juntos o se oponen para determinar la estructura y las reacciones de las moléculas.
¿Por qué es importante el efecto estérico?
Entender el efecto estérico es clave en varias áreas de la ciencia:
- En la química orgánica, es casi universal. Afecta, en mayor o menor medida, a la mayoría de las reacciones químicas.
- En la bioquímica, se ve en moléculas naturales como las enzimas. Las enzimas son proteínas grandes que ayudan a que las reacciones químicas ocurran en los seres vivos. A veces, el lugar donde la enzima actúa está "escondido" por su gran tamaño, lo que controla cómo funciona.
- En la farmacología, que es el estudio de los medicamentos, el efecto estérico se usa para saber cómo y en qué medida un medicamento actuará en el cuerpo. La forma y el tamaño de un medicamento pueden determinar si encaja en el lugar correcto para hacer su trabajo.
Véase también
 En inglés: Steric effects Facts for Kids
En inglés: Steric effects Facts for Kids