Cromatografía de intercambio iónico para niños
La cromatografía de intercambio iónico es un método especial que se usa para separar diferentes tipos de partículas, como iones y moléculas polares. Se basa en las cargas eléctricas de estas moléculas. Puede separar casi cualquier molécula que tenga una carga, desde proteínas grandes hasta pequeños aminoácidos. La mezcla que se va a analizar se llama "muestra", y las partes que se separan se conocen como "analitos". Esta técnica es muy útil para purificar proteínas, analizar la calidad del agua o en el control de calidad de productos.
Contenido
Historia de la Cromatografía Iónica
Los primeros métodos que usaban el intercambio de iones se conocen desde 1850. En ese año, los investigadores H. Thompson y J. T. Way en Inglaterra usaron arcillas para extraer amoníaco y liberar calcio de soluciones.
En 1927, se usó por primera vez una columna hecha de un mineral llamado zeolita. Su objetivo era quitar iones de calcio y magnesio que podían molestar al analizar el contenido de sulfato en el agua.
La versión moderna de la cromatografía de intercambio iónico se desarrolló durante un periodo de investigación científica importante en la década de 1940. Se necesitaba una forma de separar y concentrar ciertos elementos. Los científicos eligieron materiales que podían "atrapar" elementos cargados y luego liberarlos de forma diferente.
En 1947, se hizo pública la información sobre cómo usar esta cromatografía para separar productos de ciertos procesos. Gracias a esto, se pudieron crear nuevos materiales para el intercambio de iones. Estos materiales se usan hoy en día para purificar sustancias biológicas y otras sustancias inorgánicas.
A principios de los años 70, Hamish Small y su equipo en Dow Chemical Company crearon la cromatografía iónica. Esta fue una nueva forma de usar la cromatografía de intercambio iónico para análisis automáticos. La cromatografía iónica usa materiales de intercambio iónico más suaves y un sistema especial para quitar los iones que se acumulan. Es una técnica muy potente para encontrar pequeñas cantidades de iones. Es especialmente útil para estudiar el medio ambiente y la calidad del agua.
La tecnología de Dow Chemical fue comprada por Durrum Instrument Corp., que luego creó una empresa separada llamada Dionex. Dionex Corporation se fundó en 1980 en California.
Cómo Funciona la Cromatografía de Intercambio Iónico
La cromatografía de intercambio iónico funciona porque las partículas se "pegan" o "sueltan" basándose en sus cargas eléctricas. Esto es como cuando los imanes se atraen o se repelen. La parte fija de la cromatografía, llamada fase estacionaria, tiene grupos con carga eléctrica en su superficie. Estos grupos interactúan con los iones de la muestra que tienen la carga opuesta.
Existen dos tipos principales de esta cromatografía:
- Cromatografía de intercambio catiónico: Esta técnica retiene (o "atrapa") iones con carga positiva, llamados cationes. Esto ocurre porque la fase estacionaria tiene grupos con carga negativa, como un ácido fosfórico.
- Cromatografía de intercambio aniónico: Esta técnica retiene iones con carga negativa, llamados aniones. Para ello, usa grupos con carga positiva, como un catión de amonio cuaternario.
La fuerza con la que los iones se pegan a la fase estacionaria puede cambiarse. Esto se logra ajustando la cantidad de otros iones en la solución que se mueve a través de la columna (la fase móvil). Al cambiar esto, se puede controlar cuánto tiempo tardan las partículas en salir de la columna.
Separación de Proteínas con Cromatografía
Las proteínas son moléculas grandes que tienen muchas partes con cargas tanto positivas como negativas. La cromatografía de intercambio iónico separa las proteínas según su carga total. Esta carga total puede cambiar dependiendo de la composición de la solución por la que se mueven.
Es posible separar diferentes proteínas ajustando el pH (que indica si una solución es ácida o básica) o la cantidad de iones en la fase móvil. Por ejemplo, si una proteína tiene una carga positiva a un pH de 7, puede unirse a una columna con carga negativa. Una proteína con carga negativa no se uniría. También se puede hacer que una proteína se suelte de la columna cambiando el pH para que su carga total se vuelva negativa.
Cambiar la cantidad de iones en la fase móvil también ayuda a que las proteínas se suelten. Es como si los iones de la fase móvil se "interpusieran" entre la proteína y la fase estacionaria, haciendo que la proteína ya no se quede pegada y pueda salir de la columna.
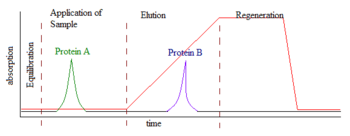
Pasos de la Cromatografía Iónica
Para realizar esta técnica, se introduce una muestra en el equipo. Esto se puede hacer a mano o con una máquina automática. Luego, una solución acuosa especial, llamada fase móvil, lleva la muestra a través de una columna de cromatografía.
La columna contiene la fase estacionaria, que suele ser una resina o un gel. Estos materiales tienen grupos con carga eléctrica unidos a ellos. Los analitos que queremos separar (iones positivos o negativos) se quedan "atrapados" en la fase estacionaria.
Para que los analitos se suelten y salgan de la columna, se aumenta la concentración de otros iones en la fase móvil. Estos nuevos iones "empujan" a los analitos de la fase estacionaria. Por ejemplo, en la cromatografía de intercambio catiónico, los analitos con carga positiva pueden ser liberados añadiendo iones de sodio, que también tienen carga positiva.
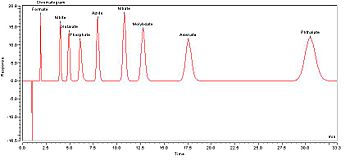
Una vez que los analitos salen de la columna, se pueden detectar de varias maneras. Las más comunes son midiendo su conductividad eléctrica o su capacidad para absorber luz ultravioleta o visible.
Para controlar todo el sistema de cromatografía iónica, se usa un programa de computadora llamado Sistema de Datos Cromatográficos (CDS). Algunos de estos sistemas también pueden controlar otros tipos de cromatografía.
Usos Importantes de la Cromatografía Iónica
Utilidad en la Salud
La cromatografía de intercambio iónico se usa para medir los niveles de hemoglobina glucosilada (HbA1c) en la sangre, lo cual es importante para controlar ciertas condiciones de salud. También se usa para analizar porfirinas y para purificar agua, produciendo agua muy pura en pequeñas cantidades.
Aplicaciones en la Industria
En la industria, esta técnica permite analizar con precisión los líquidos usados en procesos como el electrochapado. Esto es un gran avance, ya que antes se usaban pruebas menos exactas. Con la cromatografía de intercambio iónico, se pueden medir iones, catalizadores y otros aditivos importantes en estos líquidos.
Véase también
- portal:química
- Punto isoeléctrico
- Resina de intercambio catiónico
- Cromatografía
- Cromatografía líquida de alta eficacia