Tiol para niños
En el mundo de la química, un tiol es un tipo de compuesto que tiene un grupo especial llamado "grupo tiol" o "grupo sulfhidrilo". Este grupo está formado por un átomo de azufre y un átomo de hidrógeno, que se unen entre sí (-SH). Piensa en los tioles como los "primos" de los alcoholes, pero en lugar de tener oxígeno en su grupo principal, tienen azufre. La palabra "tiol" viene de la combinación de "tio-" (que significa azufre) y "alcohol".
Muchos tioles tienen un olor muy fuerte, que puede recordar al ajo o a los huevos podridos. Por esta razón, se usan como "odorantes" para el gas natural. El gas natural, por sí solo, no tiene olor, lo que lo haría peligroso si hubiera una fuga. Al añadirle tioles, podemos detectar el "olor a gas" y saber si hay un escape. Los tioles también se conocen como mercaptanos. Este nombre fue creado en 1832 y significa "captador de mercurio" en latín, porque estos compuestos se unen muy fuertemente al mercurio.
Contenido
Etimología: ¿De dónde vienen sus nombres?
El nombre tiol viene de una palabra griega que significa "azufre". Por otro lado, mercaptano viene del latín y significa "capturado por mercurio". Esto se debe a que el grupo -SH de los tioles se une con mucha fuerza al elemento mercurio.
Estructura y cómo se unen
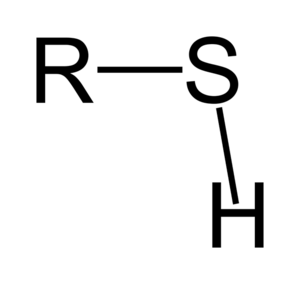
Los tioles tienen una estructura básica donde un grupo de átomos llamado "alquilo" (representado como R) se une al grupo sulfhidrilo (SH). A estos se les llama "alcanotioles". Los compuestos de azufre suelen tener estructuras parecidas a las de los compuestos con oxígeno. Por eso, los tioles se parecen a los alcoholes en su forma.
Como los átomos de azufre son más grandes que los de oxígeno, los enlaces entre el carbono y el azufre, o entre el azufre y el hidrógeno, son más largos que los enlaces correspondientes en los alcoholes. Por ejemplo, un enlace carbono-azufre mide unos 180 picómetros, que es más largo que un enlace carbono-oxígeno. Los ángulos de los enlaces en los tioles también son diferentes a los de los alcoholes.
Los enlaces entre el azufre y el hidrógeno en los tioles son más débiles que los enlaces entre el oxígeno y el hidrógeno en los alcoholes. Además, los enlaces S-H son un poco polares, pero menos polares que los enlaces O-H de los alcoholes.
Nomenclatura: ¿Cómo se nombran los tioles?
Para nombrar los tioles, se usan algunas reglas especiales. La IUPAC (la organización que establece las reglas para nombrar compuestos químicos) dice que se debe cambiar la terminación "-ol" de los alcoholes por "-tiol", "-ditiol", etc., dependiendo de cuántos grupos -SH tenga el compuesto. También se puede usar el nombre del radical orgánico seguido de "mercaptano". Si el grupo tiol no es el principal, se usa el prefijo "mercapto-".
Aquí te explicamos cómo se nombran:
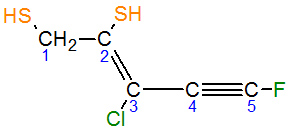
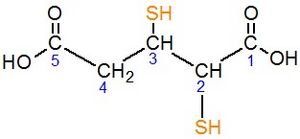
- Se busca la cadena de carbono más larga que contenga los grupos -SH.
- Se numera la cadena para que los carbonos con los grupos -SH tengan los números más bajos posibles.
- Se nombra la cadena principal según el número de carbonos (por ejemplo, "etano-" para dos, "propano-" para tres).
- Se indican los números de los carbonos donde están los grupos -SH.
- Se añade la terminación "-tiol" si hay un grupo -SH, "-ditiol" si hay dos, y así sucesivamente.
Algunos ejemplos:
- CH3-SH se llama metanotiol.
- CH3-CH2-CH2-SH se llama 1-propanotiol.
- CH2SH-CH2-CH2-CH2-SH se llama butano-1,4-ditiol.
Si el grupo -SH no es el grupo principal, se usa el prefijo "mercapto". Por ejemplo, HSCH2CH2SH se llama 2-mercaptoetanol.
También existe un sistema de nombres más común:
- Se nombra primero el radical alquilo y luego la palabra "mercaptano".
- Ejemplos: CH3-SH es metil mercaptano; CH3-CH2-CH2-SH es propil mercaptano.
Propiedades químicas: ¿Cómo reaccionan los tioles?
¿Cómo se obtienen los tioles?
Los tioles se pueden crear de formas parecidas a como se hacen los alcoholes. Las reacciones son más rápidas y eficientes porque los átomos de azufre son muy reactivos.
Una forma de obtener tioles es calentando un compuesto llamado haloalcano con una solución de sulfuro ácido de sodio.
- <chem>CH3CH2Br + NaHS -> CH3CH2SH + NaBr</chem>
Otra forma es usando tiourea, que es muy reactiva, y luego hidrolizándola. Además, algunos compuestos llamados disulfuros pueden transformarse en dos tioles usando agentes reductores.
- <chem>R-S-S-R' -> R-SH + R'-SH</chem>
Reacciones de los tioles
El grupo tiol es como el grupo hidroxilo de los alcoholes, pero con azufre. Como el azufre y el oxígeno están en el mismo grupo de la tabla periódica, tienen propiedades de unión similares. La forma de tiol sin un protón (llamada tiolato) es más reactiva que la forma con protón.
Los tioles son muy reactivos y participan en muchos procesos importantes en la naturaleza. Reaccionan con iones de metales pesados, como el mercurio, formando compuestos que no se disuelven. Por eso se les dio el nombre de "mercaptanos".
La química de los tioles es parecida a la de los alcoholes: los tioles forman compuestos como tioéteres y tioésteres, que son similares a los éteres y ésteres. Una diferencia importante es que los tioles se oxidan mucho más fácilmente. Con oxidantes suaves, se convierten en disulfuros. Con oxidantes fuertes, se transforman en ácidos sulfónicos.
Acidez de los tioles
El átomo de azufre en un tiol es muy reactivo. El grupo tiol es bastante ácido. Cuando hay una base, se forma un anión tiolato, que es muy potente. Este grupo y su anión se oxidan fácilmente, por ejemplo, con bromo, para formar disulfuros orgánicos.
- <chem>2R-SH + Br2 -> R-S-S-R + 2HBr</chem>
Si se usan oxidantes más fuertes, como el hipoclorito de sodio, se forman ácidos sulfónicos.
- <chem>2R-SH + 2H2O2 -> R-SO3H + 2H2O</chem>
Propiedades físicas: ¿Cómo son los tioles?
Olor de los tioles
Muchos tioles tienen un olor fuerte, similar al ajo. Los tioles con pocos átomos, en particular, suelen tener olores intensos y desagradables. Por ejemplo, el aerosol que usan las mofetas para defenderse está hecho principalmente de tioles. Los humanos pueden detectar estos compuestos en cantidades muy pequeñas.
No todos los tioles huelen mal. Por ejemplo, un tiol llamado furan-2-ilmetanotiol contribuye al delicioso aroma del café tostado. Otro tiol, el mercaptano de pomelo, es el responsable del olor característico del pomelo, pero solo en bajas concentraciones. Si este mercaptano está puro, su olor es desagradable.
En Estados Unidos, después de un accidente en una escuela en 1937, se hizo obligatorio añadir tioles al gas natural (que no huele) para poder detectar fugas. Hoy en día, la mayoría de los odorantes de gas son mezclas de mercaptanos y sulfuros. En la industria, cuando se usan tioles, se utilizan catalizadores especiales para eliminar su olor.
Usos de los tioles
- Algunos mercaptanos de cadena corta, como el metilmercaptano, se añaden al gas doméstico para que las personas puedan detectar fugas gracias a su fuerte olor a huevos podridos.
Véase también
 En inglés: Thiol Facts for Kids
En inglés: Thiol Facts for Kids